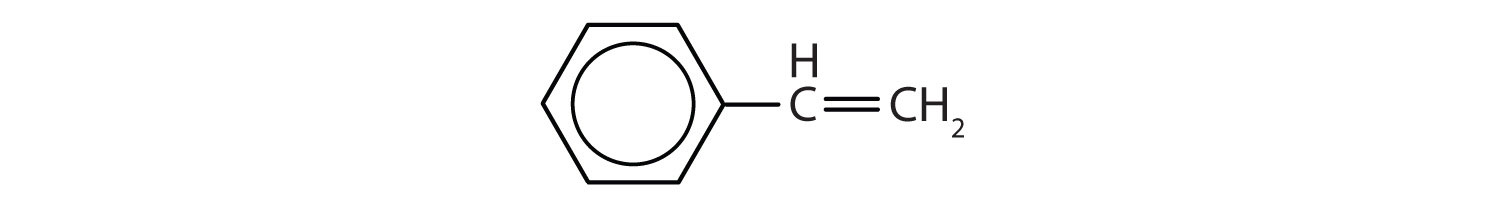
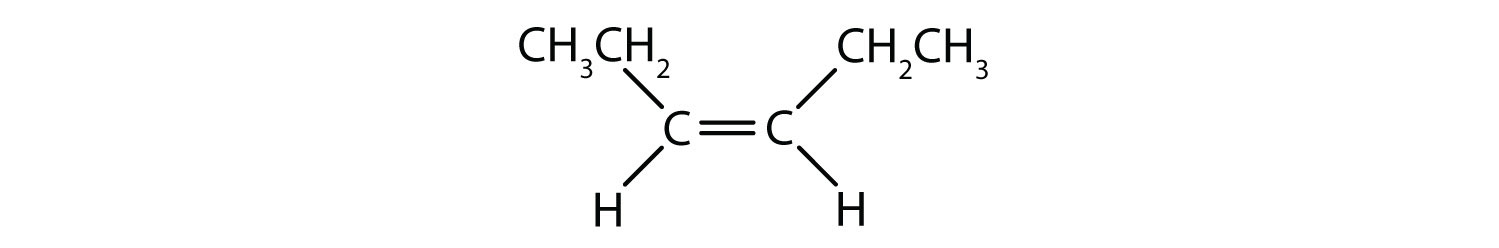
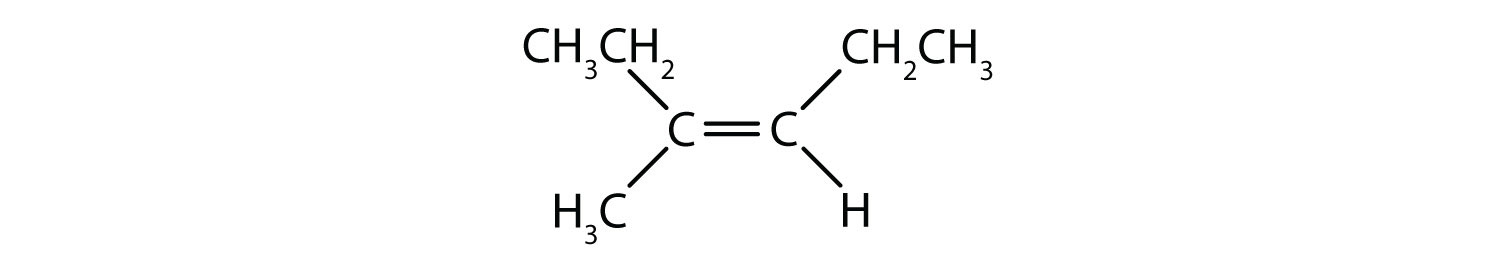
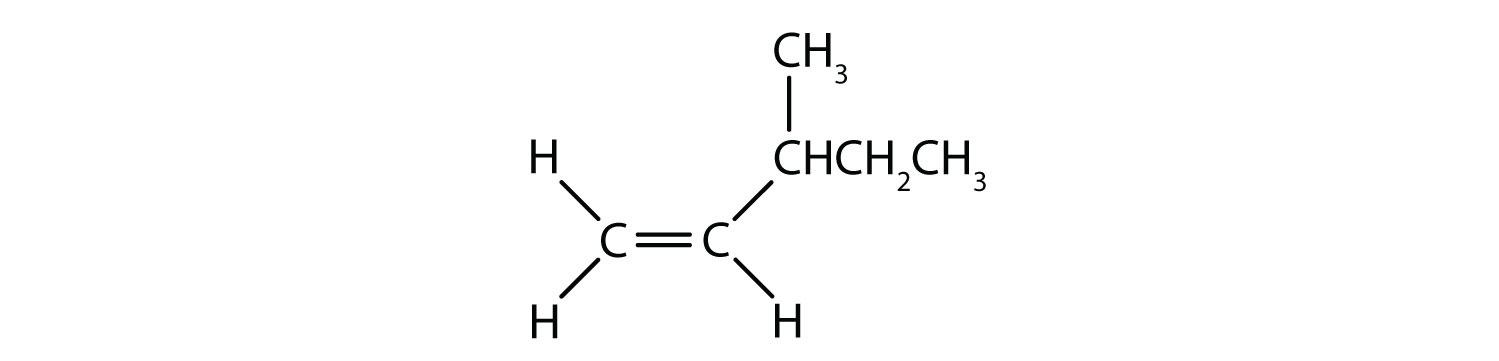
Aromaattiset hiilivedyt määritellään siten, että niillä on 6-jäseniset rengasrakenteet, joissa on vuorottelevia kaksoissidoksia (kuva 8.2).
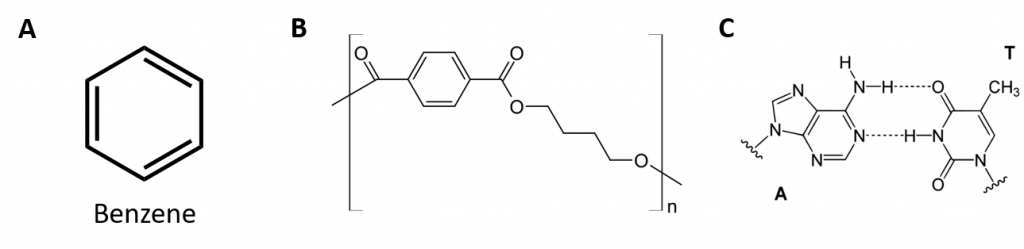
Kuva 8.2: Aromaattiset hiilivedyt. Aromaattiset hiilivedyt sisältävät 6-jäsenisen bentseenirengasrakenteen (A), jolle on ominaista vuorottelevat kaksoissidokset. Ultradur, PBT on muovipolymeeri, joka sisältää aromaattisen funktionaalisen ryhmän. Ultradurin toistuva monomeeri on esitetty kuvassa (B). Ultraduria käytetään suihkuputkissa, hammasharjan harjaksissa, kuituoptisten kaapeleiden muovikoteloissa sekä autojen ulko- ja sisäosissa. Biologisesti tärkeät molekyylit, kuten deoksiribonukleiinihappo, DNA (C) sisältävät myös aromaattisia rengasrakenteita.
Siten niiden kaavat voidaan piirtää syklisiksi alkeeneiksi, jolloin ne ovat tyydyttymättömiä. Syklisen rakenteen vuoksi aromaattisten renkaiden ominaisuudet ovat kuitenkin yleensä varsin erilaiset, eivätkä ne käyttäydy kuten tyypilliset alkeenit. Aromaattiset yhdisteet toimivat perustana monille lääkkeille, antiseptisille aineille, räjähdysaineille, liuottimille ja muoveille (esim. polyesterit ja polystyreeni).
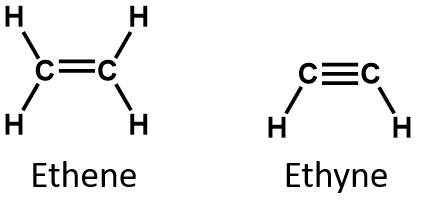
Kahdesta yksinkertaisimmasta tyydyttymättömästä yhdisteestä – etyleenistä (eteeni) ja asetyleenistä (etyyni) – käytettiin aikoinaan anestesia-aineina, ja ne otettiin käyttöön lääketieteen alalla vuonna 1924. Havaittiin kuitenkin, että asetyleeni muodostaa räjähtäviä seoksia ilman kanssa, joten sen lääketieteellisestä käytöstä luovuttiin vuonna 1925. Etyleeniä pidettiin turvallisempana, mutta sekin oli osallisena lukuisissa kuolemaan johtaneissa tulipaloissa ja räjähdyksissä anestesian aikana. Siitä huolimatta se säilyi tärkeänä anestesia-aineena 1960-luvulle asti, jolloin se korvattiin palamattomilla anestesia-aineilla, kuten halotaanilla (CHBrClCF3).
- (Takaisin alkuun)
- 8.1 Alkeenin ja alkyynin yleiskatsaus
- (Takaisin alkuun)
- 8.2 Alkeneiden ominaisuudet
- Looking Closer: Environmental Note
- Konseptin kertausharjoitukset
- Vastaukset
- Key Takeaway
- Harjoituksia
- Vastaus
- Käsitteiden kertausharjoitukset
- Vastaukset
- Keskeinen merkitys
- 8.3 Alkyynit
- Huomautus
- Käsitteiden kertausharjoitukset
- Key Takeaway
- Harjoitukset
- (Back to the Top)
- 8.4 Aromaattiset yhdisteet: Bentseeni
- Huomautus
- Terveydelle: Bentseeni ja me
- Käsitteiden kertausharjoitukset
- Aromaattisten yhdisteiden tunnistaminen
- Taidonrakentamisharjoitus
- Key Takeaway
- (Takaisin alkuun)
- Polysykliset aromaattiset hiilivedyt
- Terveydelle: Polysykliset aromaattiset hiilivedyt ja syöpä
- Biologisesti tärkeät yhdisteet, joissa on bentseenirengas
- Huomautus
- 8.5 Geometriset isomeerit
- Klikkaa tästä Kahn-akatemian video-opetusohjelma alkeenin rakenteesta.
- Cis-trans-nimikkeistö
- Click Here for a Kahn Academy Video Tutorial on Cis/Trans Isomerization
- Terveydellesi
- Click Here for a Kahn Academy Video Tutorial on Saturated-, Unsaturated-, and Trans-Fats
- Key Factors for Determining Cis/Trans Isomerization
- Työskentelyesimerkki
- Taitotehtävä
- Käsitteiden kertausharjoitukset
- Vastaukset
- Key Takeaway
- (Takaisin alkuun)
- E-Z-nimikkeistö
- Klikkaa tästä Kahn Academyn video-opetusta E/Z-isomerisaatiosta.
- (Takaisin alkuun)
(Takaisin alkuun)
8.1 Alkeenin ja alkyynin yleiskatsaus
Määritelmän mukaan alkeenit ovat hiilivetyjä, joissa on yksi tai useampi hiili-hiili-kaksoissidos (R2C=CR2), kun taas alkyynit ovat hiilivetyjä, joissa on yksi tai useampi hiili-hiili-kolmisidos (R-C≡C-R). Yhdessä niitä kutsutaan tyydyttymättömiksi hiilivedyiksi, jotka määritellään hiilivedyiksi, joilla on yksi tai useampi moninkertainen (kaksois- tai kolmoissidos) hiiliatomien välillä. Kaksois- tai kolmoissidosten luonteen vuoksi alkeenit ja alkyynit sisältävät vähemmän vetyatomeja kuin vastaavat alkaanit, joissa on sama määrä hiiliatomeja. Matemaattisesti tämä voidaan ilmaista seuraavilla yleisillä kaavoilla:
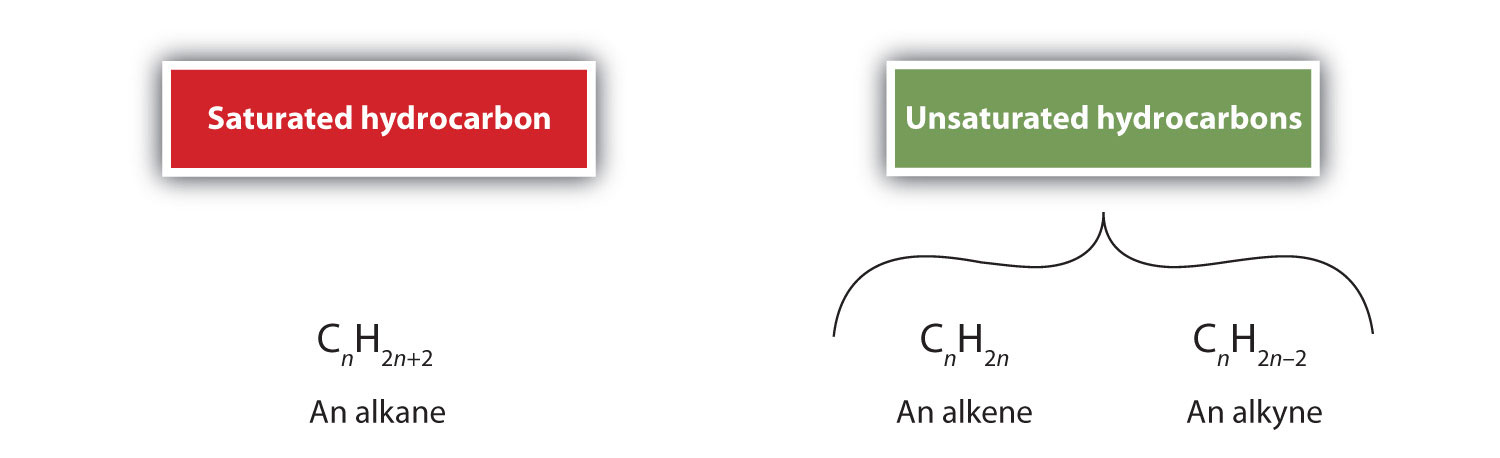
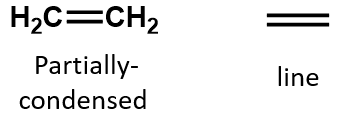
Alkeneenissä kaksoissidos on kahden hiiliatomin yhteinen eikä siihen liity vetyatomeja, vaikkakaan tiivistetty kaava ei tee tätä selväksi, eli eteenin tiivistetty kaava on CH2CH2. Molekyylin kaksois- tai kolmoissidoksen luonnetta on vielä vaikeampi havaita molekyylikaavoista. Huomaa, että etenin molekyylikaava on C2H4, kun taas etyynin molekyylikaava on C2H2. Niinpä siihen asti, kunnes orgaanisen kemian kieli tulee tutummaksi, on usein hyödyllisintä piirtää viivamaiset tai osittain kondensoituneet rakenteet, kuten alla on esitetty:
(Takaisin alkuun)
8.2 Alkeneiden ominaisuudet
Alkeneiden fysikaaliset ominaisuudet ovat samankaltaisia kuin alkaaneilla. Taulukosta 8.1 nähdään, että suoraketjuisten alkeenien kiehumispisteet kasvavat molaarisen massan kasvaessa, aivan kuten alkaaneilla. Molekyyleillä, joilla on sama määrä hiiliatomeja ja sama yleinen muoto, kiehumispisteet eroavat yleensä vain vähän toisistaan, aivan kuten voisimme odottaa aineilta, joiden moolimassa eroaa vain 2 u (vastaa kahta vetyatomia). Muiden hiilivetyjen tavoin alkeenit ovat liukenemattomia veteen mutta liukenevat orgaanisiin liuottimiin.
Joitakin edustavia alkeeneita – niiden nimet, rakenteet ja fysikaaliset ominaisuudet – on esitetty taulukossa 8.1.
Taulukko 8. Alkeenit.1 Joidenkin valikoitujen alkeneiden fysikaaliset ominaisuudet
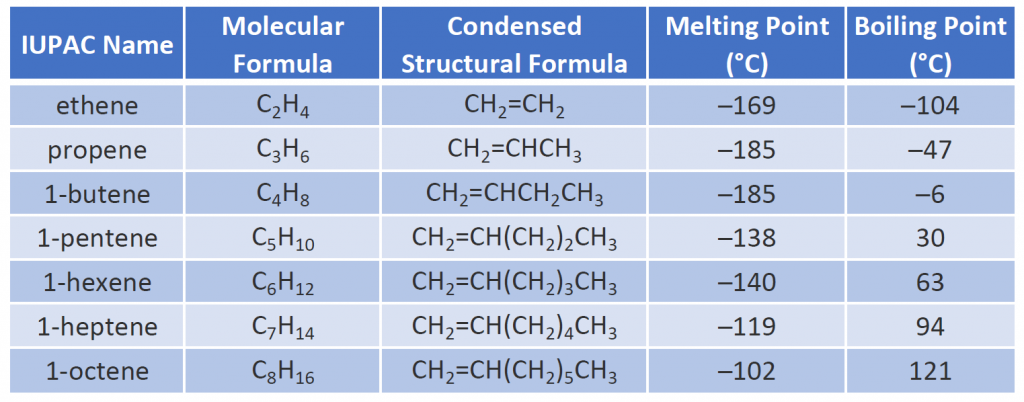
Taulukon 8.1 kahta ensimmäistä alkeenia -eteeniä ja propeenia – kutsutaan useimmiten yleisimmin niiden yleisnimillä -eteeni ja propeeni. Etyleeni on merkittävä kaupallinen kemikaali. Yhdysvaltain kemianteollisuus tuottaa vuosittain noin 25 miljardia kiloa eteeniä, enemmän kuin mitään muuta synteettistä orgaanista kemikaalia. Yli puolet tästä eteenistä käytetään polyeteenin valmistukseen, joka on yksi tunnetuimmista muoveista. Propyleeni on myös tärkeä teollisuuskemikaali. Siitä valmistetaan muoveja, isopropyylialkoholia ja monia muita tuotteita.
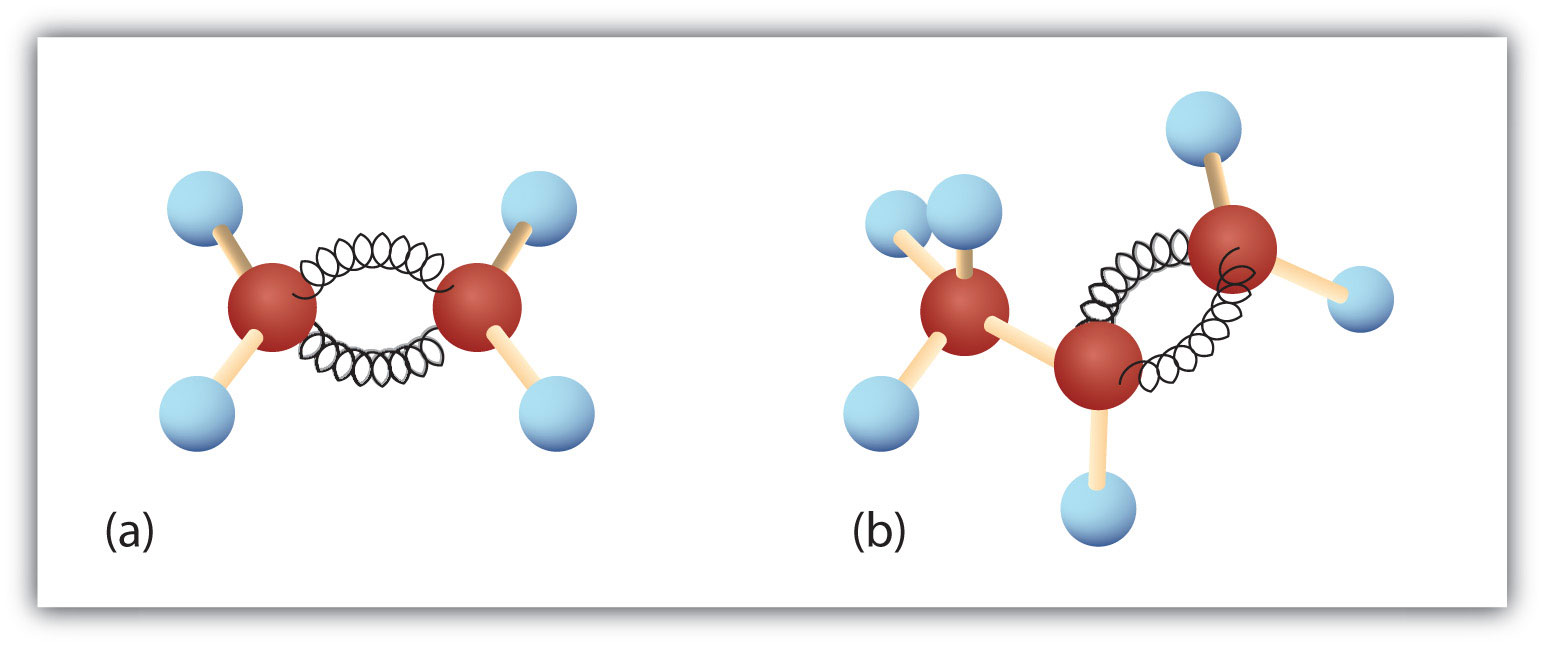
Kuva 8.3. Eteeni ja propeeni. Eteenin/eteenin (a) ja propeenin/propeenin (b) pallo- ja jousimalleista nähdään niiden muodot ja erityisesti sidoskulmat.
Looking Closer: Environmental Note
Alkeneja esiintyy luonnossa laajalti. Kypsyvät hedelmät ja vihannekset erittävät etyleeniä, joka käynnistää lisäkypsymisen. Hedelmänjalostajat lisäävät etyleeniä keinotekoisesti nopeuttaakseen kypsymisprosessia; altistuminen vain 0,1 mg:lle etyleeniä 24 tunnin ajan voi kypsyttää 1 kg tomaatteja. Valitettavasti tämä prosessi ei täysin vastaa kypsymisprosessia, eivätkä vihreinä poimitut ja tällä tavoin käsitellyt tomaatit maistu juurikaan samalta kuin viiniköynnöskypsytetyt tomaatit, jotka on poimittu tuoreena puutarhasta.
Muita luonnossa esiintyviä alkeeneita ovat mm. 1-okteeni, joka on sitruunaöljyn ainesosa, ja kalanmaksassa esiintyvä oktaadekeeni (C18H36). Dienit (kaksi kaksoissidosta) ja polyeenit (kolme tai useampi kaksoissidos) ovat myös yleisiä. Butadieeniä (CH2=CHCH=CH=CH2) esiintyy kahvissa. Lykopeeni ja karoteenit ovat isomeerisiä polyeeniä (C40H56), jotka antavat vesimelonille, tomaateille, porkkanoille ja muille hedelmille ja vihanneksille houkuttelevat punaiset, oranssit ja keltaiset värit. Hyvän näkökyvyn kannalta välttämätön A-vitamiini on peräisin karoteenista. Maailma olisi paljon vähemmän värikäs paikka ilman alkeneja.

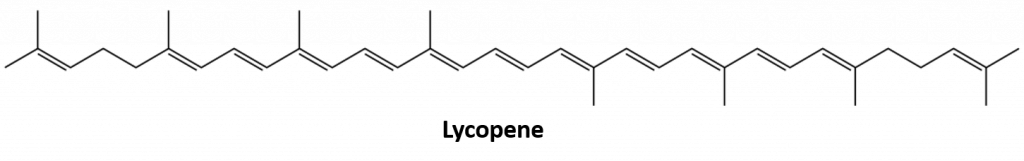
Kuva 8.4 Tomaattien kirkkaanpunainen väri johtuu lykopeenistä.
Kuva lähteestä : © Thinkstock; Lykopeenin rakenne lähteestä: Jeff Dahl
Konseptin kertausharjoitukset
-
Kuvaile lyhyesti alkeenien fysikaalisia ominaisuuksia. Miten nämä ominaisuudet vertautuvat alkaanien ominaisuuksiin?
-
Järjestä seuraavat alkeenit taulukoita katsomatta kiehumispisteen mukaisessa järjestyksessä:

Vastaukset
-
Alkeenien fysikaalisten ominaisuuksien (matalat kiehumispisteet, liukenematon vesiliukoisuuteen) perusteella ne ovat melko samankaltaisia kuin vastaaviensa alkaanien.
-
eteeni < propeeni < 1-buteeni < 1-hekseeni
Key Takeaway
- Alkeneiden fysikaaliset ominaisuudet muistuttavat paljolti vastaavien alkaanien fysikaalisten ominaisuuksien ominaisuuksia: kiehumispisteet kasvavat moolimassan kasvaessa, ja ne ovat veteen liukenemattomia.
Harjoituksia
-
Viittaamatta taulukkoon tai muuhun viitteeseen ennusta, kummalla kunkin parin jäsenellä on korkeampi kiehumispiste.
- 1-penteni vai 1-buteeni
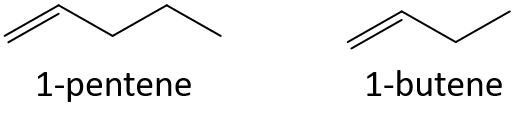
- 3-hepteeni vai 3-noneni
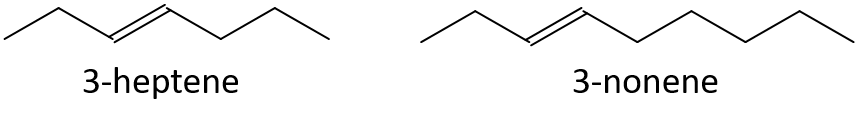
- 1-penteni vai 1-buteeni
-
Kumpi on hyvä liuotin syklohekseenille, pentaani vai vesi?
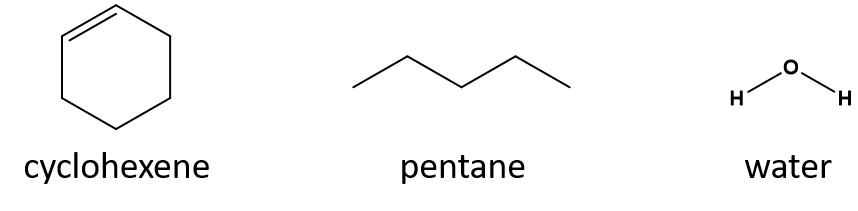
Vastaus
-
- 1-penteni
- 3- -noneeni
Käsitteiden kertausharjoitukset
-
Lyhyesti tyydyttyneen hiilivedyn ja tyydyttymättömän hiilivedyn tärkeät erot.
-
Tunnista lyhyesti alkeenin ja alkaanin väliset tärkeät erot.
-
Luokittele kukin yhdiste tyydyttyneeksi tai tyydyttymättömäksi. Tunnista kukin alkaani, alkeeni tai alkiini.
-
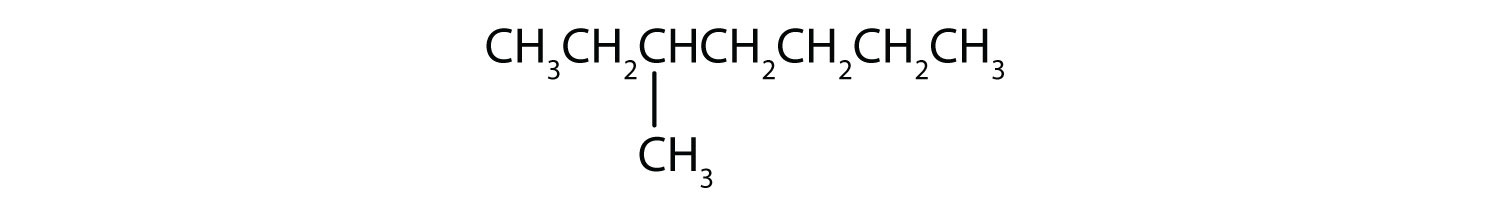
- CH3CH2C≡CCH3
-

-
Vastaukset
-
Tyydyttymättömillä hiilivedyillä on kaksois- tai kolmoissidoksia ja ne ovat melko reaktiivisia; tyydyttyneillä hiilivedyillä on vain yksinkertaisia sidoksia ja ne ovat melko epäreaktiivisia.
-
Alkeenissa on kaksoissidoksia; alkaaneissa on vain yksinkertaisia sidoksia.
-
- tyydyttymätön; alkaani
- tyydyttymätön; alkiini
- tyydyttymätön; alkeeni
Keskeinen merkitys
- Alkeneet ovat hiilivetyjä, joissa on hiilen ja hiilen välinen kaksoissidos.
8.3 Alkyynit
Yksinkertaisimmalla alkyynillä – hiilivetyllä, jolla on hiilestä hiileen ulottuva kolmoissidos – on molekyylikaava C2H2, ja se tunnetaan yleisnimellä asetyleeni (kuva 8.5). Sen rakenne on H-C≡C-H.
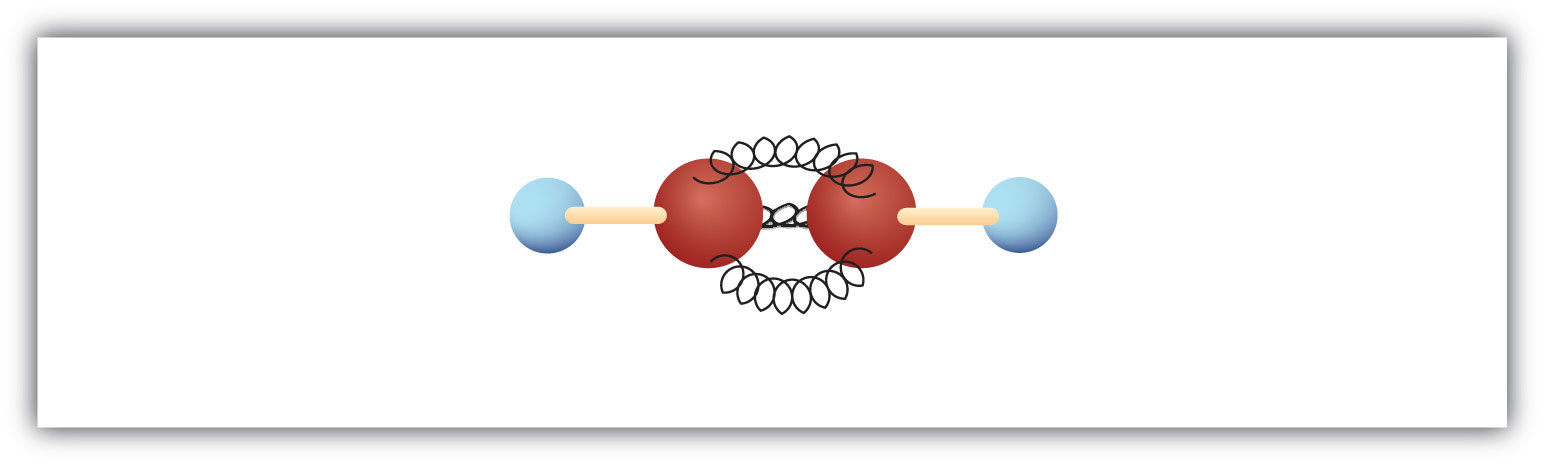
Kuva 8.5 Asetyleenin pallo-jousimalli. Asetyleeni (etyyni) on alkyyniperheen yksinkertaisin jäsen.
Huomautus
Asetyleeniä käytetään happiasetyleenipolttimissa metallien leikkaamiseen ja hitsaamiseen. Tällaisen polttimen liekki voi olla hyvin kuuma. Suurin osa asetyleenistä muutetaan kuitenkin kemiallisiksi välituotteiksi, joita käytetään vinyyli- ja akryylimuovien, kuitujen, hartsien ja monien muiden tuotteiden valmistukseen.
Alkyynit muistuttavat sekä fysikaalisilta että kemiallisilta ominaisuuksiltaan alkeeneita. Esimerkiksi alkyynit käyvät läpi monia alkeenien tyypillisiä additioreaktioita. Kansainvälisen puhtaan ja soveltavan kemian liiton (International Union of Pure and Applied Chemistry, IUPAC) alkyneiden nimet ovat samansuuntaisia kuin alkeenien nimet, paitsi että suvun pääte on -yne eikä -ene. Asetyleenin IUPAC-nimi on etyyni. Muiden alkyneiden nimiä havainnollistetaan seuraavissa harjoituksissa.
Käsitteiden kertausharjoitukset
-
Kertaa lyhyesti alkeenin ja alkyynin väliset tärkeät erot. Miten ne ovat samankaltaisia?
-
Alkiini (CH3)2CHCHCH2CH=CH2 on nimeltään 4-metyyli-1-penteni. Mikä on (CH3)2CHCHCH2C≡CH:n nimi?
-
Onko alkeneissa cis-trans-isomeriaa? Selitä.
Vastaukset
-
Alkeneilla on kaksoissidoksia, alkyyneillä kolmoissidoksia. Molemmat käyvät läpi additioreaktioita.
-
4-metyyli-1-pentyleeni
-
Ei; kolminkertaisesti sitoutunut hiiliatomi voi muodostaa vain yhden toisen sidoksen. Siihen pitäisi liittyä kaksi ryhmää, jotta se osoittaisi cis-trans-isomeriaa.
Key Takeaway
- Alkynit ovat hiilivetyjä, joilla on hiilen ja hiilen välisiä kolmoissidoksia ja jotka muistuttavat ominaisuuksiltaan paljon alkeenien ominaisuuksia.
Harjoitukset
-
Piirrä kunkin yhdisteen rakenne.
- Asetyleeni
- 3-metyyli-1-heksiini
-
Piirrä kunkin yhdisteen rakenne.
- 4-metyyli-2-heksiini
- 3-oktyyni
-
Nimeä kukin alkiini.
- CH3CH2CH2C≡CH
- CH3CH2CH2C≡CCH3
Vastaukset
-
- H-C≡C-H
-
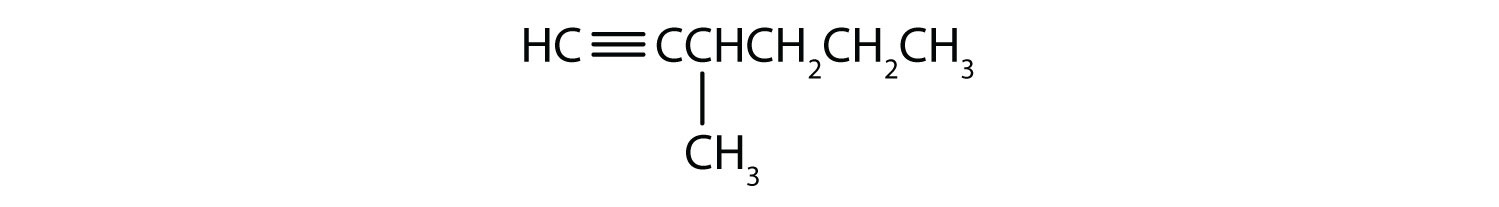
-
- 1-pentyne
- 2-heksiini
(Back to the Top)
8.4 Aromaattiset yhdisteet: Bentseeni
Seuraavaksi tarkastelemme hiilivetyjen luokkaa, jonka molekyylikaavat muistuttavat tyydyttymättömien hiilivetyjen molekyylikaavoja, mutta jotka, toisin kuin alkeenit, eivät helposti käy läpi additioreaktioita. Nämä yhdisteet muodostavat erillisen luokan, jota kutsutaan aromaattisiksi hiilivedyiksi. Aromaattiset hiilivedyt ovat yhdisteitä, jotka sisältävät bentseenirengasrakenteen.Yksinkertaisin aromaattinen yhdiste on bentseeni (C6H6), ja sillä on suuri kaupallinen merkitys, mutta sillä on myös huomattavia haitallisia terveysvaikutuksia (ks. ”Terveydelle: bentseeni ja me”).
Kaava C6H6 näyttäisi viittaavan siihen, että bentseenillä on korkea tyydyttymättömyysaste. (Heksaanin, tyydyttyneen hiilivedyn, jossa on kuusi hiiliatomia, kaava on C6H14 – kahdeksan vetyatomia enemmän kuin bentseenillä). Näennäisen alhaisesta tyydyttyneisyysasteesta huolimatta bentseeni on kuitenkin melko reagoimaton. Tämä johtuu aromaattisen renkaan vuorottelevasta kaksoissidosrakenteesta muodostuvasta resonanssirakenteesta.

Huomautus
Bentseeni on neste, joka haisee bensiiniltä, kiehuu 80 °C:ssa ja jäätyy 5,5 °C:ssa. Se on aromaattinen hiilivety, jota tuotetaan eniten. Sitä käytettiin aiemmin kahvin kofeiinipoistoon ja se oli merkittävä komponentti monissa kuluttajatuotteissa, kuten maalinpoistoaineissa, kumisementeissä ja kodin kemiallisen pesun tahranpoistoaineissa. Se poistettiin monista tuotevalmisteista 1950-luvulla, mutta toiset jatkoivat bentseenin käyttöä tuotteissa 1970-luvulle asti, jolloin se yhdistettiin leukemiakuolemiin. Bentseeni on edelleen tärkeä teollisuuden raaka-aine muovien (kuten styroksin ja nailonin), lääkkeiden, pesuaineiden, synteettisen kumin, torjunta-aineiden ja väriaineiden valmistuksessa. Sitä käytetään liuottimena esimerkiksi painolaitteiden puhdistuksessa ja huollossa sekä liimoissa, joita käytetään esimerkiksi kengänpohjien kiinnittämiseen. Bentseeni on öljytuotteiden luonnollinen ainesosa, mutta koska se on tunnettu syöpää aiheuttava aine, sen käyttöä bensiinin lisäaineena on nykyään rajoitettu.
Terveydelle: Bentseeni ja me
Suurin osa kaupallisesti käytetystä bentseenistä on peräisin maaöljystä. Sitä käytetään pesuaineiden, lääkkeiden, väriaineiden, hyönteismyrkkyjen ja muovien valmistuksen lähtöaineena. Aikoinaan laajalti orgaanisena liuottimena käytetyllä bentseenillä tiedetään nykyään olevan sekä lyhyt- että pitkäaikaisia myrkyllisiä vaikutuksia. Suurten pitoisuuksien hengittäminen voi aiheuttaa pahoinvointia ja jopa kuoleman hengitys- tai sydämen vajaatoiminnan vuoksi, kun taas toistuva altistuminen johtaa etenevään sairauteen, jossa luuytimen kyky muodostaa uusia verisoluja lopulta tuhoutuu. Tämä johtaa tilaan nimeltä aplastinen anemia, jossa sekä punasolujen että valkosolujen määrä vähenee.
Käsitteiden kertausharjoitukset
-
Miten bentseenin tyypilliset reaktiot eroavat alkeenien reaktioista?
-
Kuvaile lyhyesti bentseenin sidoksia.
-
Mitä ympyrä tarkoittaa kemistin esityksessä bentseenistä?
Vastaukset
-
Bentseeni on alkeeniin verrattuna melko epäreaktiivinen additioreaktioihin nähden.
-
Valenssielektronit jakautuvat tasaisesti kaikkien kuuden hiiliatomin kesken (eli elektronit ovat delokalisoituneita).
-
Kuusi elektronia on jaettu tasan kaikkien kuuden hiiliatomin kesken.
Aromaattisten yhdisteiden tunnistaminen
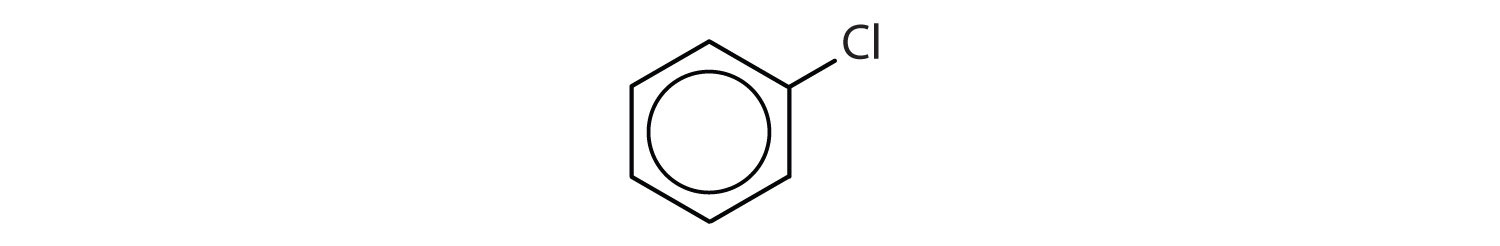
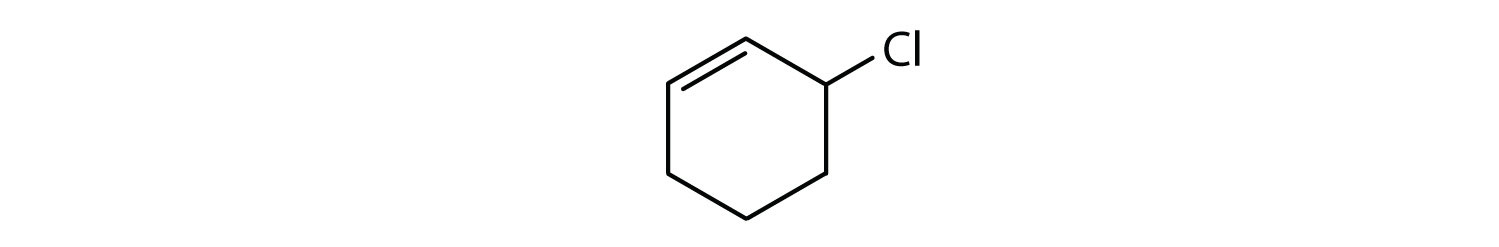
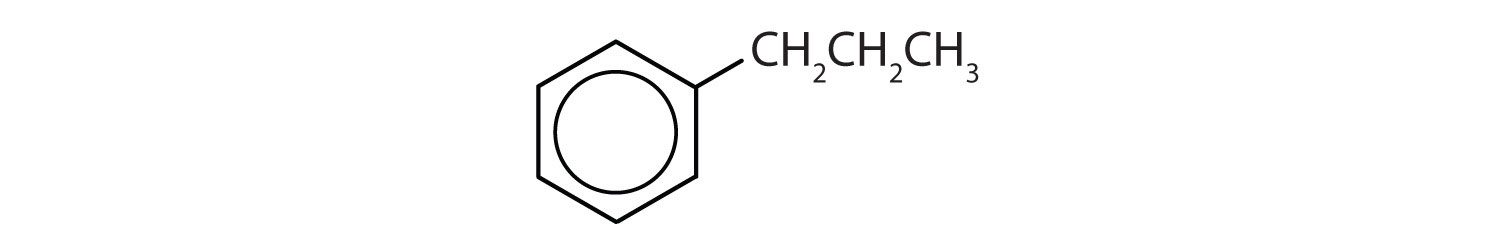
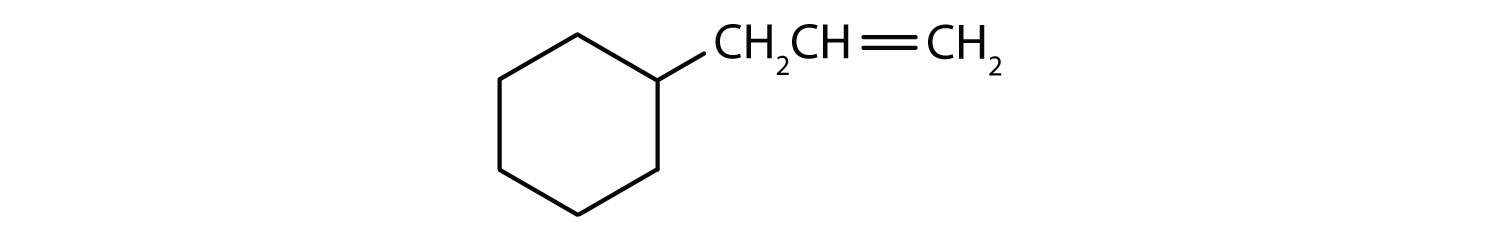
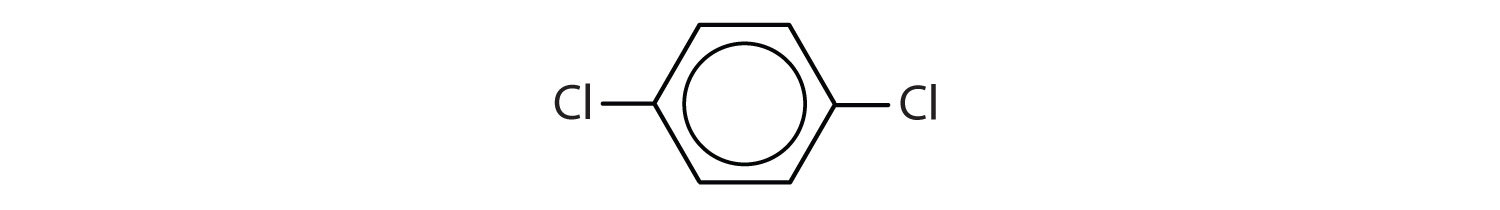
Mitkä yhdisteet ovat aromaattisia?
Liuos
- Yhdisteellä on bentseenirengas (jossa yksi vetyatomi on korvattu klooriatomilla); se on aromaattinen.
- Yhdiste on syklinen, mutta sillä ei ole bentseenirengasta; se ei ole aromaattinen.
- Yhdisteellä on bentseenirengas (jossa yksi vetyatomi on korvattu propyyliryhmällä); se on aromaattinen.
- Yhdiste on syklinen, mutta sillä ei ole bentseenirengasta; se ei ole aromaattinen.
Taidonrakentamisharjoitus
Mitkä yhdisteet ovat aromaattisia?
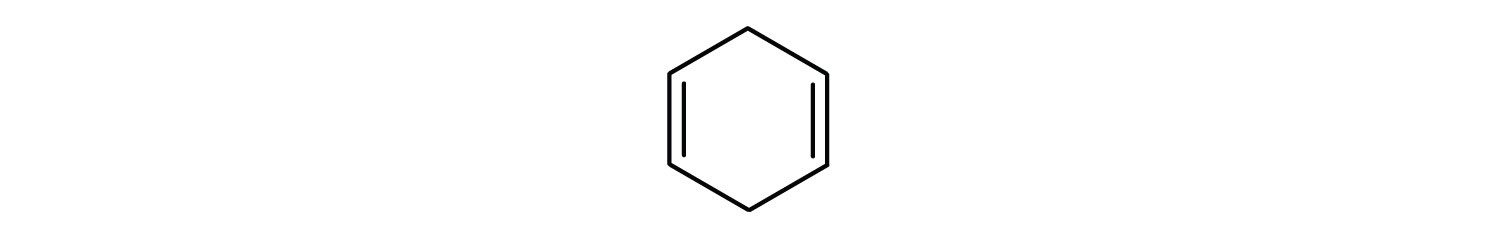
-
Internationaalisen puhtaan ja soveltavan kemian liiton (IUPAC) systeemissä aromaattiset hiilivedyt nimetään bentseenin johdannaisiksi. Alla on esitetty viisi esimerkkiä. Näissä rakenteissa ei ole merkitystä sillä, onko yksittäinen substituentti kirjoitettu renkaan ylä-, sivu- vai alapuolelle: kuusikulmio on symmetrinen, ja siksi kaikki paikat ovat ekvivalentteja.
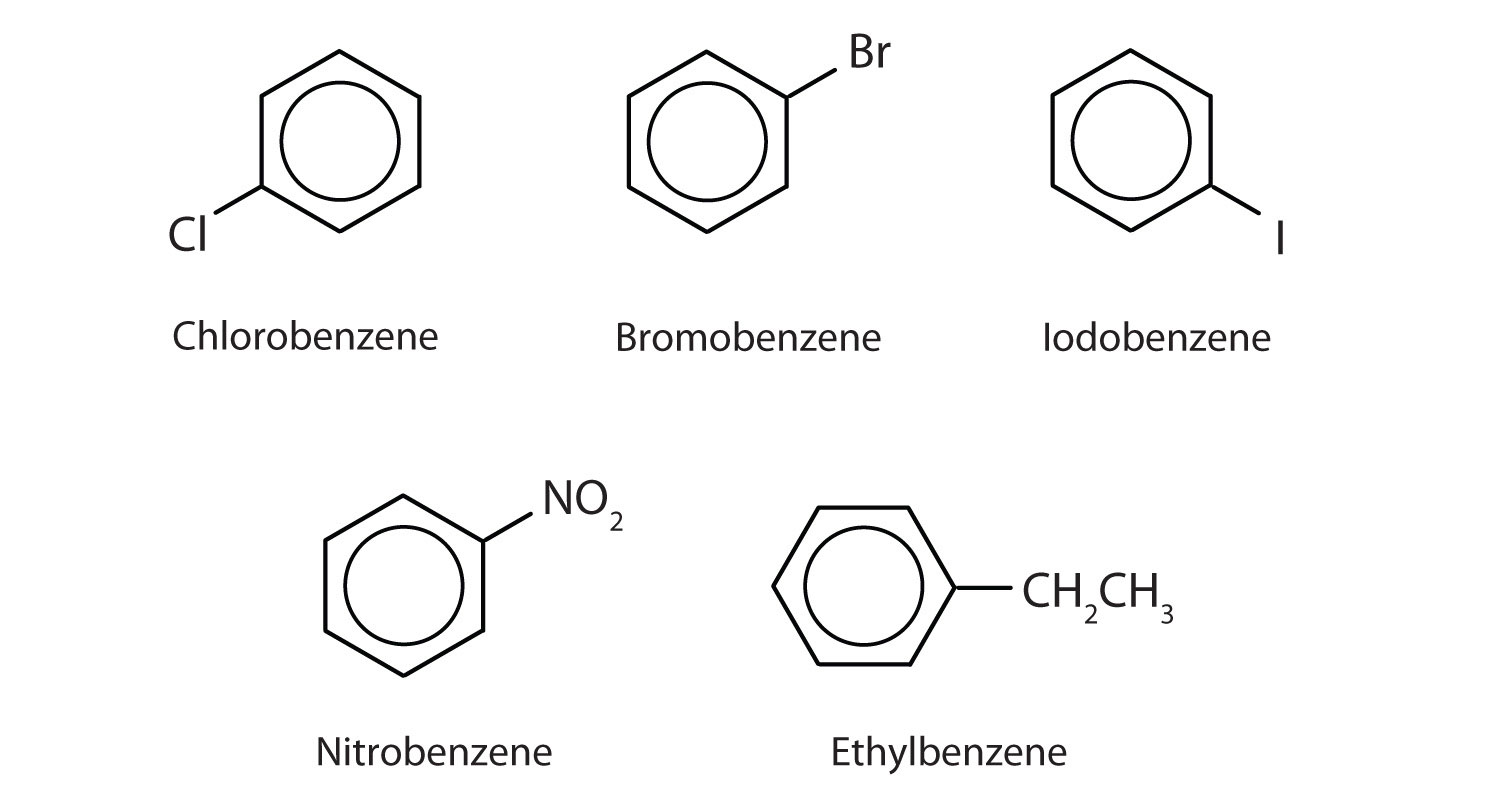
Nämä yhdisteet nimetään tavalliseen tapaan siten, että vetyatomin korvaava ryhmä nimetään substituenttiryhmäksi: Cl klooriksi, Br bromiksi, I jodiksi, NO2 nitroksi ja CH3CH2 etyyliksi.
Vaikka joihinkin yhdisteisiin viitataan yksinomaan IUPAC-nimillä, joihinkin yhdisteisiin viitataan useammin yleisnimillä, kuten seuraavassa on esitetty.
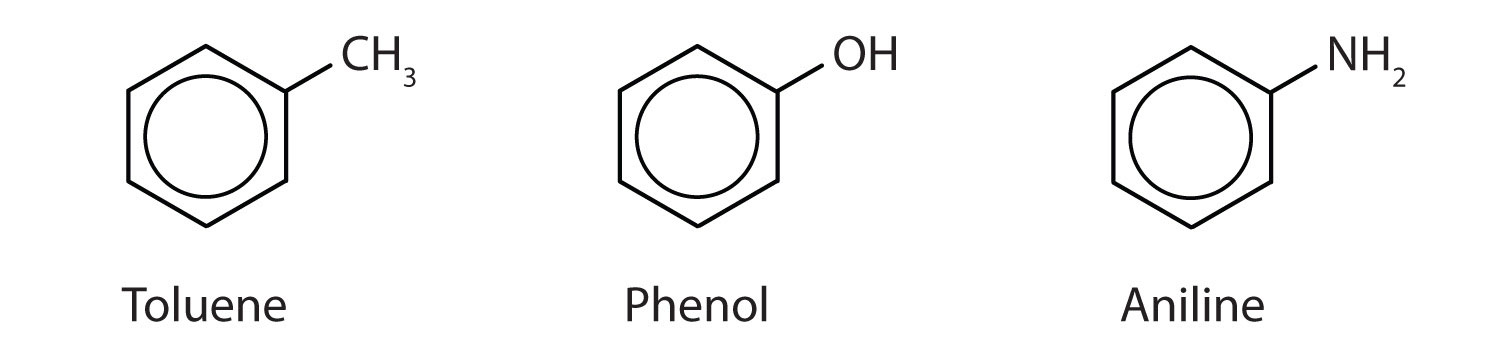
Key Takeaway
- Aromaattiset hiilivedyt näyttävät olevan tyydyttymättömiä, mutta niillä on erityyppinen sidos eivätkä ne käy läpi additioreaktioita.
(Takaisin alkuun)
Polysykliset aromaattiset hiilivedyt
Jotkut tavalliset aromaattiset hiilivedyt koostuvat fuusioituneista bentseenirenkaista – renkaista, joilla on yhteinen sivu. Näitä yhdisteitä kutsutaan polysyklisiksi aromaattisiksi hiilivedyiksi (PAH-yhdisteiksi)Aromaattinen hiilivety, joka koostuu sulautuneista bentseenirenkaista, joilla on yhteinen sivu..
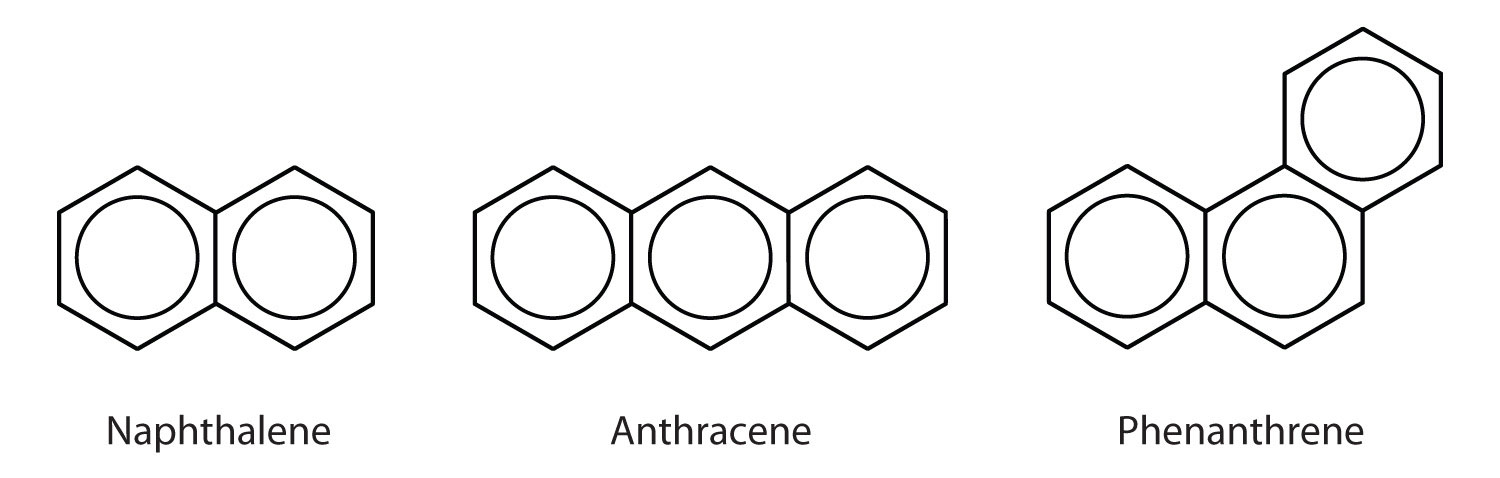
Kolme tässä esitettyä esimerkkiä ovat värittömiä, kiteisiä kiinteitä aineita, joita saadaan yleensä kivihiilitervasta. Naftaleenilla on pistävä haju ja sitä käytetään koipalloissa. Antraseenia käytetään tiettyjen väriaineiden valmistuksessa. Steroidit, kuten kolesteroli ja hormonit, estrogeeni ja testosteroni, sisältävät fenantreenirakennetta.
Terveydelle: Polysykliset aromaattiset hiilivedyt ja syöpä
Kivihiilitervan tislauksessa tarvittava voimakas kuumennus johtaa PAH-yhdisteiden muodostumiseen. Monien vuosien ajan on tiedetty, että kivihiilitervan jalostamoiden työntekijät ovat alttiita eräänlaiselle ihosyövälle, jota kutsutaan tervasyöväksi. Tutkimukset ovat osoittaneet, että monet PAH-yhdisteet ovat syöpää aiheuttavia. Yksi aktiivisimmista syöpää aiheuttavista yhdisteistä, bentsopyreeni, esiintyy kivihiilitervassa, ja sitä on eristetty myös tupakansavusta, marihuanan savusta, autojen pakokaasuista ja hiilellä paistetuista pihveistä. On arvioitu, että bentsopyreeniä päästetään vuosittain yli 1 000 tonnia ilmaan Yhdysvalloissa. Vain muutama milligramma bentsopyreeniä ruumiinpainokiloa kohti riittää aiheuttamaan syöpää koe-eläimissä.
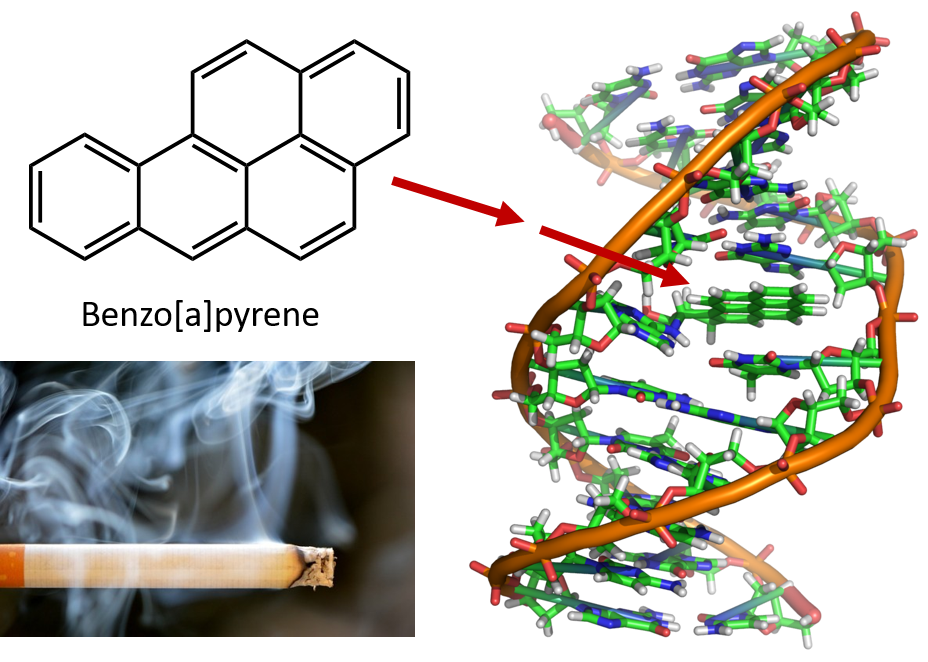
Kuva 8.6 Bentsopyreeni on polysyklinen aromaattinen hiilivety, jota syntyy sivutuotteena kivihiilitervassa, savukkeiden ja marihuanan savussa sekä hiilletyissä pihveissä. Bentsopyreeni metaboloituu biologisesti aktiivisiksi yhdisteiksi, jotka voivat muodostaa fysikaalisia addukteja DNA-molekyyleihin. Nämä adduktit voivat aiheuttaa geneettisiä mutaatioita, jotka aiheuttavat syöpää.
Kuva savukesavusta
Biologisesti tärkeät yhdisteet, joissa on bentseenirengas
Bentseenirengasta sisältävät aineet ovat yleisiä sekä eläimissä että kasveissa, vaikkakin jälkimmäisissä niitä on runsaammin. Kasvit voivat syntetisoida bentseenirengasta hiilidioksidista, vedestä ja epäorgaanisista aineista. Eläimet eivät pysty syntetisoimaan sitä, mutta ne ovat riippuvaisia tietyistä aromaattisista yhdisteistä selviytyäkseen, ja siksi niiden on saatava niitä ravinnosta. Fenyylialaniini, tyrosiini ja tryptofaani (välttämättömät aminohapot) sekä K-vitamiini, B2-vitamiini (riboflaviini) ja B9-vitamiini (foolihappo) sisältävät kaikki bentseenirengasta. Myös monissa tärkeissä lääkeaineissa, joista muutama on esitetty taulukossa 8.2, on bentseenirengas.
Huomautus
Tähän mennessä olemme tutkineet vain aromaattisia yhdisteitä, joissa on hiiltä sisältävä rengas. Monilla syklisillä yhdisteillä on kuitenkin renkaassa jokin muu alkuaine kuin hiiliatomi. Orgaanisia rengasrakenteita, joissa on jokin muu atomi kuin hiili, kutsutaan heterosyklisiksi yhdisteiksi .., Heterosyklisillä aromaattisilla yhdisteillä on myös ainutlaatuisia ja lääketieteellisesti merkittäviä ominaisuuksia.
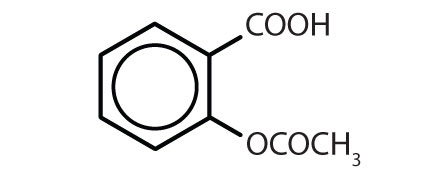
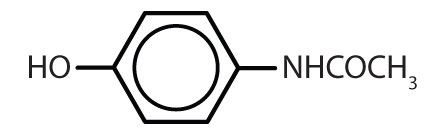
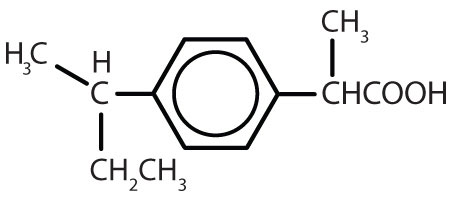
Taulukko 8.2 Joitakin lääkkeitä, jotka sisältävät bentseenirenkaan
| Nimi | Rakenne | |
|---|---|---|
| aspiriini |
 |
|
| asetaminofeeni |
 |
 |
| ibuprofeeni |
 |
|
| amfetamiini |
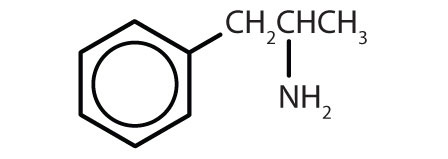 |
|
| sulfanilamidi |
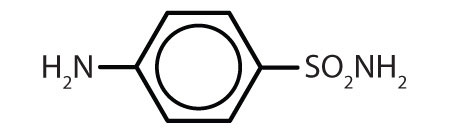 |
8.5 Geometriset isomeerit
Alkaanirakenteessa on vapaata rotaatiota hiilen ja hiilen välisten yksittäisten sidosten (C-C) ympäri. Sen sijaan alkeenien rakenne edellyttää, että hiiliatomit muodostavat kaksoissidoksen. Alkuaineiden väliset kaksoissidokset syntyvät p-orbitaalikuorien (joita kutsutaan myös pi-orbitaaleiksi) avulla. Nämä orbitaalikuoret ovat pikemminkin käsipainojen muotoisia kuin yksinkertaisissa sidoksissa käytettävät pyöreät orbitaalit. Tämä estää hiiliatomien vapaan pyörimisen kaksoissidoksen ympärillä, sillä se aiheuttaisi kaksoissidoksen katkeamisen pyörimisen aikana (kuva 8.7). Yksittäinen sidos on siis analoginen kahdelle laudalle, jotka on naulattu yhteen yhdellä naulalla. Laudat voivat vapaasti pyöriä yhden naulan ympärillä. Kaksoissidos taas vastaa kahta lautaa, jotka on naulattu yhteen kahdella naulalla. Ensimmäisessä tapauksessa laudat voivat kiertyä, kun taas jälkimmäisessä tapauksessa niitä ei voi kiertyä.

Kuva 8.7 Kaksoissidosten muodostaminen edellyttää pi-sidosten käyttöä. Jotta molekyylit voivat muodostaa kaksoissidoksia, elektronien on jaettava päällekkäisiä pi-orbitaaleja kahden atomin välillä. Tämä edellyttää, että nyytinmuotoiset pi-orbitaalit (kuva vasemmalla) pysyvät kiinteässä konformaatiossa kaksoissidoksen muodostumisen aikana. Tämä mahdollistaa sellaisten elektroniorbitaalien muodostumisen, jotka molemmat atomit voivat jakaa (kuvassa oikealla). Pyöriminen kaksoissidoksen ympärillä aiheuttaisi pi-orbitaalien vääränlaisen asettelun, jolloin kaksoissidos rikkoutuisi.
Diagrammi saatu lähteestä: JoJanderivative work – Vladsinger (talk)
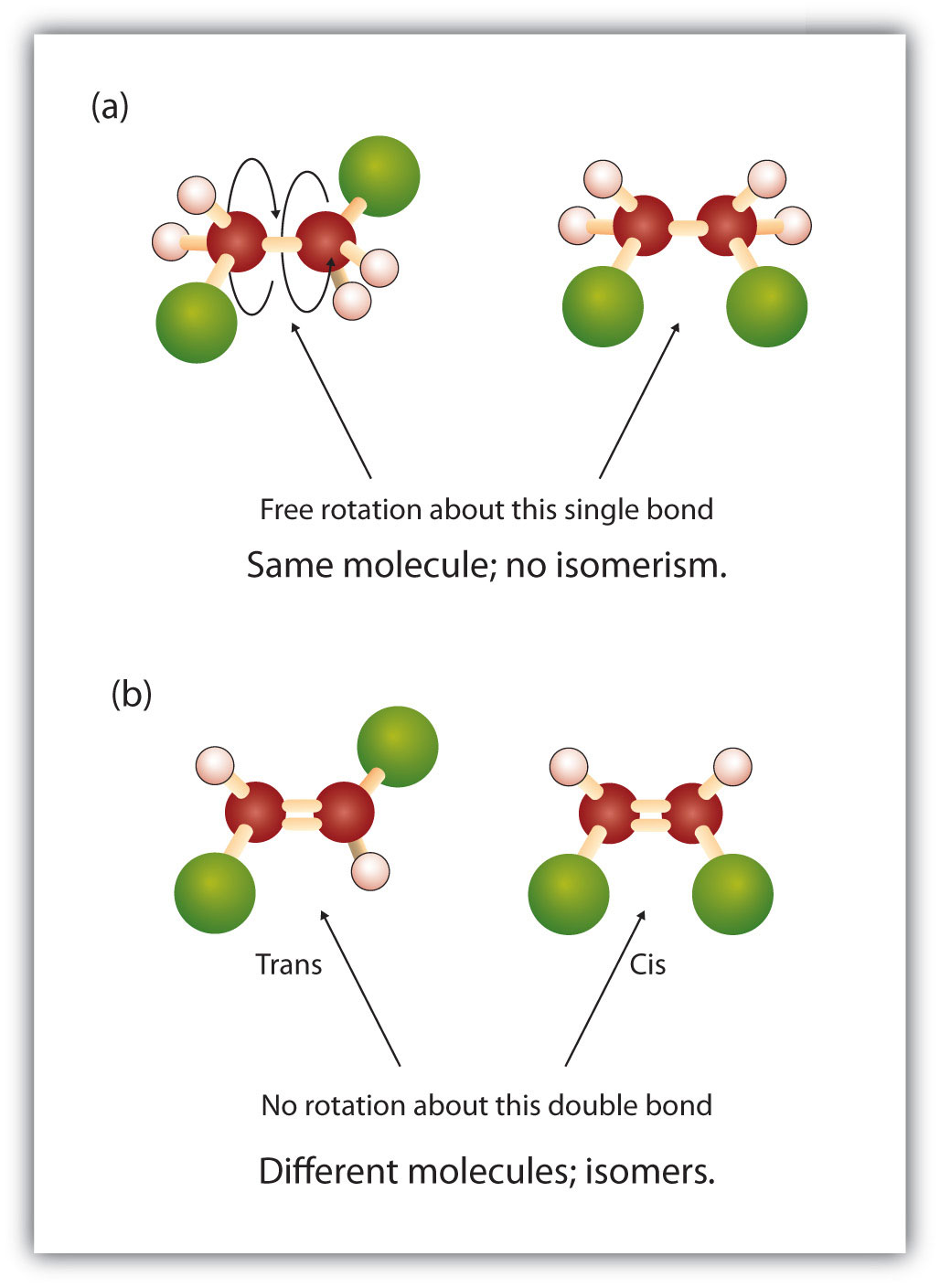
Kaksoissidoksen kiinteä ja jäykkä luonne luo mahdollisuuden ylimääräisen kiraalisen keskuksen syntymiseen ja siten stereoisomeerien mahdollisuuteen. Uusia stereoisomeerejä muodostuu, jos kumpaankin kaksoissidoksessa mukana olevaan hiileen liittyy kaksi eri atomia tai ryhmää. Tarkastellaan esimerkiksi kahta kloorattua hiilivetyä kuvassa 8.8. Ylemmässä kuvassa näkyy halogenoitu alkaani. Pyöriminen tämän hiili-hiilisidoksen ympärillä on mahdollista, eikä se johda erilaisiin isomeerikonformaatioihin. Alemmassa kuvassa halogenoidun alkeenin rotaatio kaksoissidoksen ympärillä on rajoitettu. Huomaa myös, että kukin kaksoissidokseen osallistuva hiili on myös kiinnittynyt kahteen eri atomiin (vety ja kloori). Näin ollen tämä molekyyli voi muodostaa kaksi stereoisomeeria: toisen, jossa kaksi klooriatomia on kaksoissidoksen samalla puolella, ja toisen, jossa kloorit ovat kaksoissidoksen vastakkaisilla puolilla.
Kuva 8.8 Alkeenin kaksoissidos voi muodostaa geometrisia isomeerejä. (a) Näyttää vapaan rotaation hiili-hiili-kaksoissidoksen ympärillä alkaanirakenteessa. (b) Näyttää hiili-hiili-kaksoissidoksen kiinteän asennon, joka johtaa geometrisiin (spatiaalisiin) isomeereihin.
Klikkaa tästä Kahn-akatemian video-opetusohjelma alkeenin rakenteesta.
Tässä jaksossa emme käsittele nimeämistä, joka sisältyy myös tähän video-opetusohjelmaan.(Huomautus: Kaikki Khan Academy -sisältö on saatavilla ilmaiseksi CC-BY-NC-SA -lisensointia käyttäen osoitteessa www.khanacademy.org )
Cis-trans-nimikkeistö
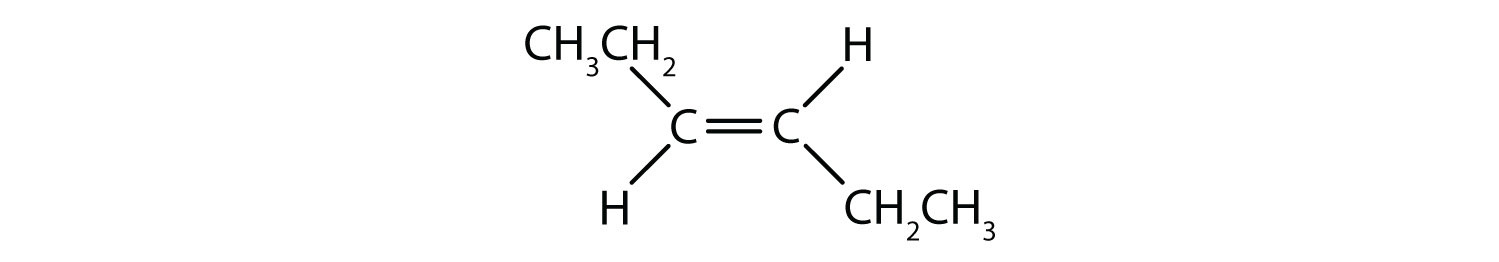
Cis-trans-nimikkeistöä voidaan käyttää yksinkertaisten isomeerien erottamiseen, kun kaksoissidoksen kumpaankin hiileen on kiinnittynyt joukko samanlaisia ryhmiä. Esimerkiksi kuvassa 8.8b kuhunkin kaksoissidokseen osallistuvaan hiileen on kiinnittynyt klooria ja myös vetyä. Cis- ja trans-järjestelmä määrittää, ovatko identtiset ryhmät kaksoissidoksen samalla puolella (cis) vai ovatko ne kaksoissidoksen vastakkaisella puolella (trans). Jos esimerkiksi vetyatomit ovat kaksoissidoksen vastakkaisella puolella, sidoksen sanotaan olevan trans-konformaatiossa. Kun vetyryhmät ovat kaksoissidoksen samalla puolella, sidoksen sanotaan olevan cis-konformaatiossa. Huomaa, että voit myös sanoa, että jos molemmat klooriryhmät ovat kaksoissidoksen vastakkaisella puolella, molekyyli on trans-konformaatiossa tai jos ne ovat samalla puolella kaksoissidosta, molekyyli on cis-konformaatiossa.
Määrittääksesi, onko molekyyli cis- vai trans-molekyyli, on hyödyllistä piirtää katkoviiva kaksoissidoksen keskelle ja ympyröidä sitten identtiset ryhmät, kuten kuvassa 8.9 on esitetty. Molemmat kuvassa 8.9 esitetyt molekyylit on nimetty 1,2-dikloorieteniksi. Näin ollen cis- ja trans-nimitys määrittelee ainoastaan stereokemian kaksoissidoksen ympärillä, mutta ei muuta molekyylin yleistä identiteettiä. Cis- ja trans-isomeereillä on kuitenkin usein erilaiset fysikaaliset ja kemialliset ominaisuudet, mikä johtuu sidosten kiinteästä luonteesta avaruudessa.
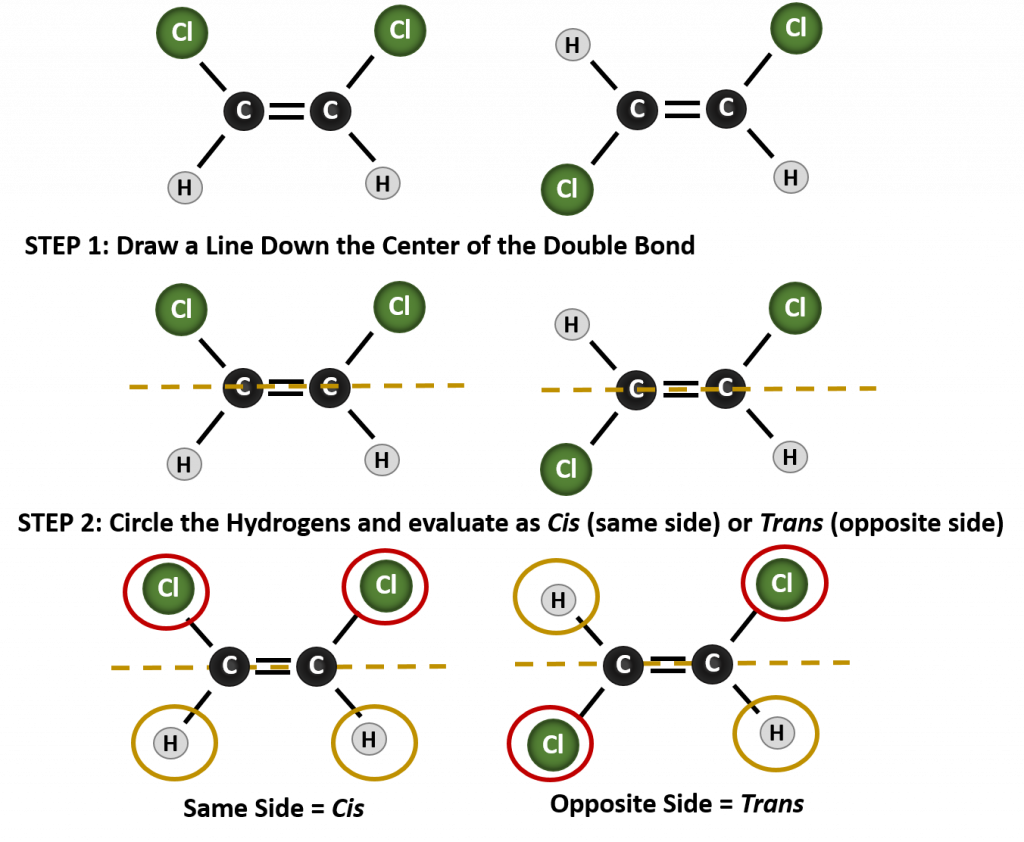
Kuva 8.9 Opas cis- tai trans-konformaatioiden määrittämiseen.
Click Here for a Kahn Academy Video Tutorial on Cis/Trans Isomerization
(Huom: Kaikki Khan Academyn sisältö on saatavilla ilmaiseksi CC-BY-NC-SA -lisensointia käyttäen osoitteessa www.khanacademy.org )
Cis-trans-isomeriaa esiintyy myös syklisissä yhdisteissä. Rengasrakenteissa ryhmät eivät pysty kiertymään minkään renkaan hiili-hiilisidoksen ympäri. Siksi ryhmät voivat olla joko renkaan samalla puolella (cis) tai vastakkaisilla puolilla (trans). Tässä esitämme kaikki sykloalkaanit tasorakenteina ja ilmoitamme ryhmien sijainnit joko renkaan tason ylä- tai alapuolella.

Terveydellesi
Luultavasti tavallisin paikka, jossa kuulet jokapäiväisessä elämässä viittauksia cis-trans-konformaatioihin, on supermarketissa tai lääkärin vastaanotolla. Se liittyy ravintorasvojen kulutukseemme. Ravinnon rasvojen epäasianmukainen tai liiallinen kulutus on yhdistetty moniin terveysongelmiin, kuten diabetekseen ja ateroskleroosiin sekä sepelvaltimotautiin. Mitä eroja siis on tyydyttyneiden ja tyydyttymättömien rasvojen välillä ja mitä ovat transrasvat ja miksi ne ovat niin suuri huolenaihe terveydelle?

Kuvio 8.10 Yleiset ravintorasvojen lähteet.
Kuva: TyMaHe
Yleisimpiä ravintorasvojen muotoja ja kehon rasvan tärkeimpiä ainesosia ihmisillä ja muilla eläimillä ovat triglyseridit (TAGit). TAG:t, kuten kuvassa 8.10 on esitetty, rakentuvat yhdestä glyserolimolekyylistä ja kolmesta rasvahappomolekyylistä, jotka on yhdistetty toisiinsa esterisidoksella. Tässä jaksossa keskitytään pitkien rasvahappojen hännän rakenteeseen, joka voi koostua alkaani- tai alkeenirakenteista. Luvussa 10 keskitytään enemmän esterisidosten muodostumiseen.

Kuva 8.11. Esimerkki triglyseridin (TAG) rakenteesta. Huomaa, että jokaisessa triglyseridissä on kolme pitkäketjuista rasvahappoa, jotka ulottuvat glyserolin selkärangasta. Kukin rasvahappo voi olla eriasteisesti tyydyttynyt ja tyydyttymätön.
Rakenne mukailtu: Wolfgang Schaefer
Täysin tyydyttyneissä rasvoissa on vain rasvahappoja, joilla on pitkäketjuiset alkaanihännät. Niiden sanotaan olevan ”tyydyttyneitä” vetyatomeilla. Tyydyttyneet rasvat ovat yleisiä amerikkalaisessa ruokavaliossa, ja niitä on punaisessa lihassa, maitotuotteissa, kuten maidossa, juustossa ja voissa, kookosöljyssä, ja niitä on monissa leivonnaisissa. Tyydyttyneet rasvat ovat huoneenlämmössä tyypillisesti kiinteitä aineita. Tämä johtuu siitä, että pitkäketjuiset alkaanit voivat pinoutua yhteen, koska niillä on enemmän molekyylien välisiä Lontoon dispersiovoimia. Tämä antaa tyydyttyneille rasvoille korkeammat sulamis- ja kiehumispisteet kuin monissa kasviöljyissä esiintyville tyydyttymättömille rasvoille.
Suuri osa luonnossa esiintyvistä tyydyttymättömistä rasvoista on cis-konformaatiossa, kuten kuvassa 8.11 on esitetty. Huomaa, että kuvassa 8.11 esitetyt rasvahapot on piirretty mukavuuden vuoksi, jotta niitä on helppo tarkastella eivätkä ne vie liikaa tilaa paperilla, mutta kirjoitetut sidoskulmat eivät kuvaa riittävästi molekyylien todellista avaruudellista orientaatiota. Kun kuvassa 8.11 esitetyt TAG:n rasvahapot piirretään oikeilla sidoskulmilla, on helppo nähdä, että cis-kaksoissidokset aiheuttavat mutkia alkeeniketjuun (kuva 8.12).
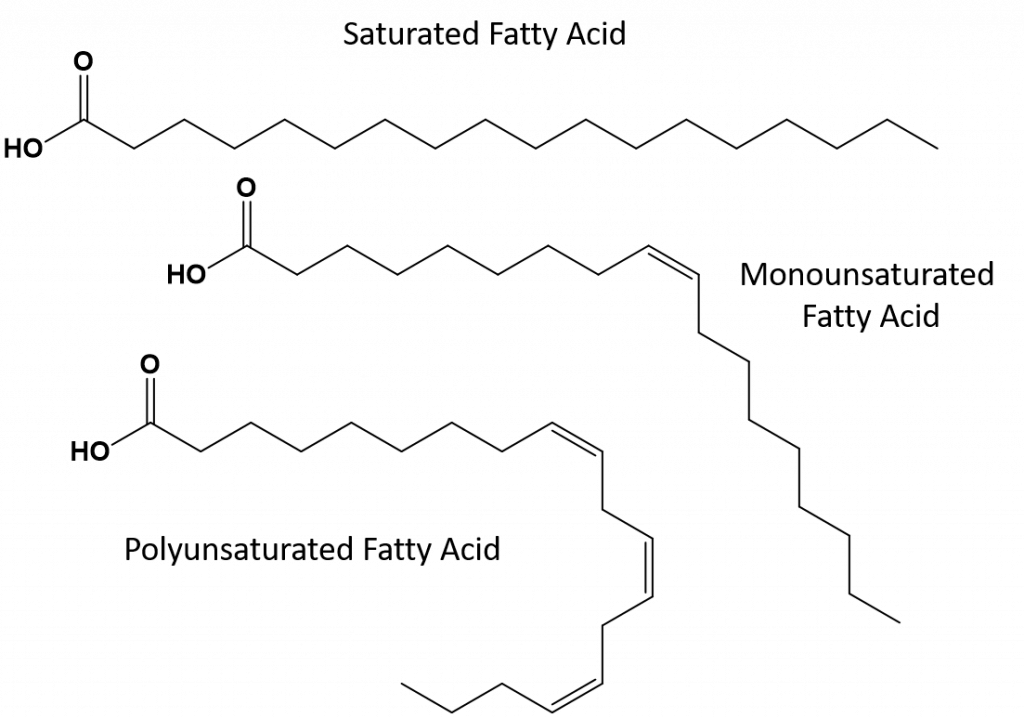
Kuva 8. TAG:n rasvahapot.12 Cis-kaksoissidokset aiheuttavat mutkia rasvahapporakenteeseen
Kertatyydyttymättömät ja monityydyttymättömät rasvat eivät siis pääse kasaantumaan yhtä helposti, eikä niillä ole yhtä paljon molekyylien välisiä vetovoimia verrattuna tyydyttyneisiin rasvoihin. Tämän seurauksena niiden sulamis- ja kiehumispisteet ovat alhaisemmat ja ne ovat yleensä nestemäisiä huoneenlämmössä. On osoitettu, että tyydyttyneiden rasvojen vähentäminen tai korvaaminen ruokavaliossa mono- ja monityydyttymättömillä rasvoilla auttaa alentamaan kolesterolin LDL-muodon (low-density-lipoprotein) pitoisuutta, joka on sepelvaltimotaudin riskitekijä.
Trans-rasvat taas sisältävät trans-konformaatiossa olevia kaksoissidoksia. Näin ollen rasvahappojen muoto on lineaarinen, kuten tyydyttyneillä rasvoilla. Transrasvoilla on myös samanlaiset sulamis- ja kiehumispisteet kuin tyydyttyneillä rasvoilla. Toisin kuin tyydyttyneitä rasvoja, transrasvoja ei kuitenkaan yleisesti esiinny luonnossa, ja niillä on kielteisiä terveysvaikutuksia. Transrasvoja syntyy pääasiassa elintarvikkeiden jalostuksen sivutuotteena (pääasiassa margariinien ja rasvanpoistajaöljyn valmistuksessa tapahtuvassa vetykäsittelyssä) tai ruoanlaitossa, erityisesti rasvakeittämisessä. Itse asiassa monet pikaruokapaikat käyttävät transrasvoja friteerausprosessissaan, koska transrasvoja voidaan käyttää useita kertoja ennen kuin ne on vaihdettava. Transrasvojen käyttö nostaa elimistön LDL-kolesterolipitoisuutta (huono kolesteroli, joka liittyy sepelvaltimotautiin) ja alentaa HDL-kolesterolia (hyvä kolesteroli elimistössä). Transrasvojen käyttö lisää sydänsairauksien ja aivohalvauksen sekä tyypin II diabeteksen kehittymisen riskiä. Riski on korreloinut niin voimakkaasti, että monet maat, kuten Norja, Ruotsi, Itävalta ja Sveitsi, ovat kieltäneet transrasvojen käytön. Yhdysvalloissa elintarvike- ja lääkevirasto FDA (Food and Drug Administration) on hiljattain hyväksynyt toimenpiteen, jonka mukaan transrasvojen käyttö elintarvikkeissa lopetetaan asteittain vuoteen 2018 mennessä. Tämän toimenpiteen arvioidaan ehkäisevän 20 000 sydänkohtausta ja 7 000 kuolemantapausta vuodessa.
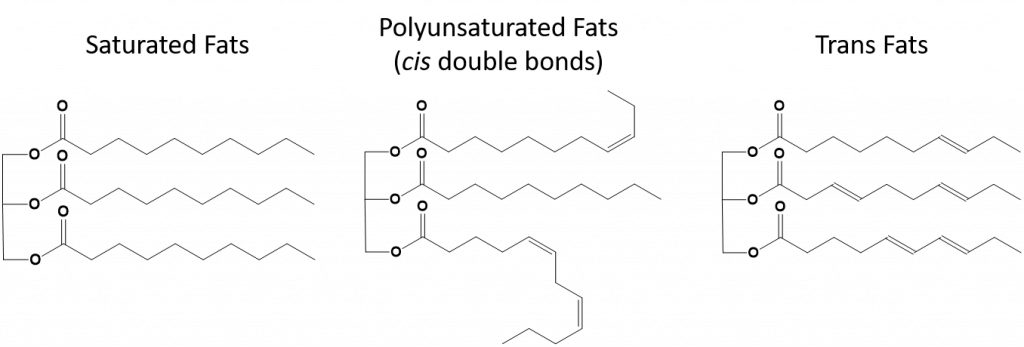
Kuva 8.13 Tyydyttyneiden, monityydyttymättömien ja transrasvojen rakenteelliset erot.
Click Here for a Kahn Academy Video Tutorial on Saturated-, Unsaturated-, and Trans-Fats
(Huomautus: Kaikki Khan Academy -sisältö on saatavilla ilmaiseksi CC-BY-NC-SA -lisensointia käyttäen osoitteessa www.khanacademy.org )
Key Factors for Determining Cis/Trans Isomerization
- Yhdisteen on sisällettävä kaksois- tai kolmoissidos tai sillä on oltava rengasrakenne, joka ei salli vapaata pyörimistä hiili-hiilisidoksen ympärillä.
- Yhdisteessä on oltava kaksi ei-identtistä ryhmää kiinnittyneenä kuhunkin hiili-hiili kaksois- tai kolmoissidokseen osallistuvaan hiileen.
Työskentelyesimerkki
Mitkä yhdisteet voivat esiintyä cis-trans (geometrisina) isomeereinä? Piirrä ne.
- CHCl=CHBr
- CH2=CBrCH3
- (CH3)2C=CHCH2CH3
- CH3CH=CHCHCH2CH3
Ratkaisu
Kaikkiin neljään rakenteeseen liittyy kaksoissidos ja ne täyttävät näin ollen 1. säännön mukaisen cis-trans-isomeriaan.
-
Tämä yhdiste täyttää säännön 2; sillä on kaksi ei-identtistä ryhmää kullakin hiiliatomilla (H ja Cl yhdellä ja H ja Br toisella). Se esiintyy sekä cis- että trans-isomeerinä:

- Tässä yhdisteessä on kaksi vetyatomia yhdessä sen kaksoissidoksissa olevasta hiiliatomista; se ei täytä sääntöä 2 eikä sitä esiinny cis- ja trans-isomeerinä.

- Tässä yhdisteessä on kaksi metyyli(CH3)-ryhmää yhdessä sen kaksoissidoksissa olevasta hiiliatomista. Se ei täytä sääntöä 2 eikä sitä ole olemassa cis- ja trans-isomeereinä.

-
Tämä yhdiste täyttää säännön 2; sillä on kaksi ei-identtistä ryhmää kummallakin hiiliatomilla, ja se esiintyy sekä cis- että trans-isomeerinä:

Taitotehtävä
-
Mitkä yhdisteet voivat esiintyä sekä cis- että trans-isomeereinä? Piirrä ne.
- CH2=CHCH2CH2CH3
- CH3CH=CHCH2CH3
- CH3CH2CH=CHCH2CH3
-
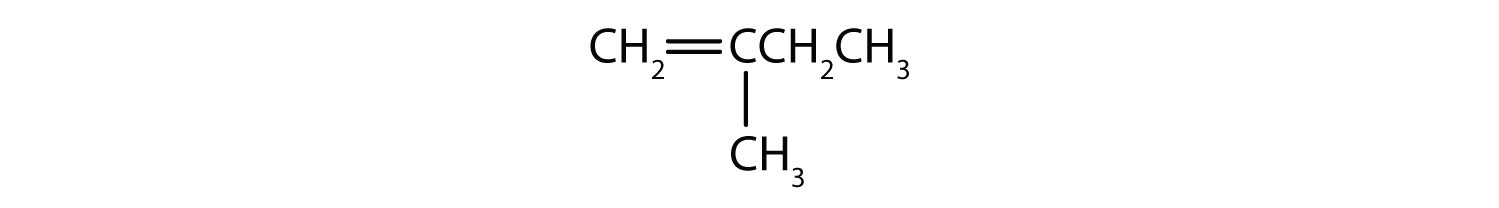
-
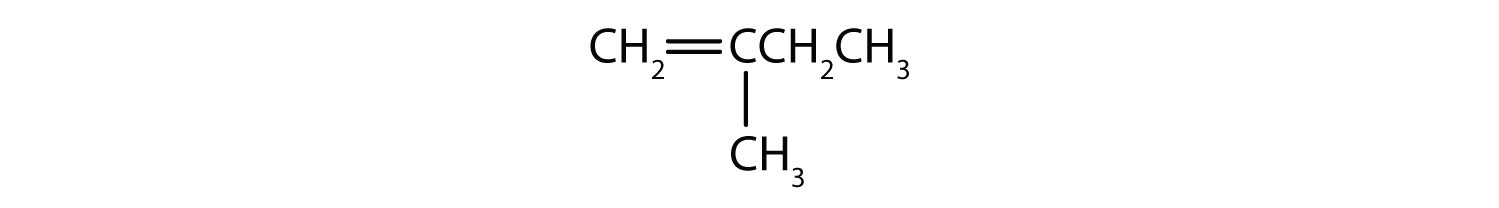
-
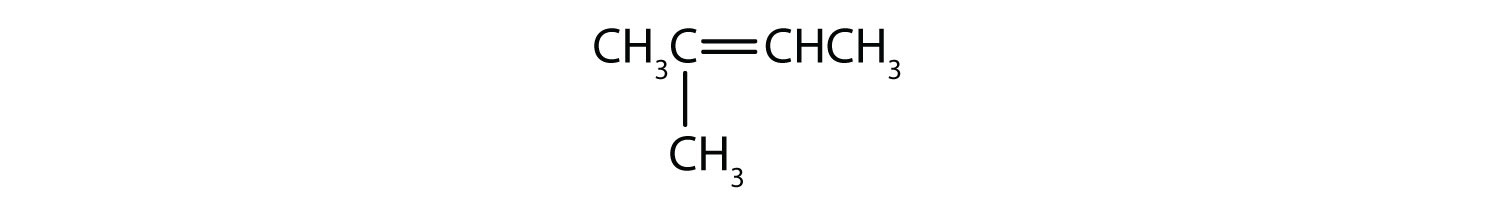
Käsitteiden kertausharjoitukset
-
Mitä ovat cis-trans (geometriset) isomeerit? Mitkä kaksi yhdistetyyppiä voivat osoittaa cis-trans-isomeriaa?
-
Luokittele kukin yhdiste cis-isomeeriksi, trans-isomeeriksi tai ei kummaksikaan.
-
Vastaukset
-
Cis-Trans-isomeerit ovat yhdisteitä, joilla on erilaiset konfiguraatiot (ryhmät pysyvästi eri paikoissa avaruudessa), koska niiden molekyylissä on jäykkä rakenne. Alkeneilla ja syklisillä yhdisteillä voi esiintyä cis-trans-isomeriaa.
-
- trans
- cis
- cis
- kumpikaan
Key Takeaway
- Cis-trans (geometrinen) isomeria on olemassa, kun molekyylissä on rajoitettu rotaatio ja jokaisessa kemialliseen sidokseen osallistuvassa hiiliatomissa on kaksi eri ryhmää.
(Takaisin alkuun)
E-Z-nimikkeistö
Tilanne muuttuu monimutkaisemmaksi, kun kaksoissidoksen muodostumiseen osallistuviin hiiliatomeihin on kiinnittynyt 4 eri ryhmää. Tällöin ei voida käyttää cis-trans-nimitysjärjestelmää, koska ei ole mitään viittausta siihen, mitä ryhmiä nimikkeistö kuvaa. Esimerkiksi alla olevassa molekyylissä voidaan sanoa, että kloori on trans bromiryhmään nähden, tai voidaan sanoa, että kloori on cis metyyliryhmään (CH3) nähden. Näin ollen pelkkä cis- tai trans-kirjoitus ei tässä tapauksessa selvästi rajoita ryhmien avaruudellista suuntautumista kaksoissidokseen nähden.
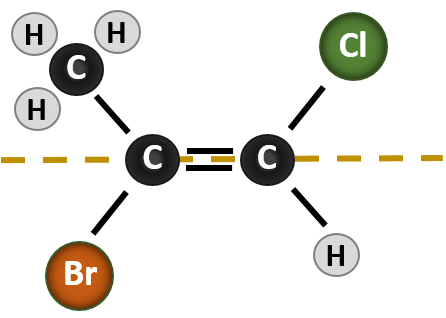
Tässä tilanteessa muodostuvien eri stereoisomeerien nimeäminen edellyttää prioriteettisääntöjen tuntemista. Muistetaan luvusta 5, että Cahn-Ingold-Prelog (CIP) -prioriteettijärjestelmässä kiraaliseen hiileen kiinnittyneille ryhmille annetaan prioriteetti niiden järjestysluvun (Z) perusteella. Atomeille, joilla on korkeampi järjestysluku (enemmän protoneja), annetaan korkeampi prioriteetti (eli S > P > O > N > C > H). Tässä nimikkeistöjärjestelmässä käytetään nimityksiä (Z) ja (E) cis/trans-järjestelmän sijasta. (E) tulee saksankielisestä sanasta entgegen eli vastakkainen. Näin ollen, kun korkeamman prioriteetin ryhmät ovat kaksoissidoksen vastakkaisella puolella, sidoksen sanotaan olevan (E)-konformaatiossa. (Z) taas tulee saksan sanasta zusammen eli yhdessä. Kun korkeamman prioriteetin ryhmät ovat kaksoissidoksen samalla puolella, sidoksen sanotaan olevan (Z)-konformaatiossa. Kuvassa 8.14 on esitetty vaiheet, joita käytetään molekyylin (E)- tai (Z)-konformaatioiden määrittämisessä.
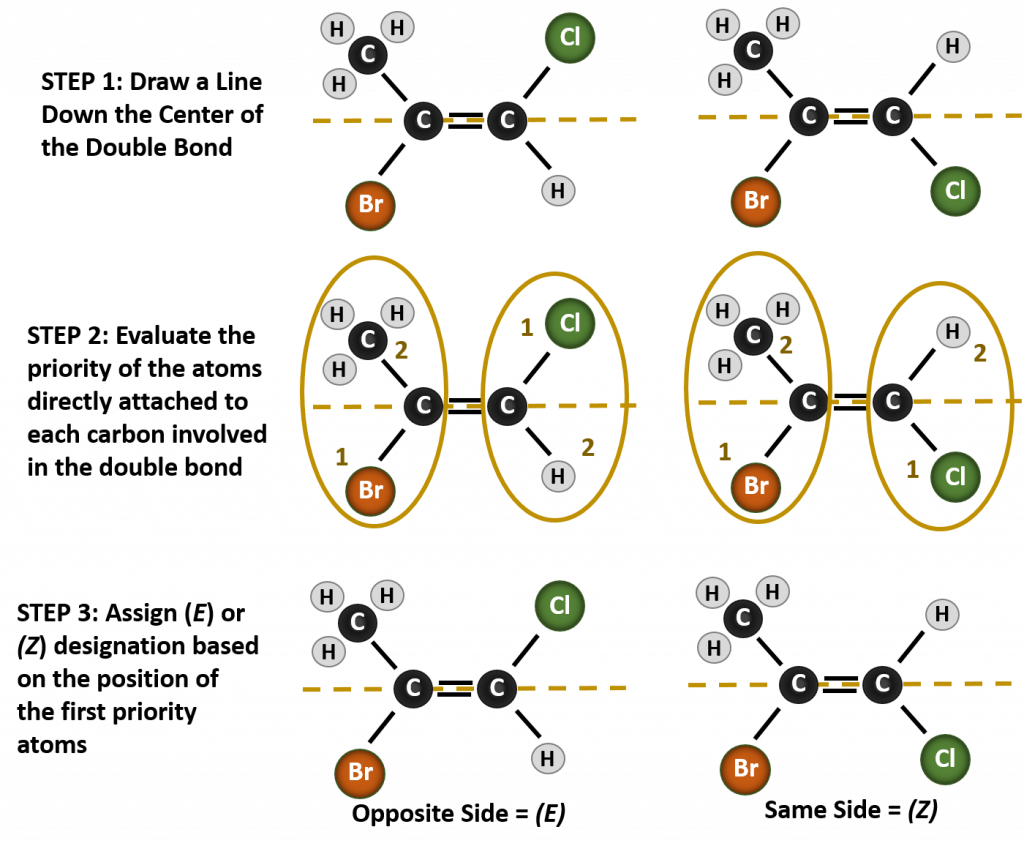
Kuva 8.14 Vaiheet, joita käytetään (E)- ja (Z)-konformaatioiden määrittämisessä.
Klikkaa tästä Kahn Academyn video-opetusta E/Z-isomerisaatiosta.
(Huomautus: Kaikki Khan Academyn sisältö on saatavilla ilmaiseksi CC-BY-NC-SA -lisensointia käyttäen osoitteessa www.khanacademy.org )