Az újszülöttek jelentős részénél az élet első hetében kezelésre szoruló hyperbilirubinémia alakul ki (“szignifikáns” hyperbilirubinémia, SHB) . A születéskori kórházi tartózkodás időtartamának csökkenése időben összefüggésbe hozható a bilirubin okozta neurológiai károsodás megnövekedett előfordulási gyakoriságával . Az egészségügyi dolgozó által a hazabocsátás után tett otthoni látogatások vagy a család által a kórházban tett látogatások felderíthetik az SHB-t, de nem mindenhol megvalósíthatóak vagy költséghatékonyak. Ezért az újszülöttek kórházból való elbocsátása előtt azonosítani kell a magas bilirubinszint kialakulásának kockázatának kitett újszülötteket
Az SHB kialakulásának kockázatának elbocsátás előtti objektív felmérése azért is fontos, mert a sárgaság mértékének vizuális felmérése korlátozott pontosságú . Az SHB kockázati rétegzése a bilirubin terhelés (a szérum teljes bilirubin vagy a transzkután bilirubin abszolút szintje vagy emelkedési sebessége), a bilirubintermelés (kilélegzett szén-monoxid) és a mögöttes klinikai kockázati tényezők azonosításával történt .
A bilirubin koncentrációja a perifériás vérben a bilirubin termelés, metabolizmus, kiválasztás és reabszorpció életkor-specifikus sebességének függvénye. Ezért az újszülött bilirubinszintjének értelmezése a születés utáni életkoron alapul. A Bhutani és munkatársai által kifejlesztett óraspecifikus bilirubin nomogram kimutatta, hogy a szérum teljes bilirubin (STB) mérése a szülészeti kórházból való elbocsátás előtt segíthet azon újszülöttek azonosításában, akiknél fennáll a kockázata annak, hogy a követés során magasabb százalékos STB-értékek alakulnak ki. A különböző kockázat-előrejelzési módszerek közül az STB hazabocsátás előtti mérése mutatta a legjobb megkülönböztető képességet az észak-amerikai újszülöttek körében. A bilirubin metabolizmus genetikailag meghatározott különbségei és a táplálási gyakorlatok különbözőségei miatt azonban a hyperbilirubinémia klinikai lefolyása eltérő lehet a különböző etnikumokhoz vagy földrajzi helyekhez tartozó újszülötteknél. Ezenkívül a korábbi nomogramot egy retrospektív kohorszból dolgozták ki, amelyben a jelentős hyperbilirubinémia kimenetelére vonatkozó információk csak a vizsgált populáció egyötödénél voltak ismertek. Ezért a különböző újszülöttpopulációkban az óraspecifikus bilirubin-nomogram elkészítése előfeltétele annak, hogy az elbocsátás előtti bilirubinmérést kockázatértékelési stratégiaként lehessen alkalmazni.
Ezt a prospektív kohorszvizsgálatot terveztük az indiai újszülöttek óraspecifikus szérum összbilirubinin nomogramjának elkészítésére és a hazabocsátás előtti bilirubinmérés hatékonyságának értékelésére a kezelésre szoruló hyperbilirubinémia előrejelzésében a terminális és késői koraszülött újszülöttek körében.
Módszerek
Ezt a prospektív kohorszvizsgálatot a diagnosztikai tesztek teljesítményének értékelésével 2010 februárjától júniusáig végeztük egy észak-indiai oktatókórházban. A vizsgálati protokollt a kórház etikai bizottsága jóváhagyta, és a szülőktől írásbeli beleegyező nyilatkozatot kaptunk. A vizsgálatba ≥35 hetes terhességgel vagy ≥2000 g születési súllyal rendelkező egészséges újszülöttek vehettek részt. Logisztikai okokból a vasárnap 24 órát betöltött újszülöttek nem vehettek részt a vizsgálatban. Kizárták azokat az újszülötteket, akiknél súlyos veleszületett rendellenesség, újszülött intenzív osztályra való felvétel, pozitív direkt Coombs-teszt (akkor végezték, ha az anya vércsoportja Rhesus-negatív volt), az első bilirubinmérés előtti fototerápia, vagy nem tudtak megjelenni a nyomon követésen.
Vizsgálati mérések és nyomon követés: A szérum teljes bilirubin első méréséhez szükséges vérmintát a metabolikus szűrés alkalmával vették le a szülés utáni 18-30 órás korban. A kapilláris vagy perifériás vénás vért előheparinizált mikrokapillárisokba vettük. A vért azonnal 5 percig 12000 rpm-en centrifugáltuk, és az összes bilirubint spektrofotométerrel (NEO-BIL plus, das srl, Olaszország) mértük.
A újszülötteket a kórházi tartózkodás alatt és a hazabocsátás után a 7. posztnatális nap befejezéséig követtük nyomon. A követéses látogatás időpontját az elbocsátáskori életkor alapján határozták meg. A 48 órás életkor előtt elbocsátott csecsemőket 72 és 96 órás életkor között, a 48 órás életkor után elbocsátott csecsemőket pedig 96 és 120 órás életkor között hívták vissza. A metabolikus szűréskor végzett első STB-mérésen kívül minden újszülöttnél további két STB-mérést végeztek. Az első mérést követően a második és harmadik STB-mérés elvégzésére vonatkozó döntés a klinikai értékelésen alapult. A sárgaság mértékének klinikai értékelését transzkután bilirubin (TcB) mérés kísérte több hullámhosszú transzkután biliméterrel (BiliChek, variációs koefficiens <5%). STB-becslésre akkor került sor, ha a tenyér/talp icterus foltos volt, vagy a TcB >12 mg/dl volt, vagy az életkor-specifikus fototerápiás küszöbérték 80%-án belül volt. Ha klinikailag nem jelezték, második és harmadik STB-mérést végeztek a születés utáni 72-96 órás, illetve 96-144 órás életkorban. A fototerápia megkezdése utáni STB-értékeket nem vettük figyelembe a nomogram elkészítésénél.
Az SHB kialakulásának kockázatát befolyásoló klinikai és epidemiológiai kockázati tényezőket rögzítettük. A következő adatokat rögzítették: születési súly, terhesség, nem, anyai végzettség és vallás, paritás, szülés előtti komplikációk, anyai ABO és Rh vércsoport, szülés módja, szülés során alkalmazott érzéstelenítés típusa és oxitocin infúzió alkalmazása a szülés során. Ezen kívül a táplálás megkezdésének életkorát, a szülés utáni első 24 órában és azt követően a szoptatástól vagy anyatejtől eltérő kiegészítő táplálást, valamint az első székletürítéskor elért életkort is feljegyezték.
Eredmény: A legfontosabb eredmény a szignifikáns hyperbilirubinémia (SHB) volt, amelyet úgy határoztak meg, hogy a hyperbilirubinémia kezelésére fényterápiára vagy cseretranszfúzióra volt szükség. A fototerápia megkezdéséről szóló döntést a csecsemő órákban kifejezett életkora és az STB-szintek alapján hozták meg, az Amerikai Gyermekgyógyászati Akadémia (AAP) irányelveinek helyi adaptációja szerint. A 38. vagy annál nagyobb terhességi héten született újszülötteknél a közepes kockázatú küszöbértéket, a 37. vagy annál kisebb terhességi héten született újszülötteknél pedig a magasabb kockázatú küszöbértéket alkalmazták a fototerápia megkezdésére. Az AAP-irányelvekben szereplő közepes kockázatú küszöbértékek majdnem azonosak a Bhutani nomogram 95
. percentilis értékeivel .
Statisztikai elemzés: Egy prospektív vizsgálatban az ≥35 hetes terhességgel született újszülöttek 10%-ánál észleltek jelentős hyperbilirubinémiát . Egy legalább 95%-os érzékenységű (konfidenciaintervallum 5%) és 0,05-ös alfa értékű diagnosztikai teszt vizsgálatához körülbelül 1000 alany bevonására volt szükség .
Az adatokat a Stata 9 (StataCorp, College Station, TX, USA) segítségével elemeztük. A nomogram elkészítéséhez az STB-értékeket hatórás epochákban (életkor±3 óra) a születés utáni életkorban 48 óráig és tizenkétórás epochákban (életkor±6 óra) a 48 órán túli életkorban kluboztuk. Az egyes epochák adatait szimmetria szempontjából vizsgáltuk. Az 5
., 10., 25., 40., 75., 90. és 95. percentilis értékeket minden epochára kiszámítottuk. A Microsoft Excel (Microsoft Corporation, Richmond, USA) programot használták az óránkénti bilirubin nomogram ábrázolásához. A 40., 75. és 95. percentilt ábrázoló simított nomogramot az R statisztikai szoftverhez készült GAMLSS csomaggal végzett köbös gerincmodellezéssel ábrázoltuk. A simítás után az esetek 36,5%-a a 40. percentilis vonal alatt, 77,8%-a a 75. percentilis vonal alatt, 95,1%-a pedig a 95. percentilis vonal alatt volt. A nomogram prediktív képességét az érzékenység, a specificitás, a pozitív prediktív érték, a negatív prediktív érték és a likelihood ratio kiszámításával, a receiver-operating characteristics (ROC) görbe felrajzolásával és a c-statisztika kiszámításával értékelték.
Eredmények
A vizsgálati időszak alatt összesen 1255 újszülött született, akik közül 1090 volt alkalmas a felvételre. Ezek közül 93-at különböző okokból kizártak (1. ábra). Összesen 997 újszülöttet vettek fel a vizsgálatba. A születési súly átlagos ± SD értéke 2627±536 g, a terhességi kor 37,8±1,5 hét volt (medián és IQR: 38 és 37-39) (I. táblázat). A vizsgált csecsemők többsége komplikációmentes terhesgondozás után született, és a méhen kívüli életbe való átmenetük eseménytelen volt. Az újszülöttek több mint 80%-át kizárólag szoptatták a kórházi tartózkodás alatt.
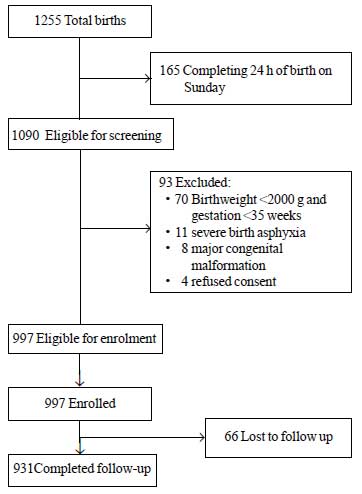
1. ábra Vizsgálat menete.
A bilirubin nomogram felépítése: A bilirubin első mérése 23,3±6,3 órás korban történt, és az átlagos STB 7,0±2,0 mg/dl volt. Huszonkilenc (2,9%) újszülöttnek volt szüksége fototerápiára az első bilirubinmérés alapján. Ezeknél az újszülötteknél a fototerápiát 27±5,6 órás korban kezdték meg, 12,3±2,0 mg/dl STB-szint mellett. Hatvanhat (6,6%) újszülöttet nem követtek nyomon a vizsgált kórházból való elbocsátás után. Az első bilirubinérték ezeknél az újszülötteknél hasonló volt azokhoz az újszülöttekhez, akiknél soha nem alakult ki SHB (6,5±1,9 vs. 6,7±1,7 mg/dl, P=0,54), és szignifikánsan alacsonyabb volt azoknál, akiknél SHB alakult ki (6,5±1,9 vs. 8,5±2,2 mg/dl, P< 0,001).
A nomogram elkészítéséhez és az STB-értékek eloszlásának értékeléséhez a születés utáni életkort hatórás epochákra osztottuk a születés utáni életkor 48 óráig és tizenkétórás epochákra a 48 órán túli életkor esetében. 42 óra kivételével az STB minden epochában szimmetrikus eloszlásúnak mutatkozott (2. ábra). A 42 órás STB-értékek eloszlása pozitívan ferde volt, és ezeket az értékeket nem használtuk fel a nomogram elkészítéséhez.
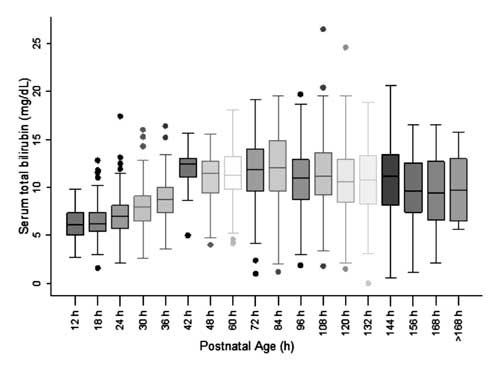
2. ábra A szérum teljes bilirubin eloszlását bemutató box-whisker plot.
Az 5
., 10., 25., 40., 75., 90. és 95. percentilis értékeket minden epochára kiszámítottuk. Életkor-specifikus szérum bilirubin nomogramot rajzoltunk a 40., 75. és 95. percentilis értékekkel a születés utáni életkor előrehaladtával (3. ábra).
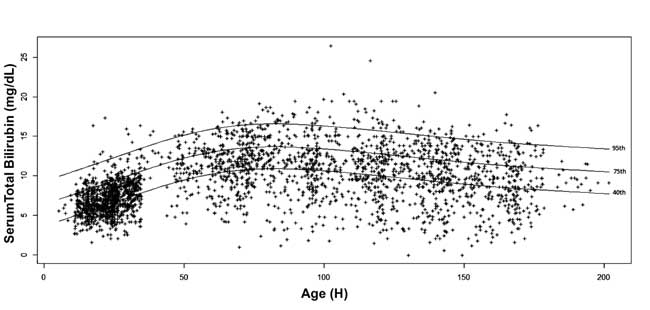
Ábra. 3 Bilirubin nomogram – óránkénti szérum teljes bilirubin 40., 75. és 95. percentilisekkel ábrázolva.
A hazabocsátás előtti STB prediktív képessége: Összességében 199 (20%) újszülöttnél alakult ki SHB (fototerápiában részesültek). Az első bilirubinértéket a hiperbilirubinémia későbbi kezelési szükségességének előrejelzésére használták. Ha a születést követő első 48 órában kettőnél több értéket kaptak, a magasabb percentilis értéket használták az előrejelzéshez.
TABLE I Predictive Characteristics of Percentile Values as Risk Demarcators for Subsequent Need of Treatment for Hyperbilirubinemia
| Elvezetés előtti szérum összbilirubin | eredmény | Teszt teljesítmény | |||||||
| Percentilis | Szám(n=928) | SHB+ | SHB- | PPV | NPV | Szenzitivitás | Specifikusság | ||
| A 95. percentilis felett | 49 | 34 | 15 | 69.4 | 81.2 | 17.1 | 97.9 | ||
| A 95. percentilis alatt | 879 | 165 | 714 | ||||||
| A 75. percentilis felett | 239 | 107 | 132 | 44.8 | 86.2 | 53.8 | 81.9 | ||
| 75. percentilis alatt | 689 | 92 | 597 | ||||||
| A 40. percentilis felett | 586 | 167 | 419 | 28.5 | 90.6 | 83.9 | 42.5 | ||
| A 40. percentilis alatt | 342 | 32 | 310 | ||||||
SHB: significant hyperbilirubinemia, PPV: positive predictive value, NPV: negative predictive value. |
|||||||||
Azok között az újszülöttek között, akiknek pre-STB mérést végeztek és befejezték a nyomon követést (n=928), 49 esetben (5.3%) újszülöttnél a hazabocsátás előtti STB meghaladta az életkor-specifikus eloszlás 95. percentilisét (I. táblázat). Ezek közül 34 újszülöttnek volt szüksége később fototerápiára (pozitív prediktív érték: 69,4%, érzékenység: 17,1%). 342 (36,8%) újszülött esetében a hazabocsátás előtti STB kisebb volt, mint az életkor-specifikus eloszlás 40. percentilise. Ezek közül 310 újszülöttnek nem volt szüksége hyperbilirubinaemia miatt későbbi kezelésre (negatív prediktív érték: 90,6%, specificitás: 42,5%). A 75. percentilis határérték pozitív prediktív értéke 44,8%, negatív prediktív értéke 86,2% volt. A 4. ábrán látható ROC-görbe az egyes percentilis határértékek diagnosztikus teljesítményét szemlélteti, a görbe alatti terület (c-statisztika) 0,73 volt.
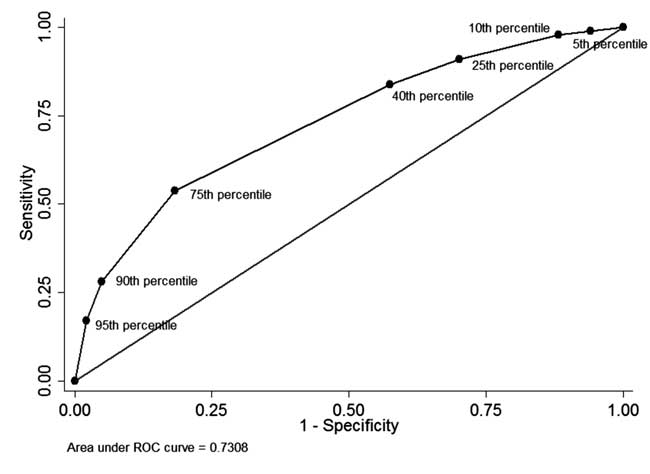
4. ábra A ROC-görbe a szérum teljes bilirubinjának a hazaengedés előtti szérumszérum különböző százalékos határértékeinek diagnosztikus képességére vonatkozóan.
A valószínűségi arány (LR) jobb eszköz a diagnosztikus teszt teljesítményének mérésére, mivel az arányt nem befolyásolja a kimenetel háttérprevalenciájának változása. A pozitív teszt LR-jét (LR+, a betegekben pozitív teszt valószínűsége/nem betegekben pozitív teszt valószínűsége) minden egyes kockázati demarkációs zónára kiszámítottuk. Az ≥95-ös percentilis STB-értéket a magas kockázatú zónába, a 75. és 94. centilis közötti értéket a felső-középső kockázatú zónába, a 40. és 74. centilis közötti értéket az alsó-középső kockázatú zónába, a 40. percentilis alatti értéket pedig az alacsony kockázatú zónába sorolták. A magas kockázati zónába tartozó 49 újszülött közül 34-nél alakult ki SHB; ezért a magas kockázati zónában az STB pozitív LR értéke 8,26 volt (II. táblázat). A felső-közepes kockázati zónába tartozó 190 újszülött közül 73-nál alakult ki SHB; ezért az STB pozitív LR értéke ebben a kockázati zónában 2,30 volt. Hasonlóképpen, az STB pozitív LR értéke az alsó-közepes kockázati zónában 0,76, az alacsony kockázati zónában pedig 0,37 volt.
TABLE IIPredictive Ability of Pre-discharge Serum Total Bilirubin for Subsequent Significant Hyperbilirubinemia (Need of Phototherapy)
| Elvezetés előtti szérum összes bilirubin | Elvezetés | Tesztelési teljesítmény | ||||||
| Elvezetés előtti teljes bilirubin | Percentilis | Teljes | SHB+ | SHB- | P:A arány | Betegség valószínűsége | LR+ | |
| Nagy kockázat | ≥95. | 49 | 34 | 15 | 7:3 | 7/10 | 8.26 | |
| Felső-középfokú | 75. a 94.-ig | 190 | 73 | 117 | 2:3 | 2/5 | 2.30 | |
| alsó-középső | 40-es 74-es | 347 | 60 | 287 | 1:5 | 1/6 | 0.76 | |
| alacsony kockázat | <40. | 342 | 32 | 310 | 1:10 | 1/11 | 0.37 | |
| 928 | 199 | 729 | 1:4 | 1/5 | ||||
| SHB: jelentős hyperbilirubinaemia; P:A arány: Kimenetel megléte : Kimenetel hiánya. | ||||||||
Diszkusszió
A bilirubin okozta neurológiai károsodás vagy kernicterus előfordulásának csökkentésére potenciális stratégiaként ajánlott a hazabocsátás előtti kockázatfelmérés a későbbi SHB kialakulására. Ebben a prospektív kohorszvizsgálatban az észak-indiai újszülöttek egy részhalmazában óraspecifikus szérum bilirubin nomogramot készítettünk, és értékeltük a kockázat elhatárolásának hatékonyságát az elbocsátás előtti STB-méréssel a későbbi fototerápia (SHB) szükségességének előrejelzésében. Vizsgálati kohorszunkban az SHB kiindulási előfordulása magas volt, 10 újszülöttből 2 újszülöttnél alakult ki SHB. A hazabocsátás előtti STB két magasabb kockázati zónában való elhelyezkedése szignifikánsan növelte a későbbi SHB kockázatát: a magas kockázati zónában 10 újszülöttből 7 újszülöttnél alakult ki SHB (pozitív LR=8,26) és a magasabb-közepes kockázati zónában 10 újszülöttből 4 újszülöttnél alakult ki SHB (pozitív LR=2,3). Az alacsony rizikójú zónában az elbocsátás előtti STB elhelyezkedése szignifikánsan csökkentette a későbbi SHB kockázatát, 10 újszülöttből 1 újszülöttnél alakult ki SHB (pozitív LR=0,37). Mivel azonban az alacsony kockázatú határérték negatív prediktív értéke csak 90% volt, az alacsony kockázatú zónában való elhelyezkedés nem volt képes kizárni a későbbi SHB lehetőségét.
Bhutani, és munkatársai egy nagy kohorszban kimutatták, hogy a magas és magas-közepes rizikójú zónában a hazabocsátás előtti STB-vel rendelkező újszülötteknél nagyobb valószínűséggel alakul ki SHB a követés során. A szerzők a szérum bilirubinszint százalékdiagramokat állítottak össze a különböző posztnatális életkorokban a közeli és a terminális újszülötteknél. Azt találták, hogy az újszülöttek 6,1%-ának szérum bilirubinszintje a hazabocsátás előtt >95. percentilis volt; e csecsemők 32,1%-ánál később hyperbilirubinémia alakult ki. Bhutani és munkatársai óraspecifikus nomogramjához képest ebben a vizsgálatban az STB percentilis értékei a születés utáni 84-108 órás korig akár 2 mg/dl-rel magasabbak. Az észak-indiai származású újszülötteknél megfigyelték, hogy magasabb bilirubinértékeket érnek el, és nagyobb a hyperbilirubinémia előfordulása. Az ebben a vizsgálatban megfigyelt 7,0±2,0 mg/dl átlagos STB a Bhutani nomogram 75. és 95. percentilise között van. Hasonlóképpen Agarwal és munkatársai 5,9±1,8 mg/dl átlagos STB-értékről számoltak be a születés utáni 24 órás korban, ami közel van a Bhutani nomogram 75. percentilis értékéhez. Vizsgálatunkban a koraszülött vagy alacsony születési súlyú újszülöttek nagyobb aránya és a kizárólagos szoptatás magasabb aránya hozzájárulhat a megnövekedett STB-értékekhez és az SHB gyakoribb előfordulási gyakoriságához. Ezenkívül az a döntésünk, hogy az AAP fototerápiás küszöbértékek középső vonalát használtuk a felső helyett, még az alacsony kockázatú újszülöttek esetében is, szintén növelte az SHB előfordulását. A születés utáni 108 órás életkoron túl az STB percentilis értékei ebben a vizsgálatban alacsonyabbak, mint a Bhutani nomogram megfelelő értékei. A klinikus megítélése alapján szelektíven követett újszülöttek STB-értékeinek bevonása a nomogram elkészítésébe magasabb STB-szinteket eredményezhetett a Bhutani-nomogram felrajzolásához, ami csökkentette annak általánosíthatóságát. Mivel a jelen vizsgálatban a nyomon követés a hyperbilirubinémia súlyosságától függetlenül befejeződött, a nomogram a születés utáni 4. és 5. napon érte el a csúcspontját, és az első hét végén természetes csökkenés következett be.
A prospektív kohorszvizsgálatban Agarwal és munkatársai 220 ≥35 hetes terhességgel született újszülöttnél mérték az STB-t 24±6 órás korban a hyperbilirubinaemia előrejelzésére . Az STB >6 mg/dl hiánya 24±6 órás korban gyakorlatilag kizárta a későbbi SHB lehetőségét (a negatív teszt valószínűségi aránya 0,07) a születést követő 5 napon belül. Az eredmény szelektív mérése azonban csak azoknál az újszülötteknél, akiknél a követés során a “klinikai” bilirubinszint >10 mg/dl volt, verifikációs torzítást eredményezett a vizsgálatban. Egy másik indiai vizsgálatban a 18-24 órás 3,99 mg/dl-es határértéket a későbbi >15 mg/dl bilirubinszint előrejelzésére 67%-os szenzitivitást és specificitást találtak. Teljes követés azonban csak azoknál a csecsemőknél volt, akik vagy újszülöttkori betegség, vagy valamilyen anyai ok, például császármetszés miatt maradtak kórházban. Az egészséges és ezért korán elbocsátott csecsemők több mint 50%-át nem követték nyomon. Egy törökországi tanulmány óraspecifikus bilirubin nomogramot mutatott be 35 és 37 hét közötti terhességi korú újszülötteknél. A 95
-edik percentilisnél nagyobb STB-érték magas pozitív prediktív értékkel bírt a későbbi SHB kialakulására . A 30. percentilisnél kisebb STB-értéknek azonban körülbelül 90%-os negatív prediktív értéke volt. Két nagy retrospektív vizsgálatban az STB korai/elutazás előtti mérésének kiváló előrejelző képességéről számoltak be, a görbe alatti terület (AUC) 0,83 volt . A mi vizsgálatunkban a 40. és 75. percentilis értékek diszkriminációs képessége alacsonyabb volt, mint a korábban közölteké . Ez a mi vizsgálatunkban a ROC-görbét az átlós vonal felé tolta el, ami csökkent megkülönböztető képességet eredményezett (AUC= 0,73). A törökországi (25,3%) és a mi vizsgálatunkban mért SHB magas kiindulási incidenciája (20%) magyarázhatja, hogy az alacsony percentilis értékek nem képesek kizárni a későbbi SHB kialakulását, ezáltal korlátozva a hazabocsátás előtti STB-mérés hasznosságát.
A későbbi SHB előrejelzésének alternatív kockázatértékelési stratégiája a klinikai kockázati tényezők értékelése. A születéskori terhességet, az előző testvérnél kezelést igénylő sárgaságot, az oxitocin infúziót, az instrumentális szülést, a szülési traumát és a nem megfelelő táplálást az SHB rizikófaktorai közé sorolták .
A klinikai kockázati modell diszkriminációs képessége azonban alacsonyabbnak bizonyult, mint a korai STB mérésé . Newman és munkatársai jobb diszkriminációs képességről számoltak be, amikor egy klinikai kockázati eszközt kombináltak a korai STB méréssel . Mivel kohorszunkban jelentős az alacsony születési súlyú és koraszülött újszülöttek aránya, feltételezzük, hogy ezeknek az objektíven mérhető klinikai kockázati tényezőknek a korai STB-méréssel való kombinációja jobb diszkriminációs képességű kockázati modellt eredményezne.
A vizsgálatban tett megfigyelések külső alkalmazhatóságát befolyásolhatja a hyperbilirubinaemia viszonylag magas előfordulása a vizsgált kohorszban, mivel a fototerápia megkezdéséhez alacsonyabb bilirubin-küszöbértékeket alkalmaznak. A fejlett országokkal ellentétben Indiában alacsonyabb bilirubin csúcsértékeknél jelentettek kernicterust, ami arra utal, hogy az indiai újszülötteknél alacsonyabb szérum bilirubin csúcsértékeknél alakulhat ki bilirubin okozta neurológiai károsodás . Ezenkívül az Indiában született újszülöttek körülbelül egyharmada alacsony születési súlyú. Ezen okok miatt az indiai Nemzeti Neonatológiai Fórum iránymutatásaiban alacsonyabb küszöbértékek alkalmazását javasolja a fototerápia megkezdéséhez, különösen azokon a területeken, ahol a glükóz-6-foszfát-dehidrogenáz-hiány gyakoribb .
Vizsgálatunk erősségei közé tartozik a prospektív vizsgálati terv, a nagy mintanagyság, a több mint 90%-os követési arány és a verifikációs torzítás hiánya. A bevont újszülöttek mintegy 7%-ánál nem tudtuk megállapítani a kimenetel előfordulását. Mivel azonban a korai STB és a demográfiai jellemzők ezeknél a követésből kimaradt újszülötteknél hasonlóak voltak azokhoz, akiknél soha nem alakult ki SHB, az óraspecifikus nomogram és a kockázatértékelő eszköz valószínűleg nem befolyásolja. Nem használtunk nagy teljesítményű folyadékkromatográfiát (HPLC), amely a bilirubin mérésének “arany standard” módszere. A bilirubint az általánosan használt, ágy melletti spektrofotometriás módszerrel mértük. A vizsgálatunkban használt biliméter alacsony variációs együtthatóval rendelkezett, és minden egyes használat előtt kalibráltuk.
Azt javasoljuk, hogy mivel a magas vagy magas-közepes rizikójú zónában a hazabocsátás előtti STB-vel rendelkező újszülötteknél nagy a valószínűsége a korai SHB kialakulásának, ezért gyakori nyomon követést kell biztosítani. Olyan környezetben, ahol a szoros nyomon követés nem kivitelezhető, megfontolandó a kórházból való elbocsátás elhalasztása addig, amíg a bilirubin alacsonyabb kockázati zónába nem csökken. Azok az újszülöttek, akiknek a hazabocsátás előtti STB-je az alacsonyabb-közepes vagy alacsony kockázati zónában van, a helyi politikának megfelelően elbocsáthatók. Biztosítani kell azonban a megfelelő nyomon követést, mivel az SHB későbbi kialakulása nem zárható ki.
Összefoglalva, a megfelelő diszkriminációs képesség ellenére a mi vizsgálatunkban a magasabb szintű nyomon követés növeli a bizalmat a hazabocsátás előtti STB-nek az indiai csecsemők SHB-jét előrejelző képességével kapcsolatban. További vizsgálatokra van szükség az ebben az óraspecifikus bilirubin nomogramban meghatározott kockázati demarkációs zónák teljesítményének validálásához.
Munkatársak: DC: a tanulmány koncepciója és tervezése; UP és SK: adatgyűjtés; DC: az adatok elemzése; UP: a tanulmány szerkesztése DC, SK és SJ kritikus hozzájárulásával. Minden szerző jóváhagyta a kézirat végleges változatát a benyújtásra.
Finanszírozás: Nincs; Versenytárs érdekeltségek:
1. Jelentés 2002-2003: Nemzeti Újszülött Perinatális Adatbázis Hálózat. New Delhi: National Neonatology Forum of India; 2004.
2. Watchko JF. A veszélyes hyperbilirubinaemia kockázatának kitett újszülöttek azonosítása: új klinikai felismerések. Pediatr Clin North Am. 2009;56:671-87.
3. A hyperbilirubinaemia kezelése a 35. vagy több hetes terhességgel született újszülötteknél. Gyermekgyógyászat. 2004;114:297-316.
4. Lodha R, Deorari AK, Jatana V, Paul VK. A teljes szérum bilirubin nem invazív becslése több hullámhosszú spektrális reflexióval újszülötteknél. Indian Pediatr. 2000;37:771-5.
5. Agarwal R, Kaushal M, Aggarwal R, Paul VK, Deorari AK. Korai újszülöttkori hyperbilirubinémia az első napi szérum bilirubinszint segítségével. Indian Pediatr. 2002;39:724-30.
6. Stevenson DK, Fanaroff AA, Maisels MJ, Young BW, Wong RJ, Vreman HJ, et al. Prediction of hyperbilirubinemia in near-term and term infants. Pediatrics 2001;108:31-39.
7. Bhutani VK, Gourley GR, Adler S, Kreamer B, Dalin C, Johnson LH. A teljes szérum bilirubin nem invazív mérése egy több rasszból álló, újszülöttkori előszülött populációban a súlyos hyperbilirubinémia kockázatának felmérésére. Pediatrics. 2000;106:E17.
8. Bhutani VK, Johnson L, Sivieri EM. Az elbocsátás előtti órára jellemző szérum bilirubin prediktív képessége a későbbi szignifikáns hyperbilirubinaemiára egészséges terminális és közel terminális újszülötteknél. Pediatrics. 1999;103:6-14.
9. Ip S, Chung M, Kulig J, O’Brien R, Sege R, Glicken S, et al. An evidence-based review of important issues concerning neonatal hyperbilirubinemia. Pediatrics. 2004;114:e130-53.
10. Trikalinos TA, Chung M, Lau J, Ip S. Systematic review of screening for bilirubin encephalopathy in neonates. Pediatrics. 2009;124:1162-71.
11. Carley S, Dosman S, Jones SR, Harrison M. Egyszerű nomogramok a mintanagyság kiszámításához diagnosztikai vizsgálatokban. Emerg Med J. 2005;22:180-1.
12. Fay DL, Schellhase KG, Suresh GK. Bilirubinszűrés normális újszülötteknél: az óraspecifikus bilirubin nomogram kritikája. Pediatrics. 2009;124:1203-5.
13. Awasthi S, Rehman H. Az újszülöttkori hyperbilirubinaemia korai előrejelzése. Indian J Pediatr. 1998;65:131-9.
14. Sarici SU, Serdar MA, Korkmaz A, Erdem G, Oran O, Tekinalp G, et al. Incidence, course, and prediction of hyperbilirubinemia in near-term and term newborns. Pediatrics. 2004;113:775-80.
15. Keren R, Bhutani VK, Luan X, Nihtianova S, Cnaan A, Schwartz JS. A jelentős hyperbilirubinaemia kockázatának kitett újszülöttek azonosítása: két ajánlott megközelítés összehasonlítása. Arch Dis Child. 2005;90:415-21.
16. Newman TB, Liljestrand P, Escobar GJ. A klinikai kockázati tényezők és a szérum bilirubinszintek kombinálása az újszülöttkori hyperbilirubinaemia előrejelzésére. Arch Pediatr Adolesc Med. 2005;159:113-9.
17. Newman TB, Xiong B, Gonzales VM, Escobar GJ. Az extrém újszülöttkori hyperbilirubinaemia előrejelzése és megelőzése egy érett egészségügyi fenntartó szervezetben. Arch Pediatr Adolesc Med. 2000;154: 1140-7.
18. Keren R, Luan X, Friedman S, Saddlemire S, Cnaan A, Bhutani VK. Alternatív kockázatértékelési stratégiák összehasonlítása a szignifikáns neonatális hyperbilirubinaemia előrejelzésére terminális és közeli korú csecsemőknél. Pediatrics. 2008;121:e170-9.
19. Murki S, Kumar P, Majumdar S, Marwaha N, Narang A. A kernicterus kockázati tényezői terminális csecsemőknél nem hemolitikus sárgaságban. Indian Pediatr. 2001;38:757-62.
20. Agrawal VK, Shukla R, Misra PK, Kapoor RK, Malik GK. Agytörzsi auditív kiváltott válasz újszülötteknél hyperbilirubinaemiával. Indian Pediatr. 1998;35:513-8.
21. Kumar P, Jain N, Thakre R, Murki S, Venkataseshan S (szerk.). Bizonyítékalapú klinikai gyakorlati irányelvek. National Neonatology Forum of India, New Delhi, India, 2010.
22. Kaur G, Srivastav J, Jain S, Chawla D, Chavan BS, Atwal R, et al. Preliminary report on neonatal screening for congenital hypothyroidism, congenital adrenal hyperplasia and glucose-6-phosphate dehydrogenase deficiency: a Chandigarh experience. Indian J Pediatr. 2010;77:969-73.
