U významné části novorozenců se během prvního týdne života vyvine hyperbilirubinémie vyžadující léčbu („významná“ hyperbilirubinémie, SHB) . Zkrácení doby hospitalizace při porodu bylo časově spojeno se zvýšeným výskytem neurologického poškození vyvolaného bilirubinem . Domácí návštěvy zdravotnického pracovníka po propuštění nebo návštěvy rodiny v nemocnici mohou odhalit SHB, ale nejsou všeobecně proveditelné nebo nákladově efektivní. Proto je třeba před propuštěním novorozenců z porodnice identifikovat ty, u nichž hrozí riziko vzniku vysokých hladin bilirubinu
Objektivní posouzení rizika vzniku SHB před propuštěním je důležité také z důvodu omezené přesnosti vizuálního posouzení rozsahu žloutenky . Stratifikace rizika SHB byla provedena měřením bilirubinové zátěže (absolutní hladiny nebo rychlosti vzestupu celkového bilirubinu v séru nebo transkutánního bilirubinu), produkce bilirubinu (vydechovaný oxid uhelnatý) a identifikací základních klinických rizikových faktorů .
Koncentrace bilirubinu v periferní krvi je funkcí věkově specifické rychlosti produkce, metabolismu, vylučování a reabsorpce bilirubinu. Proto je interpretace hladiny bilirubinu u novorozence založena na postnatálním věku. Hodinově specifický nomogram bilirubinu vyvinutý Bhutanim a kol. ukázal, že měření celkového bilirubinu v séru (STB) před propuštěním z porodnice může pomoci při identifikaci novorozenců, u nichž je riziko vyšších percentilových hodnot STB během následného sledování. Z různých metod predikce rizika prokázalo měření STB před propuštěním nejlepší diskriminační schopnost u severoamerických novorozenců . Vzhledem ke geneticky podmíněným rozdílům v metabolismu bilirubinu a odlišnostem ve způsobu výživy se však klinický průběh hyperbilirubinémie může u novorozenců patřících k různým etnikům nebo zeměpisným lokalitám lišit. Předchozí nomogram byl navíc vypracován na základě retrospektivní kohorty, u níž byly informace o výsledku významné hyperbilirubinemie známy pouze u pětiny studované populace . Proto je sestavení hodinově specifického nomogramu bilirubinu u různých populací novorozenců předpokladem pro využití měření bilirubinu před propuštěním jako strategie hodnocení rizika.
Naplánovali jsme tuto prospektivní kohortovou studii s cílem zkonstruovat hodinově specifický nomogram celkového bilirubinu v séru u indických novorozenců a zhodnotit účinnost měření bilirubinu před propuštěním v predikci hyperbilirubinémie vyžadující léčbu u donošených a nedonošených novorozenců.
Metody
Tato prospektivní kohortová studie s hodnocením účinnosti diagnostického testu byla provedena od února do června 2010 ve fakultní nemocnici v severní Indii. Protokol studie byl schválen etickou komisí nemocnice a od rodičů byl získán písemný informovaný souhlas. Do studie mohli být zařazeni zdraví novorozenci s těhotenstvím ≥ 35 týdnů nebo porodní hmotností ≥ 2000 g. Z logistických důvodů nebyli do studie zařazeni novorozenci, kteří dovršili 24 hodin života v neděli. Ze studie byli vyloučeni novorozenci se závažnou vrozenou vývojovou vadou, hospitalizovaní na novorozenecké jednotce intenzivní péče, s pozitivním přímým Coombsovým testem (byl proveden v případě, že krevní skupina matky byla Rhesus negativní), s fototerapií před prvním měřením bilirubinu nebo s nemožností dostavit se ke kontrole.
Měření a sledování: Vzorek krve pro první měření celkového bilirubinu v séru byl odebrán v době metabolického screeningu v 18-30 h postnatálního věku. Kapilární nebo periferní žilní krev byla odebrána do předem heparinizovaných mikrokapilár. Krev byla ihned centrifugována při 12 000 otáčkách za minutu po dobu 5 minut a celkový bilirubin byl měřen spektrofotometrem (NEO-BIL plus, das srl, Itálie).
Neonatologové byli sledováni během pobytu v nemocnici a po propuštění až do ukončení 7. poporodního dne. O načasování následné návštěvy bylo rozhodnuto na základě věku při propuštění. Děti propuštěné před 48. hodinou věku byly volány zpět mezi 72. a 96. hodinou věku a děti propuštěné po 48. hodině věku mezi 96. a 120. hodinou věku. Kromě prvního měření STB v době metabolického screeningu byla u každého novorozence provedena další dvě měření STB. Po prvním měření bylo rozhodnutí o provedení druhého a třetího měření STB založeno na klinickém hodnocení. Klinické posouzení stupně žloutenky bylo doplněno měřením transkutánního bilirubinu (TcB) pomocí transkutánního bilimetru s více vlnovými délkami (BiliChek, variační koeficient <5 %). Odhad STB byl proveden, pokud byly dlaně/plosky zbarveny ikterem nebo TcB byl >12 mg/dl nebo do 80 % prahové hodnoty fototerapie specifické pro daný věk. Pokud to nebylo klinicky indikováno, bylo druhé a třetí měření STB provedeno v 72-96 h a 96-144 h postnatálního věku. Hodnoty STB po zahájení fototerapie nebyly do konstrukce nomogramu zahrnuty.
Byly zaznamenány klinické a epidemiologické rizikové faktory, které mohou ovlivňovat riziko vzniku SHB. Byly zaznamenány následující údaje: porodní hmotnost, gravidita, pohlaví, vzdělání a náboženství matky, parita, předporodní komplikace, krevní skupina ABO a Rh matky, způsob porodu, typ anestezie použité při porodu a použití infuze oxytocinu během porodu. Dále byl zaznamenán věk při zahájení kojení, příkrmy (jiné než kojení nebo odstříkané mateřské mléko) během a po prvních 24 hodinách po porodu a věk při odchodu první stolice.
Výsledky: Klíčovým výsledkem byla významná hyperbilirubinémie (SHB), která byla definována jako potřeba fototerapie nebo výměnné transfuze pro léčbu hyperbilirubinémie. Rozhodnutí o zahájení fototerapie bylo učiněno na základě věku dítěte v hodinách a hladiny STB podle místní adaptace pokynů Americké pediatrické akademie (AAP) . U novorozenců narozených ve 38. a více týdnech těhotenství byla pro zahájení fototerapie použita hranice středního rizika a u novorozenců narozených ve 37. a méně ukončeném týdnu těhotenství hranice vyššího rizika. Hodnoty prahu středního rizika v pokynech AAP jsou téměř totožné s hodnotami 95
percentilu Bhutaniho nomogramu .
Statistická analýza: V prospektivní studii byla významná hyperbilirubinémie pozorována u 10 % novorozenců narozených v ≥35. týdnu těhotenství . Pro vyšetření diagnostického testu se senzitivitou nejméně 95 % (interval spolehlivosti 5 %) a hodnotou alfa 0,05 bylo třeba zařadit přibližně 1000 subjektů .
Data byla analyzována pomocí programu Stata 9 (StataCorp, College Station, TX, USA). Pro konstrukci nomogramu byly hodnoty STB klubány do šestihodinových epoch (věk ± 3 hodiny) pro postnatální věk do 48 h a dvanáctihodinových epoch (věk ± 6 hodin) pro věk nad 48 h. Data pro každou epochu byla zkoumána z hlediska symetrie. Pro každou epochu byly vypočteny hodnoty 5
, 10., 25., 40., 75., 90. a 95. percentilu. K vykreslení nomogramu bilirubinu specifického pro danou hodinu byl použit program Microsoft Excel (Microsoft Corporation, Richmond, USA). Vyhlazený nomogram zobrazující 40., 75. a 95. percentil byl vykreslen pomocí kubického modelování páteře pomocí balíčku GAMLSS pro statistický software R. Po vyhlazení bylo 36,5 % případů pod linií 40. percentilu, 77,8 % případů bylo pod linií 75. percentilu a 95,1 % případů bylo pod linií 95. percentilu. Prediktivní schopnost nomogramu byla hodnocena výpočtem senzitivity, specificity, pozitivní prediktivní hodnoty, negativní prediktivní hodnoty a poměru pravděpodobnosti, vynesením křivky ROC (receiver-operating characteristics) a výpočtem c-statistiky.
Výsledky
V průběhu sledovaného období se narodilo celkem 1255 novorozenců, z nichž 1090 bylo způsobilých k zařazení do studie. Z nich bylo 93 z různých důvodů vyřazeno (obr. 1). Do studie bylo zařazeno celkem 997 novorozenců. Průměrná hodnota ± SD pro porodní hmotnost byla 2627±536 g a pro gestační věk 37,8±1,5 týdne (medián a IQR: 38 a 37-39) (webová tabulka I). Většina studovaných dětí se narodila po nekomplikovaném prenatálním průběhu a měla bezproblémový přechod do mimoděložního života. Více než 80 % novorozenců bylo během hospitalizace výlučně kojeno.
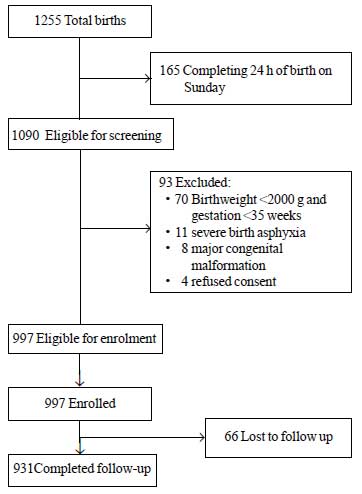
Obr. 1 Průběh studie.
Konstrukce nomogramu bilirubinu: První měření bilirubinu bylo provedeno ve 23,3±6,3 h věku a průměrná hodnota STB byla 7,0±2,0 mg/dl. Na základě prvního měření bilirubinu potřebovalo fototerapii 29 (2,9 %) novorozenců. U těchto novorozenců byla fototerapie zahájena ve 27±5,6 h věku s hladinou STB 12,3±2,0 mg/dl. Šedesát šest (6,6 %) novorozenců bylo po propuštění ze studijní nemocnice ztraceno ze sledování. První hodnota bilirubinu u těchto novorozenců byla srovnatelná s novorozenci, u kterých se SHB nikdy nevyvinul (6,5±1,9 vs 6,7±1,7 mg/dl, P=0,54) a byla významně nižší než u těch, u kterých se SHB vyvinul (6,5±1,9 vs 8,5±2,2 mg/dl, P< 0,001).
Pro konstrukci nomogramu a posouzení rozložení hodnot STB byl postnatální věk rozdělen na šestihodinové epochy pro postnatální věk do 48 h a dvanáctihodinové epochy pro věk nad 48 h. Bylo zjištěno, že STB v každé z epoch s výjimkou 42 h je rozložen symetricky (obr. 2). Distribuce hodnot STB ve 42 h byla pozorována jako pozitivně zkreslená a tyto hodnoty nebyly použity pro konstrukci nomogramu.
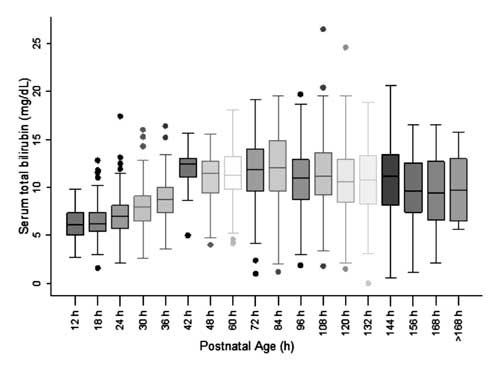
Obr. 2 Box-whisker plot zobrazující distribuci celkového bilirubinu v séru.
Pro každou epochu byly vypočteny hodnoty 5
, 10., 25., 40., 75., 90. a 95. percentilu. Byl nakreslen věkově specifický nomogram sérového bilirubinu s hodnotami 40., 75. a 95. percentilu v postupujícím postnatálním věku (obr. 3)
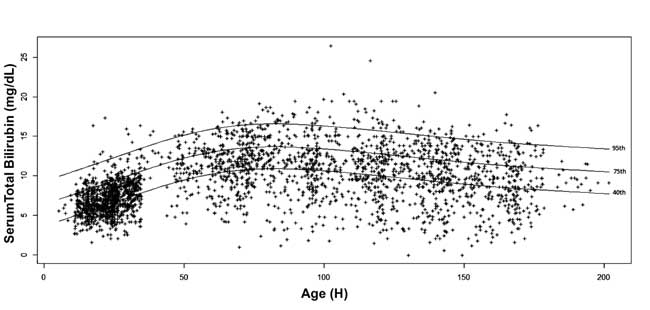
Obr. 3. 3 Bilirubinový nomogram – hodinově specifický celkový bilirubin v séru zobrazený jako 40., 75. a 95. percentil.
Prediktivní schopnost STB před propuštěním: Celkem se u 199 (20 %) novorozenců vyvinula SHB (dostali fototerapii). První hodnota bilirubinu byla použita k predikci následné potřeby léčby hyperbilirubinemie. Pokud byly v prvních 48 hodinách po porodu získány více než dvě hodnoty, byla pro účely predikce použita vyšší percentilová hodnota.
TABLE I Predictive Characteristics of Percentile Values as Risk Demarcators for Subsequent Need of Treatment for Hyperbilirubinemia
| Celkový bilirubin v séru před propuštěním | Výsledek | Výkon testu | |||||
| Percentil | Počet(n=928) | SHB+ | SHB- | PPV | NPV | Citlivost | Specifičnost |
| Nad 95. percentil | 49 | 34 | 15 | 69.4 | 81.2 | 17.1 | 97.9 |
| Pod 95. percentilem | 879 | 165 | 714 | ||||
| Více než 75. percentil | 239 | 107 | 132 | 44.8 | 86.2 | 53.8 | 81.9 |
| Pod 75. percentilem | 689 | 92 | 597 | ||||
| Více než 40. percentil | 586 | 167 | 419 | 28.5 | 90.6 | 83.9 | 42.5 |
| Pod 40. percentilem | 342 | 32 | 310 | ||||
SHB: significant hyperbilirubinemia, PPV: positive predictive value, NPV: negative predictive value. |
|||||||
Mezi novorozenci, kteří měli před.měření STB při propuštění a dokončili sledování (n=928), u 49 (5.3 %) novorozenců byl STB před propuštěním vyšší než 95. percentil věkově specifického rozdělení (tabulka I). Z těchto 34 novorozenců následně potřebovalo fototerapii (pozitivní prediktivní hodnota: 69,4 %, senzitivita: 17,1 %). U 342 (36,8 %) novorozenců byla STB před propuštěním nižší než 40. percentil věkově specifického rozdělení. Z nich 310 novorozenců nepotřebovalo následnou léčbu hyperbilirubinémie (negativní prediktivní hodnota: 90,6 % a specificita: 42,5 %). Pozitivní prediktivní hodnota 75. percentilové hranice byla 44,8 % a negativní prediktivní hodnota 86,2 %. Křivka ROC, jak je znázorněna na obr. 4, ilustruje diagnostickou výkonnost jednotlivých percentilových cut-off s plochou pod křivkou (c-statistika) 0,73.
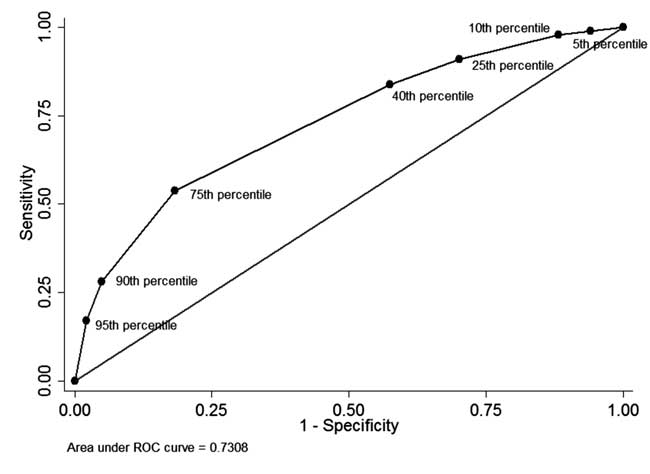
Obr. 4 Křivka ROC pro diagnostickou schopnost různých percentilových cut-off celkového bilirubinu v séru před propuštěním
Poměr pravděpodobnosti (LR) je lepším nástrojem měření diagnostické výkonnosti testu, protože poměr není ovlivněn změnou prevalence výsledku na pozadí. LR pozitivního testu (LR+, pravděpodobnost pozitivního testu u nemocných/pravděpodobnost pozitivního testu u neonemocných) byl vypočten pro každou rizikovou demarkační zónu. STB před propuštěním ≥ 95. percentil byl přiřazen k zóně vysokého rizika, mezi 75. a 94. centilem k zóně vyššího středního rizika, mezi 40. a 74. centilem k zóně nižšího středního rizika a pod 40. percentilem k zóně nízkého rizika. Ze 49 novorozenců v zóně vysokého rizika se u 34 vyvinula SHB; pozitivní LR pro STB v zóně vysokého rizika tedy byla 8,26 (tabulka II). Ze 190 novorozenců v zóně vyššího středního rizika se u 73 vyvinula SHB; pozitivní LR pro STB v této rizikové zóně tedy byla 2,30. Podobně pozitivní LR pro STB v zóně nižšího středního rizika byla 0,76 a pro zónu nízkého rizika 0,37.
TABLE IIPredictive Ability of Pre-discharge Serum Total Bilirubin for Subsequent Significant Hyperbilirubinemia (Need of Phototherapy)
| Před propuštěním celkový bilirubin v séru | Výsledky | Výsledky vyšetření | |||||
| Před propuštěním.vypouštění kumulativní riziková zóna | Percentil | Celkem | SHB+ | SHB- | P:A poměr | Pravděpodobnost onemocnění | LR+ |
| Vysoké riziko | ≥95. | 49 | 34 | 15 | 7:3 | 7/10 | 8.26 |
| Vyšší střední | 75. až 94. | 190 | 73 | 117 | 2:3 | 2/5 | 2.30 |
| Mírně pokročilý | 40. až 74. | 347 | 60 | 287 | 1:5 | 1/6 | 0.76 |
| Nízké riziko | <40. | 342 | 32 | 310 | 1:10 | 1/11 | 0.37 |
| 928 | 199 | 729 | 1:4 | 1/5 | |||
| SHB: významná hyperbilirubinémie; poměr P:A: Přítomnost výsledku : nepřítomnost výsledku. | |||||||
Diskuse
Před propuštěním se doporučuje posoudit riziko následného rozvoje SHB jako potenciální strategie ke snížení výskytu neurologického poškození nebo kernikteru vyvolaného bilirubinem. V této prospektivní kohortové studii jsme sestavili hodinově specifický nomogram sérového bilirubinu u podskupiny severoindických novorozenců a vyhodnotili jsme účinnost vymezení rizika pomocí měření STB před propuštěním při predikci následné potřeby fototerapie (SHB). Základní výskyt SHB byl v našem studijním souboru vysoký – u 2 z 10 novorozenců se vyvinula SHB. Umístění STB před propuštěním ve dvou zónách vyššího rizika významně zvýšilo riziko následné SHB, přičemž u 7 z 10 novorozenců v zóně vysokého rizika došlo k rozvoji SHB (pozitivní LR=8,26) a u 4 z 10 novorozenců v zóně vyššího a středního rizika k rozvoji SHB (pozitivní LR=2,3). Umístění STB před propuštěním v zóně nízkého rizika významně snižovalo riziko následné SHB, přičemž u 1 z 10 novorozenců došlo k rozvoji SHB (pozitivní LR=0,37). Protože však negativní prediktivní hodnota cut-off nízkého rizika byla pouze 90 %, umístění v zóně nízkého rizika nebylo schopno vyloučit možnost následné SHB.
Bhutani a kol. na velkém souboru prokázali, že u novorozenců s STB před propuštěním v zóně vysokého a středního rizika je vyšší pravděpodobnost výskytu SHB během následného sledování. Autoři sestrojili percentilové grafy hladiny sérového bilirubinu v různém postnatálním věku u donošených a donošených novorozenců. Zjistili, že 6,1 % novorozenců mělo před propuštěním sérový bilirubin >95. percentil; 32,1 % těchto novorozenců vykazovalo následně hyperbilirubinémii. Ve srovnání s hodinově specifickým nomogramem podle Bhutani, et al. jsou percentilové hodnoty STB v této studii vyšší až o 2 mg/dl do 84-108 h postnatálního věku. Bylo zjištěno, že novorozenci severoindického původu dosahují vyšších hodnot bilirubinu a mají vyšší výskyt hyperbilirubinémie . Průměrná hodnota STB 7,0 ± 2,0 mg/dl zjištěná v této studii je mezi 75. a 95. percentilem Bhutaniho nomogramu. Podobně Agarwal a kol. uvádějí průměrnou hodnotu STB 5,9±1,8 mg/dl ve 24 hodinách postnatálního věku, která se blíží 75. percentilu Bhutaniho nomogramu. Vyšší podíl předčasně narozených novorozenců nebo novorozenců s nízkou porodní hmotností a vyšší míra výlučného kojení v naší studii mohou být faktory, které přispívají ke zvýšeným hodnotám STB a zvýšenému výskytu SHB. Kromě toho naše rozhodnutí použít střední místo horní linie prahových hodnot fototerapie podle AAP i u novorozenců s nízkým rizikem také zvýšilo výskyt SHB. Po 108 h postnatálního věku jsou percentilové hodnoty STB v této studii nižší než odpovídající hodnoty v Bhutaniho nomogramu. Zahrnutí hodnot STB od novorozenců, kteří byli selektivně sledováni na základě úsudku lékaře pro konstrukci nomogramu, mohlo mít za následek použití vyšších hodnot STB pro vykreslení Bhutaniho nomogramu, a tedy snížení jeho zobecnitelnosti . Vzhledem k tomu, že v této studii bylo sledování ukončeno bez ohledu na závažnost hyperbilirubinémie, dosahuje nomogram vrcholu 4. a 5. den postnatálního věku s přirozeným poklesem na konci prvního týdne.
Agarwal a kol. v prospektivní kohortové studii měřili STB ve 24±6 h věku u 220 novorozenců narozených v ≥35. týdnu těhotenství pro predikci hyperbilirubinémie . Nepřítomnost STB >6 mg/dl ve 24±6 h věku prakticky vyloučila možnost následné SHB (poměr pravděpodobnosti negativního testu 0,07) do 5 dnů po narození. Selektivní měření výsledků pouze u těch novorozenců, kteří měli během sledování „klinickou“ hladinu bilirubinu >10 mg/dl, však vneslo do studie verifikační zkreslení. V jiné indické studii bylo zjištěno, že hraniční hodnota 3,99 mg/dl v 18-24 h má senzitivitu a specificitu po 67 % pro předpověď následné hladiny bilirubinu >15 mg/dl . Úplné sledování však bylo přítomno pouze u kojenců, kteří zůstali v nemocnici buď pro novorozenecké onemocnění, nebo z nějakého důvodu matky, např. císařský řez. Více než 50 % kojenců, kteří byli zdraví, a tedy propuštěni předčasně, nebylo sledováno. Studie z Turecka představila hodinově specifický nomogram bilirubinu u novorozenců s gestačním stářím mezi 35. a 37. týdnem. Hodnota STB vyšší než 95
. percentil měla vysokou pozitivní prediktivní hodnotu pro následný rozvoj SHB . Hodnota STB nižší než 30. percentil však měla negativní prediktivní hodnotu přibližně 90 %. Dvě rozsáhlé retrospektivní studie uvádějí vynikající prediktivní schopnost časného/předpouštěcího měření STB s plochou pod křivkou (AUC) 0,83 . V naší studii byla diskriminační schopnost hodnot 40. a 75. percentilu nižší než dříve uváděné . To posunulo křivku ROC v naší studii směrem k diagonální linii, což vedlo ke snížení diskriminační schopnosti (AUC = 0,73). Vysoká výchozí incidence SHB v turecké (25,3 %) a naší studii (20 %) může vysvětlovat neschopnost nízkých hodnot percentilu vyloučit vznik následné SHB, což omezuje užitečnost měření STB před propuštěním.
Alternativní strategií hodnocení rizika pro predikci následné SHB je hodnocení klinických rizikových faktorů. Jako rizikové faktory SHB byly uváděny gravidita při porodu, žloutenka vyžadující léčbu u předchozího sourozence v anamnéze, infuze oxytocinu, instrumentální porod, porodní trauma a nedostatečná výživa .
Bylo však zjištěno, že diskriminační schopnost modelu klinického rizika je nižší než u časného měření STB . Newman a kol. uvádějí lepší diskriminační schopnost při kombinaci nástroje klinického rizika s časným měřením STB . Vzhledem k významnému podílu novorozenců s nízkou porodní hmotností a předčasně narozených novorozenců v našem souboru předpokládáme, že kombinace těchto objektivně měřitelných klinických rizikových faktorů s časným měřením STB by vytvořila rizikový model s lepší diskriminační schopností.
Vnější použitelnost pozorování provedených ve studii může být ovlivněna relativně vysokým výskytem hyperbilirubinémie ve studijní kohortě z důvodu používání nižších prahových hodnot bilirubinu pro zahájení fototerapie. Na rozdíl od vyspělých zemí byl v Indii kernikterus hlášen při nižších hladinách maximálního bilirubinu, což naznačuje, že u indických novorozenců může dojít k neurologickému poškození způsobenému bilirubinem při nižších maximálních hladinách sérového bilirubinu . Kromě toho má přibližně třetina novorozenců narozených v Indii nízkou porodní hmotnost. Z těchto důvodů indické Národní neonatologické fórum ve svých pokynech navrhuje používat nižší prahové hodnoty pro zahájení fototerapie, zejména v oblastech s vyšším výskytem deficitu glukózo-6-fosfátdehydrogenázy .
Mezi silné stránky naší studie patří prospektivní design studie, velká velikost vzorku, více než 90% míra sledování a absence verifikačního zkreslení. Výskyt výsledku se nám nepodařilo zjistit u přibližně 7 % zařazených novorozenců. Protože však časná STB a demografické charakteristiky u těchto ztracených novorozenců byly podobné těm, u kterých se SHB nikdy nevyvinula, není pravděpodobné, že by byly ovlivněny hodinový nomogram a nástroj pro hodnocení rizika. Nepoužili jsme vysokoúčinnou kapalinovou chromatografii (HPLC), která je „zlatým standardem“ pro měření bilirubinu. Bilirubin jsme měřili běžněji používanou metodou spektrofotometrie u lůžka pacienta. Bilimetr použitý v naší studii měl nízký variační koeficient a před každým použitím byl kalibrován.
Doporučujeme, aby vzhledem k tomu, že novorozenci s STB před propuštěním v zóně vysokého nebo středního rizika mají vysokou pravděpodobnost časného rozvoje SHB, bylo zajištěno jejich časté sledování. V prostředí, kde není možné pečlivé sledování, lze zvážit odložení propuštění z nemocnice do doby, než bilirubin klesne do nižšího rizikového pásma. Novorozence s STB před propuštěním v pásmu nižšího středního nebo nízkého rizika lze propustit podle místní politiky. Mělo by však být zajištěno odpovídající sledování, protože následný rozvoj SHB nelze vyloučit.
Závěrem lze říci, že i přes slušnou diskriminační schopnost zvyšuje vyšší úroveň sledování v naší studii důvěru ve schopnost STB před propuštěním předpovědět SHB u indických kojenců. K ověření účinnosti rizikových demarkačních zón definovaných v tomto hodinově specifickém nomogramu bilirubinu jsou zapotřebí další studie. DC: koncipoval a navrhl studii; UP a SK: shromáždili data; DC: analyzoval data; UP: vypracoval návrh článku s kritickými příspěvky DC, SK a SJ. Všichni autoři schválili konečnou verzi rukopisu určenou k odeslání.
Financování: Žádné; Konkurenční zájmy:
1. Zpráva za období 2002-2003: National Neonatal Perinatal Database Network. New Delhi: National Neonatology Forum of India; 2004.
2. Watchko JF. Identifikace novorozenců s rizikem nebezpečné hyperbilirubinémie: nové klinické poznatky. Pediatr Clin North Am. 2009;56:671-87.
3. Management hyperbilirubinémie u novorozence ve 35. a více týdnech těhotenství. Pediatrie. 2004;114:297-316.
4. Lodha R, Deorari AK, Jatana V, Paul VK. Neinvazivní odhad celkového bilirubinu v séru pomocí vícevlnné spektrální reflektance u novorozenců. Indian Pediatr. 2000;37:771-5.
5. Agarwal R, Kaushal M, Aggarwal R, Paul VK, Deorari AK. Časná neonatální hyperbilirubinémie pomocí hladiny bilirubinu v séru prvního dne. Indian Pediatr. 2002;39:724-30.
6. Stevenson DK, Fanaroff AA, Maisels MJ, Young BW, Wong RJ, Vreman HJ, et al. Prediction of hyperbilirubinemia in near-term and term infants. Pediatrics 2001;108:31-39.
7. Bhutani VK, Gourley GR, Adler S, Kreamer B, Dalin C, Johnson LH. Neinvazivní měření celkového sérového bilirubinu u multirasové populace novorozenců před propuštěním k posouzení rizika závažné hyperbilirubinémie. Pediatrics. 2000;106:E17.
8. Bhutani VK, Johnson L, Sivieri EM. Prediktivní schopnost hodinově specifického sérového bilirubinu před propuštěním pro následnou významnou hyperbilirubinémii u zdravých donošených a téměř donošených novorozenců. Pediatrics. 1999;103:6-14.
9. Ip S, Chung M, Kulig J, O’Brien R, Sege R, Glicken S, et al. An evidence-based review of important issues concerning neonatal hyperbilirubinemia. Pediatrics. 2004;114:e130-53.
10. Trikalinos TA, Chung M, Lau J, Ip S. Systematic review of screening for bilirubin encephalopathy in neonates. Pediatrics. 2009;124:1162-71.
11. Carley S, Dosman S, Jones SR, Harrison M. Jednoduché nomogramy pro výpočet velikosti vzorku v diagnostických studiích. Emerg Med J. 2005;22:180-1.
12. Fay DL, Schellhase KG, Suresh GK. Screening bilirubinu u normálních novorozenců: kritika hodinově specifického nomogramu bilirubinu. Pediatrics. 2009;124:1203-5.
13. Awasthi S, Rehman H. Early prediction of neonatal hyperbilirubinemia (Časná predikce novorozenecké hyperbilirubinémie). Indian J Pediatr. 1998;65:131-9.
14. Sarici SU, Serdar MA, Korkmaz A, Erdem G, Oran O, Tekinalp G, et al. Incidence, course, and prediction of hyperbilirubinemia in near-term and term newborns. Pediatrics. 2004;113:775-80.
15. Keren R, Bhutani VK, Luan X, Nihtianova S, Cnaan A, Schwartz JS. Identifikace novorozenců s rizikem významné hyperbilirubinémie: srovnání dvou doporučených přístupů. Arch Dis Child. 2005;90:415-21.
16. Newman TB, Liljestrand P, Escobar GJ. Kombinace klinických rizikových faktorů se sérovými hladinami bilirubinu k predikci hyperbilirubinémie u novorozenců. Arch Pediatr Adolesc Med. 2005;159:113-9.
17. Newman TB, Xiong B, Gonzales VM, Escobar GJ. Predikce a prevence extrémní neonatální hyperbilirubinémie ve vyspělé zdravotnické organizaci. Arch Pediatr Adolesc Med. 2000;154: 1140-7.
18. Keren R, Luan X, Friedman S, Saddlemire S, Cnaan A, Bhutani VK. A comparison of alternative risk-assessment strategies for predicting significant neonatal hyperbilirubinemia in term and near-term infants [Srovnání alternativních strategií hodnocení rizika pro predikci významné novorozenecké hyperbilirubinémie u donošených a donošených dětí]. Pediatrics. 2008;121:e170-9.
19. Murki S, Kumar P, Majumdar S, Marwaha N, Narang A. Risk factors for kernicterus in term babies with non-hemolytic jaundice. Indian Pediatr. 2001;38:757-62.
20. Agrawal VK, Shukla R, Misra PK, Kapoor RK, Malik GK. Sluchová evokovaná odpověď mozkového kmene u novorozenců s hyperbilirubinémií. Indian Pediatr. 1998;35:513-8.
21. Kumar P, Jain N, Thakre R, Murki S, Venkataseshan S (eds). Evidence Based Clinical Practice Guidelines [Pokyny pro klinickou praxi založené na důkazech]. National Neonatology Forum of India, New Delhi, India, 2010.
22. Kaur G, Srivastav J, Jain S, Chawla D, Chavan BS, Atwal R, et al. Preliminary report on neonatal screening for congenital hypothyroidism, congenital adrenal hyperplasia and glucose-6-phosphate dehydrogenase deficiency: a Chandigarh experience. Indian J Pediatr. 2010;77:969-73.
.
