O proporție semnificativă de nou-născuți dezvoltă hiperbilirubinemie care necesită tratament (hiperbilirubinemie „semnificativă”, SHB) în prima săptămână de viață. Scăderea duratei de spitalizare la naștere a fost asociată temporal cu o incidență crescută a leziunilor neurologice induse de bilirubină . Vizitele la domiciliu efectuate după externare de către un lucrător medical sau vizitele la spital de către familie pot detecta SHB, dar nu sunt universal fezabile sau eficiente din punct de vedere al costurilor. Prin urmare, înainte ca nou-născuții să fie externați din spitalul de nașteri, trebuie identificați cei cu risc de a dezvolta niveluri ridicate de bilirubină
Evaluarea obiectivă înainte de externare pentru riscul de a dezvolta SHB este, de asemenea, importantă din cauza acurateței limitate a evaluării vizuale a amplorii icterului . Stratificarea riscului pentru SHB a fost realizată prin măsurarea încărcăturii de bilirubină (nivelurile absolute sau rata de creștere a bilirubinei totale serice sau a bilirubinei transcutanate), producția de bilirubină (monoxid de carbon expirat) și identificarea factorilor de risc clinic subiacenți .
Concentrația de bilirubină în sângele periferic este o funcție a ratelor specifice vârstei de producție, metabolizare, excreție și reabsorbție a bilirubinei. Prin urmare, interpretarea nivelului de bilirubină la un nou-născut se bazează pe vârsta postnatală. Nomograma bilirubinei specifică orei dezvoltată de Bhutani, et al. a demonstrat că măsurarea bilirubinei totale serice (STB) înainte de externarea din spitalul de nașteri poate ajuta la identificarea nou-născuților care prezintă riscul de a avea valori mai mari ale STB în percentile în timpul urmăririi. Dintre diferitele metode de predicție a riscului, măsurarea STB înainte de externare a demonstrat cea mai bună capacitate de discriminare în rândul nou-născuților nord-americani. Cu toate acestea, din cauza diferențelor determinate genetic în metabolismul bilirubinei și a disimilitudinilor în practicile de hrănire, evoluția clinică a hiperbilirubinemiei poate varia la nou-născuții aparținând unor etnii sau locații geografice diferite. În plus, nomograma anterioară a fost elaborată pe baza unei cohorte retrospective în care informațiile despre rezultatul hiperbilirubinemiei semnificative erau cunoscute doar pentru o cincime din populația studiată . Prin urmare, construirea unei nomograme a bilirubinei specifice fiecărei ore în diferite populații neonatale este o condiție prealabilă pentru a utiliza măsurarea bilirubinei înainte de externare ca o strategie de evaluare a riscului.
Am planificat acest studiu de cohortă prospectiv pentru a construi o nomogramă a bilirubinei totale serice specifică orei la nou-născuții indieni și pentru a evalua eficacitatea măsurării bilirubinei înainte de externare în prezicerea hiperbilirubinemiei care necesită tratament în rândul nou-născuților la termen și a nou-născuților prematuri târzii.
Metode
Acest studiu de cohortă prospectiv cu evaluarea performanței testelor de diagnosticare a fost efectuat în perioada februarie-iunie 2010 la un spital universitar din nordul Indiei. Protocolul studiului a fost aprobat de Comitetul de etică al spitalului și s-a obținut consimțământul informat în scris de la părinți. Nou-născuții sănătoși cu gestație ≥35 săptămâni sau greutate la naștere ≥2000 g au fost eligibili pentru înscrierea în studiu. Din motive logistice, nou-născuții care au împlinit 24 h de viață duminica nu au fost eligibili pentru înscrierea în studiu. Au fost excluși nou-născuții cu malformații congenitale majore, admiterea în unitatea de terapie intensivă neonatală, testul Coombs direct pozitiv (a fost efectuat dacă grupul sanguin al mamei era Rhesus negativ), fototerapie înainte de prima măsurare a bilirubinei sau incapacitatea de a veni pentru urmărire.
Măsurătorile studiului și urmărirea: Proba de sânge pentru prima măsurare a bilirubinei totale serice a fost prelevată în momentul screeningului metabolic la 18-30 h de vârstă postnatală. Sângele venos capilar sau periferic a fost recoltat în microcapilare preheparinizate. Sângele a fost centrifugat imediat la 12000 rpm timp de 5 minute și bilirubina totală a fost măsurată cu un spectrofotometru (NEO-BIL plus, das srl, Italia).
Neonații au fost urmăriți în timpul șederii în spital și după externare până la finalizarea celei de-a 7-a zile postnatale. Momentul vizitei de urmărire a fost decis în funcție de vârsta la externare. Bebelușii externați înainte de 48 de ore au fost rechemați între 72 și 96 de ore, iar bebelușii externați după 48 de ore între 96 și 120 de ore. În plus față de prima măsurare a STB în momentul screeningului metabolic, au fost efectuate încă două măsurători STB la fiecare nou-născut. După prima măsurare, decizia de a efectua a doua și a treia măsurare a STB s-a bazat pe evaluarea clinică. Evaluarea clinică a gradului de icter a fost însoțită de măsurarea bilirubinei transcutanate (TcB) cu un bilimetru transcutanat cu mai multe lungimi de undă (BiliChek, coeficient de variație <5%). Estimarea STB s-a făcut dacă palmele/solii erau colorate cu icter sau TcB era >12 mg/dL sau în limita a 80% din pragul de fototerapie specific vârstei. Dacă nu era indicată clinic, a doua și a treia măsurare a STB s-a făcut la 72-96 h și, respectiv, 96-144 h de la vârsta postnatală. Valorile STB după începerea fototerapiei nu au fost incluse pentru construirea nomogramei.
Au fost înregistrați factorii de risc clinic și epidemiologic care pot influența riscul de a dezvolta SHB. Au fost înregistrate următoarele date: greutatea la naștere, gestația, sexul, educația și religia maternă, paritatea, complicațiile prenatale, grupa sanguină ABO și Rh maternă, modul de naștere, tipul de anestezie utilizat în timpul nașterii și utilizarea perfuziei de oxitocină în timpul travaliului. În plus, au fost notate, de asemenea, vârsta la inițierea hrănirii, alimentația suplimentară (alta decât alimentația la sân sau laptele matern exprimat) în timpul și după primele 24 de ore de la naștere și vârsta la trecerea primului scaun.
Rezultat: Rezultatul cheie a fost hiperbilirubinemia semnificativă (SHB) care a fost definită ca necesitate de fototerapie sau transfuzie de schimb pentru tratamentul hiperbilirubinemiei. Decizia de a începe fototerapia a fost luată pe baza vârstei copilului în ore și a nivelurilor STB, conform adaptării locale a ghidurilor Academiei Americane de Pediatrie (AAP) . La nou-născuții născuți la 38 sau mai multe săptămâni de gestație, s-a folosit pragul de risc mediu, iar la nou-născuții născuți la 37 sau mai puțin de săptămâni complete de gestație, pragul de risc mai ridicat, pentru a iniția fototerapia. Valorile pragului de risc mediu din ghidurile AAP sunt aproape identice cu valorile percentilei 95
a din nomograma Bhutani .
Analiză statistică: Într-un studiu prospectiv a fost observată o hiperbilirubinemie semnificativă la 10% dintre nou-născuții născuți la ≥35 săptămâni de gestație . Pentru investigarea unui test de diagnostic cu o sensibilitate de cel puțin 95% (interval de încredere 5%) și o valoare alfa de 0,05, a fost nevoie de înscrierea a aproximativ 1000 de subiecți .
Datele au fost analizate folosind Stata 9 (StataCorp, College Station, TX, SUA). Pentru construirea nomogramei, valorile STB au fost clubate în epoci de șase ore (vârstă±3 ore) pentru vârsta postnatală până la 48 h și epoci de douăsprezece ore (vârstă±6 ore) pentru vârsta peste 48 h. Datele pentru fiecare epocă au fost examinate pentru simetrie. Valorile percentilei 5
, 10, 25, 40, 75, 90 și 95 au fost calculate pentru fiecare epocă. Microsoft Excel (Microsoft Corporation, Richmond, SUA) a fost utilizat pentru a trasa nomograma bilirubinei specifică orei. Nomograma netezită care descrie percentila 40, 75 și 95 a fost trasată cu ajutorul modelării coloanei vertebrale cubice cu ajutorul pachetului GAMLSS pentru software-ul statistic R. După netezire, 36,5 % dintre cazuri au fost sub linia percentilei 40, 77,8 % dintre cazuri au fost sub linia percentilei 75 și 95,1 % dintre cazuri au fost sub linia percentilei 95. Capacitatea predictivă a nomogramei a fost evaluată prin calcularea sensibilității, a specificității, a valorii predictive pozitive, a valorii predictive negative și a raportului de verosimilitate, prin trasarea curbei caracteristicilor de funcționare a receptorului (ROC) și prin calcularea statisticii c.
Rezultate
În timpul perioadei de studiu, s-au născut în total 1255 de nou-născuți, dintre care 1090 au fost eligibili pentru înrolare. Dintre aceștia, 93 au fost excluși din diferite motive (Fig. 1). Un total de 997 de nou-născuți au fost înrolați în studiu. Valoarea medie ± SD pentru greutatea la naștere a fost de 2627±536 g, iar pentru vârsta de gestație a fost de 37,8±1,5 săptămâni (mediana și IQR: 38 și 37-39) (Tabelul Web I). Majoritatea sugarilor din studiu s-au născut după o evoluție antenatală fără complicații și au avut o tranziție fără evenimente la viața extrauterină. Mai mult de 80% dintre nou-născuți au fost alăptați exclusiv la sân în timpul șederii în spital.
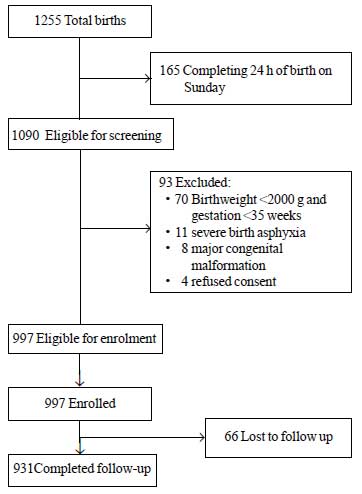
Fig.1 Fluxul studiului.
Construcția nomogramei bilirubinei: Prima măsurare a bilirubinei a fost efectuată la vârsta de 23,3±6,3 h, iar STB medie a fost de 7,0±2,0 mg/dL. Douăzeci și nouă (2,9%) de nou-născuți au avut nevoie de fototerapie pe baza primei măsurători a bilirubinei. La acești nou-născuți, fototerapia a fost începută la vârsta de 27±5,6 h, cu niveluri STB de 12,3±2,0 mg/dL. Șaizeci și șase (6,6%) de nou-născuți au fost pierduți la urmărire după externarea din spitalul de studiu. Prima valoare a bilirubinei la acești nou-născuți a fost comparabilă cu cea a nou-născuților care nu au dezvoltat niciodată SHB (6,5±1,9 vs 6,7±1,7 mg/dL, P=0,54) și a fost semnificativ mai mică decât a celor care au dezvoltat SHB (6,5±1,9 vs 8,5±2,2 mg/dL, P< 0,001).
Pentru construirea nomogramei și evaluarea distribuției valorilor STB, vârsta postnatală a fost împărțită în epoci de șase ore pentru vârsta postnatală de până la 48 h și epoci de douăsprezece ore pentru vârsta de peste 48 h. S-a observat că STB la fiecare dintre epoci, cu excepția celei de 42 h, a fost distribuită simetric (Fig. 2). Distribuția valorilor STB la 42 h a fost observată ca fiind înclinată pozitiv și aceste valori nu au fost utilizate pentru construirea nomogramei.
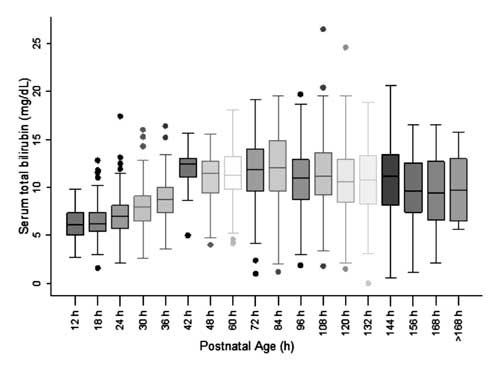
Fig. 2 Graficul Box-whisker care arată distribuția bilirubinei totale serice.
S-au calculat valorile percentililor 5
, 10, 25, 40, 75, 90 și 95 pentru fiecare epocă. A fost trasată nomograma bilirubinei serice specifică vârstei cu valorile percentilei 40, 75 și 95 la avansarea vârstei postnatale (Fig. 3).
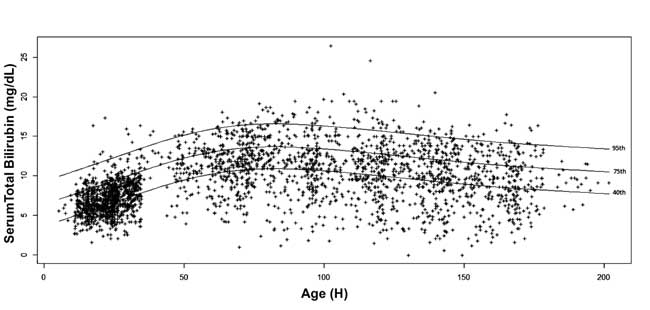
Fig. 3 Nomograma bilirubinei – bilirubina serică totală specifică orei reprezentată cu percentilele 40, 75 și 95.
Capacitatea predictivă a STB înainte de externare: În total, 199 (20%) nou-născuți au dezvoltat SHB (au primit fototerapie). Prima valoare a bilirubinei a fost utilizată pentru a prezice nevoia ulterioară de tratament pentru hiperbilirubinemie. În cazul în care au fost obținute mai mult de două valori în primele 48 de ore de la naștere, valoarea percentila mai mare a fost utilizată în scopul predicției.
TABLE I Predictive Characteristics of Percentile Values as Risk Demarcators for Subsequent Need of Treatment for Hyperbilirubinemia
| Bilirubina totală serică înainte de externare | Rezultat | Rezultatele testului | |||||||
| Percentila | Număr(n=928) | SHB+ | SHB- | PPV | NPV | Sensibilitate | Specificitate | ||
| Superioară percentilei 95 | 49 | 34 | 15 | 69.4 | 81.2 | 17.1 | 97.9 | ||
| Dincolo de percentila 95 | 879 | 165 | 714 | ||||||
| Supra percentila 75 | 239 | 107 | 132 | 44.8 | 86.2 | 53.8 | 81.9 | ||
| Sub percentila 75 | 689 | 92 | 597 | ||||||
| Supra percentila 40 | 586 | 167 | 419 | 28.5 | 90.6 | 83.9 | 42.5 | ||
| Sub percentila 40 | 342 | 32 | 310 | ||||||
SHB: significant hyperbilirubinemia, PPV: positive predictive value, NPV: negative predictive value. |
|||||||||
Printre nou-născuții care au avut pre-măsurarea STB la externare și au finalizat urmărirea (n=928), în 49 (5.3%) nou-născuți STB înainte de externare a fost mai mare decât percentila 95 a distribuției specifice vârstei (tabelul I). Dintre aceștia, 34 de nou-născuți au necesitat ulterior fototerapie (valoare predictivă pozitivă: 69,4 %, sensibilitate: 17,1 %). La 342 (36,8%) de nou-născuți, STB înainte de externare a fost mai mică decât a 40-a percentila a distribuției specifice vârstei. Dintre aceștia, 310 nou-născuți nu au avut nevoie de tratament ulterior pentru hiperbilirubinemie (valoare predictivă negativă: 90,6% și specificitate: 42,5%). Valoarea predictivă pozitivă a cut-off-ului percentilei 75 a fost de 44,8% și valoarea predictivă negativă a fost de 86,2%. Curba ROC, așa cum este prezentată în Fig. 4, ilustrează performanța diagnostică a fiecărui percentile-cutoff, aria sub curbă (statistica c) fiind de 0,73.
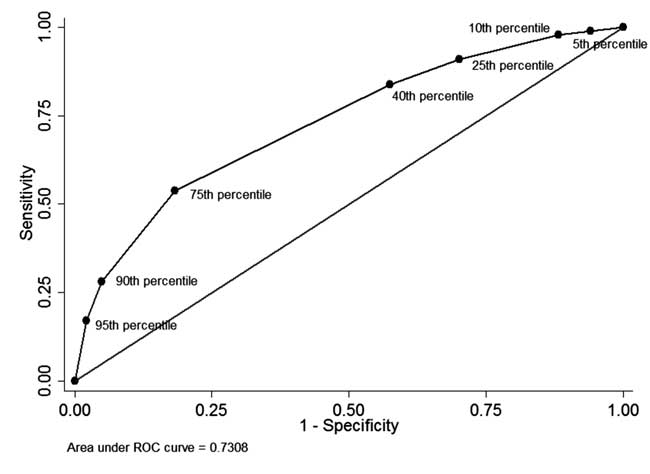
Fig. 4 Curba ROC pentru capacitatea de diagnosticare a diferitelor cut-off-uri de percentila ale bilirubinei totale serice înainte de externare.
Raportul de probabilitate (LR) este un instrument mai bun de măsurare a performanței testului de diagnostic, deoarece raportul nu este afectat de modificarea prevalenței de fond a rezultatului. LR al testului pozitiv (LR+, probabilitatea ca testul să fie pozitiv în cazul bolnavilor/ probabilitatea ca testul să fie pozitiv în cazul celor care nu sunt bolnavi) a fost calculat pentru fiecare zonă de demarcație a riscului. Un STB înainte de externare de ≥95 percentila a fost atribuit ca fiind în zona de risc ridicat, între 75 și 94 percentila în zona de risc intermediar-superior, între 40 și 74 percentila în zona de risc intermediar-inferior și sub 40 percentila în zona de risc scăzut. Dintre cei 49 de nou-născuți din zona de risc înalt, 34 au dezvoltat SHB; prin urmare, LR pozitiv pentru STB în zona de risc înalt a fost de 8,26 (tabelul II). Dintre cei 190 de nou-născuți din zona de risc mediu-superior, 73 au dezvoltat SHB; prin urmare, LR pozitiv pentru STB în această zonă de risc a fost de 2,30. În mod similar, LR pozitiv pentru STB în zona de risc inferior-intermediar a fost de 0,76, iar pentru zona de risc scăzut a fost de 0,37.
TABLE IIPredictive Ability of Pre-discharge Serum Total Bilirubin for Subsequent Significant Hyperbilirubinemia (Need of Phototherapy)
| Bilirubina totală serică înainte de externare | Rezultat | Performanța testelor | |||||||
| Pre-zona de risc cumulativ la descărcare | Percentila | Total | SHB+ | SHB- | P:A ratio | Probabilitatea de îmbolnăvire | LR+ | ||
| Risc ridicat | ≥95th | 49 | 34 | 15 | 7:3 | 7/10 | 8.26 | ||
| Intermediar-superior | De la 75 la 94 | 190 | 73 | 117 | 2:3 | 2/5 | 2.30 | ||
| Lower-intermediate | 40th to 74th | 347 | 60 | 287 | 1:5 | 1/6 | 0.76 | ||
| Risc scăzut | <40th | 342 | 32 | 310 | 1:10 | 1/11 | 0.37 | ||
| 928 | 199 | 729 | 1:4 | 1/5 | |||||
| SHB: hiperbilirubinemie semnificativă; raport P:A: Prezența rezultatului : Absența rezultatului. | |||||||||
Discuție
Evaluarea riscului înainte de externare pentru dezvoltarea ulterioară a SHB este recomandată ca o strategie potențială pentru a reduce incidența leziunilor neurologice induse de bilirubină sau a kernicterului. În acest studiu de cohortă prospectiv, am construit o nomogramă a bilirubinei serice specifică orei la un subgrup de nou-născuți din nordul Indiei și am evaluat eficacitatea demarcării riscului prin măsurarea STB înainte de externare pentru a prezice nevoia ulterioară de fototerapie (SHB). Incidența de bază a SHB a fost ridicată în cohorta studiului nostru, 2 din 10 nou-născuți dezvoltând SHB. Localizarea STB înainte de externare în două zone de risc mai ridicat a crescut semnificativ riscul de SHB ulterior, 7 din 10 nou-născuți din zona de risc ridicat dezvoltând SHB (LR pozitiv=8,26) și 4 din 10 nou-născuți din zona de risc înalt-intermediar dezvoltând SHB (LR pozitiv=2,3). Amplasarea STB înainte de externare în zona de risc scăzut a scăzut semnificativ riscul de SHB ulterioară, 1 din 10 nou-născuți dezvoltând SHB (LR pozitiv=0,37). Cu toate acestea, deoarece valoarea predictivă negativă a cut-off-ului de risc scăzut a fost de numai 90%, localizarea în zona de risc scăzut nu a fost capabilă să excludă posibilitatea unei SHB ulterioare.
Bhutani, et al. au arătat într-o cohortă mare că nou-născuții cu STB înainte de externare în zonele de risc înalt și înalt-intermediar au o probabilitate mai mare de a avea SHB în timpul urmăririi. Autorii au construit diagrame de percentile ale nivelului de bilirubină serică la diferite vârste postnatale la nou-născuți la termen și la termen. Ei au constatat că 6,1% dintre nou-născuți au avut bilirubina serică înainte de externare > percentila 95; 32,1% dintre acești nou-născuți au prezentat ulterior hiperbilirubinemie. În comparație cu nomograma orară specifică a lui Bhutani, et al. , valorile percentilei de STB din acest studiu sunt mai mari cu până la 2 mg/dL până la 84-108 h de vârstă postnatală. S-a observat că nou-născuții de origine nord-indiană ating valori mai mari ale bilirubinei și au o incidență mai mare a hiperbilirubinemiei . STB medie de 7,0±2,0 mg/dL observată în acest studiu se situează între percentila 75 și 95 a nomogramei Bhutani. În mod similar, Agarwal, et al. au raportat o STB medie de 5,9±1,8 mg/dL la 24 h de vârstă postnatală, care este aproape de valoarea percentilei 75 a nomogramei Bhutani. Proporția mai mare de nou-născuți prematuri sau cu greutate mică la naștere și rata mai mare de alăptare exclusivă în studiul nostru pot fi factorii care contribuie la creșterea valorilor STB și la creșterea incidenței SHB. În plus, decizia noastră de a utiliza linia de mijloc în loc de linia superioară a pragurilor de fototerapie AAP chiar și la nou-născuții cu risc scăzut a crescut, de asemenea, incidența SHB. Dincolo de 108 h de vârstă postnatală, valorile percentilice ale STB din acest studiu sunt mai mici decât valorile corespunzătoare din nomograma Bhutani. Includerea valorilor STB de la nou-născuții care au fost urmăriți în mod selectiv la aprecierea clinicianului pentru construirea nomogramei ar fi putut duce la utilizarea unor niveluri mai ridicate de STB pentru trasarea nomogramei Bhutani, diminuând astfel generalizabilitatea acesteia din urmă . În studiul de față, deoarece urmărirea a fost finalizată indiferent de severitatea hiperbilirubinemiei, nomograma atinge vârful în a 4-a și a 5-a zi de vârstă postnatală, cu un declin natural la sfârșitul primei săptămâni.
Într-un studiu de cohortă prospectiv, Agarwal, et al. au măsurat STB la vârsta de 24±6 h la 220 de nou-născuți născuți la ≥35 săptămâni de gestație pentru predicția hiperbilirubinemiei . Absența STB >6 mg/dL la vârsta de 24±6 h a exclus practic posibilitatea unei SHB ulterioare (raportul de probabilitate al testului negativ 0,07) în termen de 5 zile de la naștere. Cu toate acestea, măsurarea selectivă a rezultatului numai la acei nou-născuți care în timpul urmăririi au avut un nivel „clinic” al bilirubinei >10 mg/dL a introdus o prejudecată de verificare în studiu. Într-un alt studiu indian, s-a constatat că un cut-off de 3,99 mg/dL la 18-24 h a avut o sensibilitate și o specificitate de 67% fiecare pentru predicția nivelului ulterior de bilirubină >15 mg/dL . Cu toate acestea, urmărirea completă a fost prezentă numai în cazul sugarilor care au rămas în spital fie din cauza unei boli neonatale, fie din anumite motive materne, cum ar fi operația cezariană. Mai mult de 50% dintre nou-născuți, care erau sănătoși și, prin urmare, au fost externați mai devreme, nu au fost urmăriți. Un studiu din Turcia a prezentat nomograma bilirubinei specifice fiecărei ore la nou-născuții cu o vârstă gestațională între 35 și 37 de săptămâni. Valoarea STB mai mare decât percentila 95
a a avut o valoare predictivă pozitivă ridicată pentru dezvoltarea ulterioară a SHB . Cu toate acestea, valoarea STB mai mică de percentila 30 a avut o valoare predictivă negativă de aproximativ 90%. Două studii retrospective mari au raportat o capacitate predictivă excelentă a măsurării timpurii/prealabile la externare a STB cu o arie sub curbă (AUC) de 0,83 . În studiul nostru, capacitatea de discriminare a valorilor percentilei 40 și 75 a fost mai mică decât cele raportate anterior . Acest lucru a deplasat curba ROC în studiul nostru spre linia diagonală, ceea ce a dus la scăderea capacității de discriminare (AUC= 0,73). Incidența inițială ridicată a SHB în Turcia (25,3%) și în studiul nostru (20%) poate explica incapacitatea valorilor percentilei scăzute de a exclude dezvoltarea SHB ulterioare, limitând astfel utilitatea măsurării STB înainte de externare.
O strategie alternativă de evaluare a riscului pentru predicția SHB ulterioare este evaluarea factorilor de risc clinic. Gestația la naștere, istoricul de icter care a necesitat tratament la fratele anterior, infuzia de oxitocină, nașterea instrumentală, traumatismul la naștere și alimentația inadecvată au fost implicați ca factori de risc de SHB .
Cu toate acestea, s-a raportat că capacitatea de discriminare a modelului de risc clinic este mai mică decât cea a măsurării timpurii a STB . Newman, et al. au raportat o capacitate de discriminare îmbunătățită atunci când un instrument de risc clinic a fost combinat cu măsurarea timpurie a STB . Datorită proporției semnificative de nou-născuți cu greutate mică la naștere și de nou-născuți prematur în cohorta noastră, speculăm că combinarea acestor factori de risc clinic măsurabili în mod obiectiv cu măsurarea timpurie a STB ar genera un model de risc cu o capacitate de discriminare îmbunătățită.
Aplicabilitatea externă a observațiilor făcute în cadrul studiului poate fi influențată de incidența relativ ridicată a hiperbilirubinemiei în cohorta de studiu din cauza utilizării unor praguri mai mici de bilirubină pentru începerea fototerapiei. Spre deosebire de țările dezvoltate, kernicterul a fost raportat la niveluri mai scăzute ale vârfului de bilirubină în India, ceea ce indică faptul că nou-născuții indieni pot dezvolta leziuni neurologice induse de bilirubină la niveluri mai scăzute ale vârfului de bilirubină serică . În plus, aproximativ o treime dintre nou-născuții născuți în India au o greutate mică la naștere. Din aceste motive, Forumul Național de Neonatologie din India, în ghidurile sale, sugerează utilizarea unor praguri mai mici pentru începerea fototerapiei, în special în zonele cu o incidență mai mare a deficitului de glucoză-6-fosfat dehidrogenază .
Punctele forte ale studiului nostru includ designul prospectiv al studiului, dimensiunea mare a eșantionului, rata de urmărire mai mare de 90% și absența prejudecăților de verificare. Nu am putut constata apariția rezultatului la aproximativ 7% dintre nou-născuții înrolați. Cu toate acestea, deoarece STB timpuriu și caracteristicile demografice la acești nou-născuți pierduți la urmărire au fost similare cu cei care nu au dezvoltat niciodată SHB, este puțin probabil ca nomograma specifică orei și instrumentul de evaluare a riscului să fie afectate. Nu am utilizat cromatografia lichidă de înaltă performanță (HPLC), care este metoda „gold-standard” pentru măsurarea bilirubinei. Am măsurat bilirubina prin spectrofotometrie, o metodă mai frecvent utilizată la patul bolnavului. Bilimetrul utilizat în studiul nostru a avut un coeficient de variație scăzut și a fost calibrat înainte de fiecare utilizare.
Recomandăm că, deoarece nou-născuții cu STB înainte de externare în zona de risc înalt sau înalt-intermediar au o probabilitate mare de a dezvolta SHB precoce și trebuie asigurată o urmărire frecventă. În mediile în care urmărirea atentă nu este fezabilă, se poate lua în considerare amânarea externării din spital până când bilirubina scade în zone de risc mai mici. Nou-născuții cu STB înainte de externare în zonele de risc scăzut-intermediar sau scăzut pot fi externați în conformitate cu politica locală. Cu toate acestea, trebuie asigurată o urmărire adecvată, deoarece dezvoltarea ulterioară a SHB nu poate fi exclusă.
În concluzie, în ciuda unei capacități de discriminare corecte, nivelul mai ridicat de urmărire din studiul nostru crește încrederea în capacitatea STB înainte de externare de a prezice SHB la nou-născuții indieni. Sunt necesare studii suplimentare pentru a valida performanța zonelor de demarcație a riscului definite în această nomogramă de bilirubină specifică orei.
Contribuabili: Prof: DC: a conceptualizat și proiectat studiul; UP și SK: au colectat datele; DC: a analizat datele; UP: a redactat lucrarea cu contribuții critice de la DC, SK și SJ. Toți autorii aprobă versiunea finală a manuscrisului în vederea trimiterii.
Finanțare: Nici unul; Interese concurente: Nici unul declarat.
1. Raport 2002-2003: Rețeaua națională de baze de date neonatale perinatale. New Delhi: Forumul Național de Neonatologie din India; 2004.
2. Watchko JF. Identificarea nou-născuților cu risc de hiperbilirubinemie periculoasă: perspective clinice emergente. Pediatr Clin North Am. 2009;56:671-87.
3. Managementul hiperbilirubinemiei la nou-născutul cu 35 sau mai multe săptămâni de gestație. Pediatrie. 2004;114:297-316.
4. Lodha R, Deorari AK, Jatana V, Paul VK. Estimarea non-invazivă a bilirubinei serice totale prin reflectanță spectrală cu mai multe lungimi de undă la nou-născuți. Indian Pediatr. 2000;37:771-5.
5. Agarwal R, Kaushal M, Aggarwal R, Paul VK, Deorari AK. Hiperbilirubinemia neonatală precoce utilizând nivelul de bilirubină serică din prima zi. Indian Pediatr. 2002;39:724-30.
6. Stevenson DK, Fanaroff AA, Maisels MJ, Young BW, Wong RJ, Vreman HJ, et al. Predicția hiperbilirubinemiei la nou-născuții aproape de termen și la termen. Pediatrics 2001;108:31-39.
7. Bhutani VK, Gourley GR, Adler S, Kreamer B, Dalin C, Johnson LH. Măsurarea neinvazivă a bilirubinei serice totale la o populație multirasială de nou-născuți înainte de externare pentru a evalua riscul de hiperbilirubinemie severă. Pediatrie. 2000;106:E17.
8. Bhutani VK, Johnson L, Sivieri EM. Capacitatea de predicție a unei bilirubine serice specifice orei înainte de externare pentru o hiperbilirubinemie semnificativă ulterioară la nou-născuții sănătoși la termen și aproape de termen. Pediatrie. 1999;103:6-14.
9. Ip S, Chung M, Kulig J, O’Brien R, Sege R, Glicken S, et al. An evidence-based review of important issues concerning neonatal hyperbilirubinemia. Pediatrie. 2004;114:e130-53.
10. Trikalinos TA, Chung M, Lau J, Ip S. Ip S. Revizuirea sistematică a screening-ului pentru encefalopatie bilirubinică la nou-născuți. Pediatrie. 2009;124:1162-71.
11. Carley S, Dosman S, Jones SR, Harrison M. Nomograme simple pentru a calcula dimensiunea eșantionului în studiile de diagnosticare. Emerg Med J. 2005;22:180-1.
12. Fay DL, Schellhase KG, Suresh GK. Screeningul bilirubinei pentru nou-născuții normali: o critică a nomogramei bilirubinei specifice orei. Pediatrie. 2009;124:1203-5.
13. Awasthi S, Rehman H. Predicția precoce a hiperbilirubinemiei neonatale. Indian J Pediatr. 1998;65:131-9.
14. Sarici SU, Serdar MA, Korkmaz A, Erdem G, Oran O, Tekinalp G, et al. Incidența, evoluția și predicția hiperbilirubinemiei la nou-născuții aproape de termen și la termen. Pediatrie. 2004;113:775-80.
15. Keren R, Bhutani VK, Luan X, Nihtianova S, Cnaan A, Schwartz JS. Identificarea nou-născuților cu risc de hiperbilirubinemie semnificativă: o comparație a două abordări recomandate. Arch Dis Child. 2005;90:415-21.
16. Newman TB, Liljestrand P, Escobar GJ. Combinarea factorilor de risc clinic cu nivelurile serice de bilirubină pentru a prezice hiperbilirubinemia la nou-născuți. Arch Pediatr Adolesc Med. 2005;159:113-9.
17. Newman TB, Xiong B, Gonzales VM, Escobar GJ. Predicția și prevenirea hiperbilirubinemiei neonatale extreme într-o organizație de întreținere a sănătății matură. Arch Pediatr Adolesc Med. 2000;154: 1140-7.
18. Keren R, Luan X, Friedman S, Saddlemire S, Cnaan A, Bhutani VK. O comparație a strategiilor alternative de evaluare a riscului pentru prezicerea hiperbilirubinemiei neonatale semnificative la nou-născuții la termen și aproape de termen. Pediatrics. 2008;121:e170-9.
19. Murki S, Kumar P, Majumdar S, Marwaha N, Narang A. Factori de risc pentru kernicterus la nou-născuții la termen cu icter non-hemolitic. Indian Pediatr. 2001;38:757-62.
20. Agrawal VK, Shukla R, Misra PK, Kapoor RK, Malik GK. Răspunsul evocat auditiv al trunchiului cerebral la nou-născuții cu hiperbilirubinemie. Indian Pediatr. 1998;35:513-8.
21. Kumar P, Jain N, Thakre R, Murki S, Venkataseshan S (eds). Ghiduri de practică clinică bazate pe dovezi. National Neonatology Forum of India, New Delhi, India, 2010.
22. Kaur G, Srivastav J, Jain S, Chawla D, Chavan BS, Atwal R, et al. Preliminary report on neonatal screening for congenital hypothyroidism, congenital adrenal hyperplasia and glucose-6-phosphate dehydrogenase deficiency: a Chandigarh experience. Indian J Pediatr. 2010;77:969-73.
.
