Leerdoelen
- De opbouw en het gebruik van een typisch fasediagram verklaren
- Fasediagrammen gebruiken om stabiele fasen bij gegeven temperaturen en drukken te identificeren, en om faseovergangen te beschrijven die het gevolg zijn van veranderingen in deze eigenschappen
- Beschrijf de superkritische vloeibare fase van de materie
In de vorige module werd de variatie van de evenwichtsdampdruk van een vloeistof met de temperatuur beschreven. Gezien de definitie van het kookpunt geven grafieken van dampspanning versus temperatuur weer hoe het kookpunt van de vloeistof varieert met de druk. Ook werd het gebruik van verwarmings- en afkoelingscurven beschreven om het smelt- (of vries-) punt van een stof te bepalen. Het verrichten van dergelijke metingen over een breed drukbereik levert gegevens op die grafisch kunnen worden weergegeven als een fasediagram. Een fasediagram is een combinatie van grafieken van druk versus temperatuur voor de fasenovergang vloeistof-gas, vast-vloeibaar, en vast-gas van een stof. Deze diagrammen geven de fysische toestanden aan die bestaan onder specifieke omstandigheden van druk en temperatuur, en geven ook de drukafhankelijkheid van de fase-overgangstemperaturen (smeltpunten, sublimatiepunten, kookpunten). Een typisch fasediagram voor een zuivere stof is weergegeven in figuur 1.
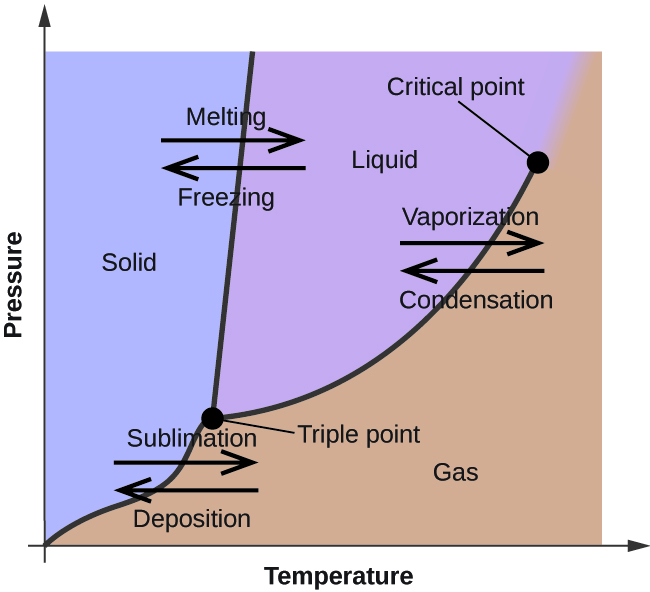
Om het nut van deze diagrammen te illustreren, bekijken we het fasediagram voor water in figuur 2.
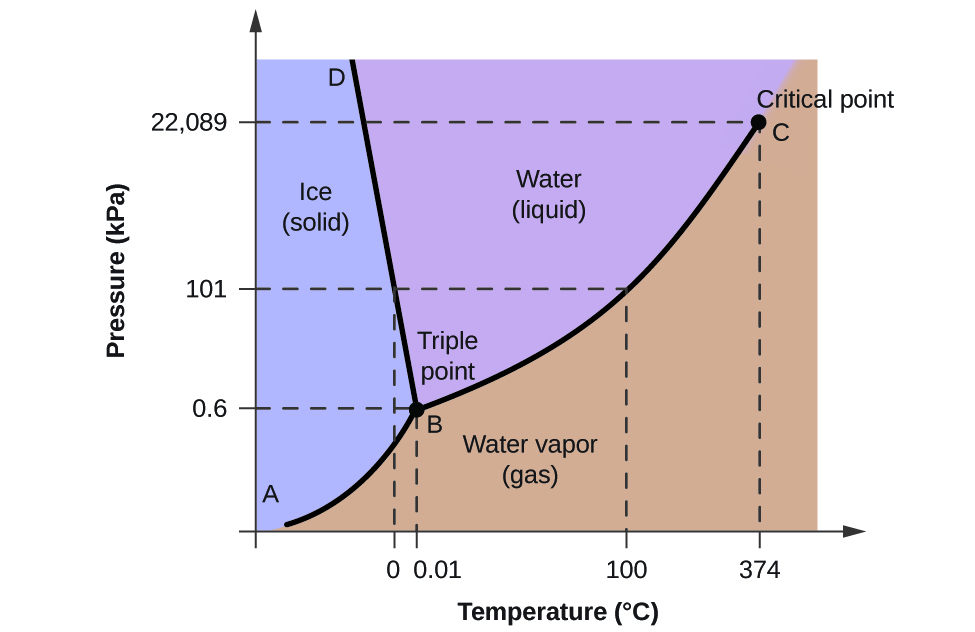
We kunnen het fasediagram gebruiken om de fysische toestand van een watermonster onder bepaalde druk- en temperatuuromstandigheden vast te stellen. Bijvoorbeeld, een druk van 50 kPa en een temperatuur van -10 °C komen overeen met het gebied in het diagram dat met “ijs” wordt aangeduid. Onder deze omstandigheden bestaat water alleen als vaste stof (ijs). Een druk van 50 kPa en een temperatuur van 50 °C komen overeen met het gebied “water” – hier bestaat water alleen als vloeistof. Bij 25 kPa en 200 °C bestaat water alleen in gasvormige toestand. Merk op dat in het H2O-fasendiagram de druk- en temperatuurassen niet op een constante schaal zijn getekend om een aantal belangrijke kenmerken te kunnen illustreren zoals hier beschreven.
De curve BC in figuur 2 is het diagram van dampspanning versus temperatuur zoals beschreven in de vorige module van dit hoofdstuk. Deze “vloeistof-damp”-kromme scheidt de vloeibare en gasvormige gebieden van het fasediagram en geeft het kookpunt voor water bij elke druk. Bijvoorbeeld, bij 1 atm is het kookpunt 100 °C. Merk op dat de vloeistof-dampkromme eindigt bij een temperatuur van 374 °C en een druk van 218 atm, wat aangeeft dat water boven deze temperatuur niet vloeibaar kan zijn, ongeacht de druk. De fysische eigenschappen van water onder deze omstandigheden houden het midden tussen die van de vloeibare en de gasvormige fase. Deze unieke toestand van de materie wordt een superkritische vloeistof genoemd, een onderwerp dat in het volgende deel van deze module zal worden beschreven.
De vaste stof-dampkromme, in figuur 2 aangeduid met AB, geeft de temperaturen en drukken aan waarbij ijs en waterdamp in evenwicht zijn. Deze temperatuur-drukparen komen overeen met de sublimatie- of neerslagpunten voor water. Als we zouden inzoomen op de vast-gaslijn in figuur 2, zouden we zien dat ijs een dampdruk heeft van ongeveer 0,20 kPa bij -10 °C. Als we dus een bevroren monster in een vacuüm plaatsen met een druk van minder dan 0,20 kPa, zal het ijs sublimeren. Dit is de basis voor het “vriesdroog”-proces dat vaak wordt gebruikt om levensmiddelen te conserveren, zoals het in figuur 3 afgebeelde ijs.

De vast-vloeibaarkromme met het label BD toont de temperaturen en drukken waarbij ijs en vloeibaar water in evenwicht zijn, wat overeenkomt met de smelt- en vriespunten voor water. Merk op dat deze curve een lichte negatieve helling vertoont (voor de duidelijkheid sterk overdreven), wat aangeeft dat het smeltpunt van water enigszins daalt naarmate de druk toeneemt. Water is in dit opzicht een ongewone stof, aangezien de meeste stoffen een stijging van het smeltpunt vertonen bij toenemende druk. Dit gedrag is gedeeltelijk verantwoordelijk voor de beweging van gletsjers, zoals die welke in figuur 4 wordt getoond. De bodem van een gletsjer ondervindt door zijn gewicht een immense druk die een deel van het ijs kan doen smelten, waardoor een laag vloeibaar water ontstaat waarop de gletsjer gemakkelijker kan glijden.

Het snijpunt van de drie curven is in figuur 2 aangeduid met B. Bij de druk en temperatuur die dit punt aangeeft, bestaan alle drie fasen van het water naast elkaar in evenwicht. Dit temperatuur-druk gegevenspaar wordt het tripelpunt genoemd. Bij drukken lager dan het tripelpunt kan water niet als vloeistof bestaan, ongeacht de temperatuur.
Voorbeeld 1
Bepaling van de toestand van water
Bepaal met behulp van het fasediagram voor water uit figuur 2 de toestand van water bij de volgende temperaturen en drukken:
(a) -10 °C en 50 kPa
(b) 25 °C en 90 kPa
(c) 50 °C en 40 kPa
(d) 80 °C en 5 kPa
(e) -10 °C en 0.3 kPa
(f) 50 °C en 0,3 kPa
Oplossing
Met behulp van het fasendiagram voor water kunnen we bepalen dat de toestand van water bij elke gegeven temperatuur en druk als volgt is: (a) vast; (b) vloeibaar; (c) vloeibaar; (d) gas; (e) vast; (f) gas.
Check Your Learning
Welke faseveranderingen kan water ondergaan als de temperatuur verandert, als de druk op 0,3 kPa wordt gehouden? Als de druk op 50 kPa wordt gehouden?
Antwoord:
Bij 0,3 kPa: \bij -58 °C. Bij 50 kPa: \text{s};{longrightarrow};\text{l} bij 0 °C, \text{l};{longrightarrow};\text{g} bij 78 °C
Beschouw het fasediagram voor koolstofdioxide in figuur 5 als een ander voorbeeld. De vast-vloeibaarkromme vertoont een positieve helling, wat erop wijst dat het smeltpunt van CO2 stijgt met de druk, zoals dat voor de meeste stoffen het geval is (water is een opmerkelijke uitzondering, zoals eerder beschreven). Merk op dat het tripelpunt ruim boven 1 atm ligt, wat aangeeft dat kooldioxide niet als vloeistof kan bestaan onder omgevingsdruk. In plaats daarvan leidt afkoeling van gasvormig kooldioxide bij 1 atm tot afzetting in vaste toestand. Evenzo smelt vast kooldioxide niet bij een druk van 1 atm, maar sublimeert het om gasvormig CO2 te vormen. Merk tenslotte op dat het kritieke punt voor kooldioxide wordt waargenomen bij een relatief bescheiden temperatuur en druk in vergelijking met water.
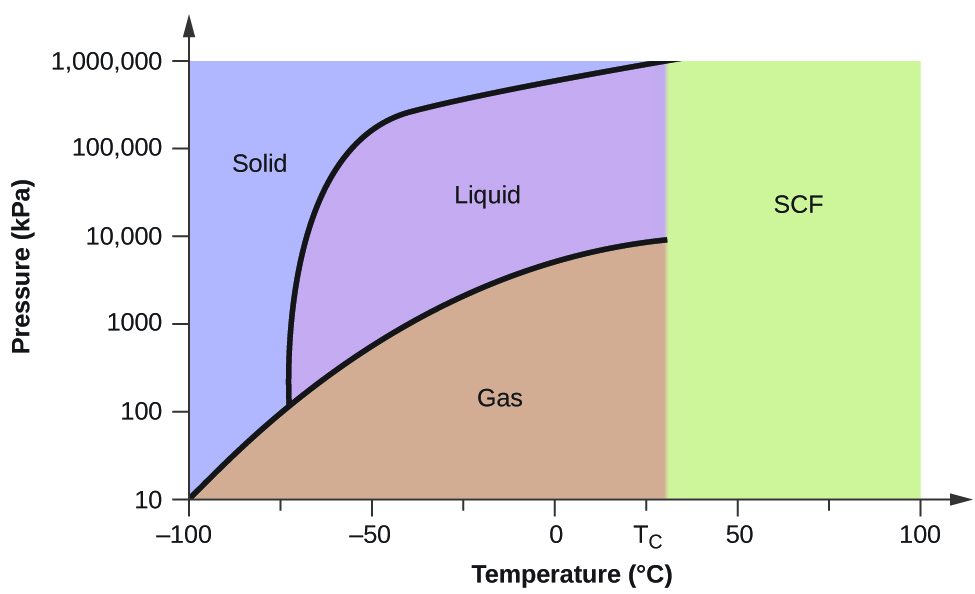
Voorbeeld 2
Bepaling van de toestand van kooldioxide
Bepaal met behulp van het in figuur 5 weergegeven fasediagram van kooldioxide de toestand van CO2 bij de volgende temperaturen en drukken:
(a) -30 °C en 2000 kPa
(b) -60 °C en 1000 kPa
(c) -60 °C en 100 kPa
(d) 20 °C en 1500 kPa
(e) 0 °C en 100 kPa
(f) 20 °C en 100 kPa
Oplossing
Met behulp van het gegeven fasediagram voor koolstofdioxide, kunnen we bepalen dat de toestand van CO2 bij elke gegeven temperatuur en druk als volgt is: (a) vloeibaar; (b) vast; (c) gas; (d) vloeibaar; (e) gas; (f) gas.
Check Your Learning
Bepaal de faseveranderingen die koolstofdioxide ondergaat wanneer de temperatuur wordt gevarieerd, waarbij de druk constant wordt gehouden op 1500 kPa? Bij 500 kPa? Bij welke temperatuur doen deze faseveranderingen zich ongeveer voor?
Antwoord:
bij 1500 kPa: \bij -45 °C, bij -10 °C; bij 500 kPa:
Als we een monster water in een afgesloten vat plaatsen bij 25 °C, de lucht verwijderen en het verdampings-condensatie-evenwicht laten ontstaan, houden we een mengsel over van vloeibaar water en waterdamp bij een druk van 0,03 atm. Een duidelijke grens tussen de dichtere vloeistof en het minder dichte gas is duidelijk waarneembaar. Naarmate de temperatuur toeneemt, neemt de druk van de waterdamp toe, zoals beschreven door de vloeistof-gas curve in het fasediagram voor water (figuur 2), en blijft er een twee-fasen evenwicht van vloeibare en gasvormige fasen over. Bij een temperatuur van 374 °C is de dampdruk gestegen tot 218 atm, en elke verdere stijging van de temperatuur leidt tot het verdwijnen van de grens tussen vloeibare en gasvormige fasen. Al het water in de container is nu aanwezig in één enkele fase waarvan de fysische eigenschappen het midden houden tussen die van de gasvormige en de vloeibare toestand. Deze fase van materie wordt een superkritische vloeistof genoemd, en de temperatuur en druk waarboven deze fase bestaat is het kritieke punt (figuur 6). Boven de kritische temperatuur kan een gas niet vloeibaar worden gemaakt, hoeveel druk er ook op wordt uitgeoefend. De druk die nodig is om een gas bij zijn kritische temperatuur vloeibaar te maken, wordt de kritische druk genoemd. De kritische temperatuur en de kritische druk van enkele veel voorkomende stoffen zijn gegeven in tabel 6.
| Stof | Critische temperatuur (K) | Critische druk (atm) |
|---|---|---|
| waterstof | 33.2 | 12.8 |
| stikstof | 126.0 | 33.5 |
| zuurstof | 154.3 | 49,7 |
| kooldioxide | 304,2 | 73,0 |
| ammoniak | 405,5 | 111,5 |
| zwaveldioxide | 430.3 | 77,7 |
| water | 647,1 | 217,7 |
| Tabel 6. | ||
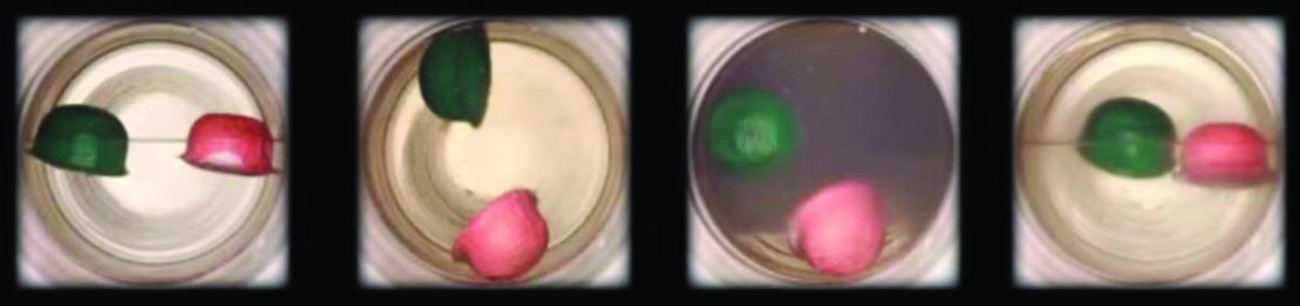

Zie de overgang van vloeibare naar superkritische vloeistof voor koolstofdioxide.
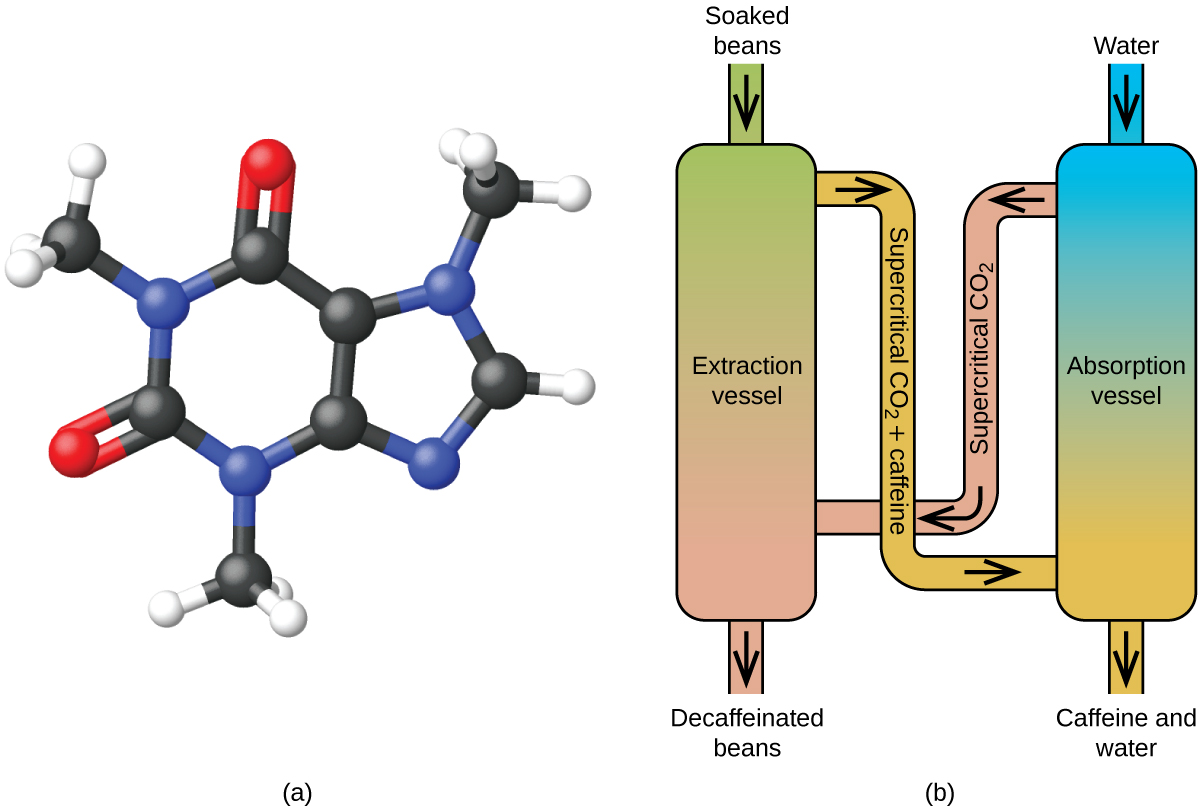
Zoals een gas zal een superkritische vloeistof uitzetten en een vat vullen, maar de dichtheid is veel groter dan de typische gasdichtheid, en ligt meestal dicht bij die van vloeistoffen. Net als vloeistoffen zijn deze vloeistoffen in staat om niet-vluchtige stoffen op te lossen. Zij vertonen echter vrijwel geen oppervlaktespanning en een zeer lage viscositeit, zodat zij effectiever door zeer kleine openingen in een vast mengsel kunnen dringen en oplosbare componenten kunnen verwijderen. Deze eigenschappen maken superkritische vloeistoffen uiterst nuttige oplosmiddelen voor een breed scala van toepassingen. Superkritisch kooldioxide is bijvoorbeeld een zeer populair oplosmiddel geworden in de levensmiddelenindustrie, dat wordt gebruikt om koffie cafeïnevrij te maken, vetten uit aardappelchips te verwijderen en smaak- en geurstoffen te extraheren uit citrusoliën. Het is niet giftig, relatief goedkoop, en wordt niet als vervuilend beschouwd. Na gebruik kan het CO2 gemakkelijk worden teruggewonnen door de druk te verlagen en het resulterende gas op te vangen.
Voorbeeld 3
De kritische temperatuur van kooldioxide
Als we op een koele dag (18 °C) met een kooldioxide-brandblusser schudden, kunnen we vloeibaar CO2 in de cilinder horen klotsen. Dezelfde cilinder lijkt echter geen vloeistof te bevatten op een warme zomerdag (35 °C). Verklaar deze waarnemingen.
Oplossing
Op de koele dag is de temperatuur van het CO2 lager dan de kritische temperatuur van CO2, 304 K of 31 °C (tabel 6), zodat er vloeibaar CO2 in de cilinder aanwezig is. Op de warme dag is de temperatuur van het CO2 hoger dan zijn kritische temperatuur van 31 °C. Boven deze temperatuur kan CO2 met geen enkele hoeveelheid druk vloeibaar worden gemaakt, zodat er geen vloeibaar CO2 in de brandblusser aanwezig is.
Check Your Learning
Ammoniak kan bij kamertemperatuur vloeibaar worden gemaakt door compressie; zuurstof kan onder deze omstandigheden niet vloeibaar worden gemaakt. Waarom gedragen de twee gassen zich verschillend?
Antwoord:
De kritische temperatuur van ammoniak is 405,5 K, dat is hoger dan kamertemperatuur. De kritische temperatuur van zuurstof ligt onder kamertemperatuur; zuurstof kan dus niet vloeibaar worden gemaakt bij kamertemperatuur.
Decafeïneren van koffie met behulp van superkritisch CO2
Koffie is ’s werelds op een na meest verhandelde grondstof, na alleen aardolie. Over de hele wereld houden mensen van het aroma en de smaak van koffie. Velen van ons zijn ook afhankelijk van één bestanddeel van koffie – cafeïne – om ons ’s morgens op gang te helpen of ’s middags alert te blijven. Maar laat op de dag kan het stimulerende effect van koffie u uit uw slaap houden, dus u kunt ervoor kiezen om ’s avonds cafeïnevrije koffie te drinken.
Sinds het begin van de 20e eeuw zijn er veel methoden gebruikt om koffie te cafeïneren. Alle hebben voor- en nadelen, en alle zijn afhankelijk van de fysische en chemische eigenschappen van cafeïne. Omdat cafeïne een enigszins polaire molecule is, lost het goed op in water, een polaire vloeistof. Maar omdat veel van de meer dan 400 bestanddelen die bijdragen aan de smaak en het aroma van koffie ook oplossen in H2O, kunnen bij het cafeïnevrij maken met heet water ook sommige van deze bestanddelen worden verwijderd, wat een nadelige invloed heeft op de geur en smaak van de cafeïnevrije koffie. Dichloormethaan (CH2Cl2) en ethylacetaat (CH3CO2C2H5) hebben een polariteit die vergelijkbaar is met die van cafeïne, en zijn daarom zeer effectieve oplosmiddelen voor cafeïne-extractie, maar beide verwijderen ook enkele smaak- en aromacomponenten, en hun gebruik vereist lange extractie- en reinigingstijden. Omdat beide oplosmiddelen giftig zijn, is bezorgdheid geuit over de gevolgen voor de gezondheid van achtergebleven oplosmiddelen in de cafeïnevrije koffie.
Superkritische vloeistofextractie met gebruikmaking van kooldioxide wordt nu op grote schaal toegepast als een effectievere en milieuvriendelijker methode voor cafeïnevrij maken (figuur 7). Bij temperaturen boven 304,2 K en drukken boven 7376 kPa is CO2 een superkritische vloeistof, met eigenschappen van zowel gas als vloeistof. Als een gas dringt het diep in de koffiebonen door; als een vloeistof lost het bepaalde stoffen effectief op. Superkritische kooldioxide-extractie van gestoomde koffiebonen verwijdert 97-99% van de cafeïne, maar laat de smaak- en aromabestanddelen van de koffie intact. Omdat CO2 onder standaardomstandigheden een gas is, kan het gemakkelijk uit de geëxtraheerde koffiebonen worden verwijderd, net als de terugwinning van de cafeïne uit het extract. De cafeïne die via dit proces uit koffiebonen wordt teruggewonnen, is een waardevol product dat vervolgens kan worden gebruikt als toevoeging aan andere voedingsmiddelen of geneesmiddelen.
Key Concepts and Summary
De temperatuur- en drukomstandigheden waarbij een stof in vaste, vloeibare en gasvormige toestand bestaat, worden samengevat in een fasediagram voor die stof. Fasendiagrammen zijn gecombineerde diagrammen van drie druk-temperatuur evenwichtskrommen: vast-vloeibaar, vloeibaar-gas, en vast-gas. Deze krommen geven de relaties weer tussen de fase-overgangstemperaturen en de drukken. Het snijpunt van de drie krommen is het tripelpunt van de stof – de temperatuur en druk waarbij alle drie fasen in evenwicht zijn. Bij drukken beneden het tripelpunt kan een stof niet in vloeibare toestand bestaan, ongeacht de temperatuur. Het eindpunt van de vloeistof-gas curve vertegenwoordigt het kritische punt van de stof, de druk en temperatuur waarboven een vloeibare fase niet kan bestaan.
Chemistry End of Chapter Exercises
- Van het fasediagram voor water (figuur 2), bepaal de toestand van water bij:
(a) 35 °C en 85 kPa
(b) -15 °C en 40 kPa
(c) -15 °C en 0.1 kPa
(d) 75 °C en 3 kPa
(e) 40 °C en 0,1 kPa
(f) 60 °C en 50 kPa
- Welke faseveranderingen vinden plaats wanneer water bij een constante temperatuur van 0,005 °C aan wisselende druk wordt blootgesteld? Bij 40 °C? Bij -40 °C?
- Drukkookpannen zorgen ervoor dat voedsel sneller gaar wordt, omdat de hogere druk in de snelkookpan de kooktemperatuur van water verhoogt. Een bepaalde snelkookpan heeft een veiligheidsventiel dat is ingesteld om stoom af te blazen als de druk hoger wordt dan 3,4 atm. Wat is bij benadering de maximale temperatuur die in deze snelkookpan kan worden bereikt? Leg uw redenering uit.
- Van het fasediagram voor koolstofdioxide in figuur 5, bepaal de toestand van CO2 bij:
(a) 20 °C en 1000 kPa
(b) 10 °C en 2000 kPa
(c) 10 °C en 100 kPa
(d) -40 °C en 500 kPa
(e) -80 °C en 1500 kPa
(f) -80 °C en 10 kPa
- Bepaal de faseveranderingen die kooldioxide ondergaat als de druk verandert als de temperatuur op -50 °C wordt gehouden? Als de temperatuur op -40 °C wordt gehouden? Bij 20 °C? (Zie het fasediagram in figuur 5.)
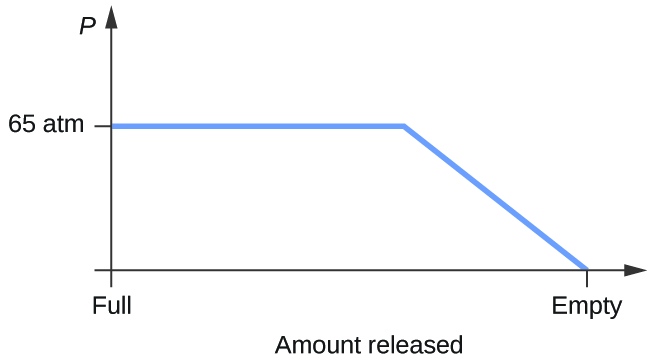
- Bedenk een cilinder met daarin een mengsel van vloeibaar kooldioxide in evenwicht met gasvormig kooldioxide bij een begindruk van 65 atm en een temperatuur van 20 °C. Schets een grafiek van de verandering in de cilinderdruk met de tijd als gasvormig kooldioxide vrijkomt bij constante temperatuur.
- Droog ijs, CO2(s), smelt niet bij atmosferische druk. Het sublimeert bij een temperatuur van -78 °C. Wat is de laagste druk waarbij CO2(s) zal smelten tot CO2(l)? Bij welke temperatuur zal dit ongeveer gebeuren? (Zie figuur 5 voor het fasediagram.)
- Als door een zware storm de elektriciteit uitvalt, kan het nodig zijn een waslijn te gebruiken om de was te drogen. In veel delen van het land bevriest de was in het holst van de winter snel als hij aan de lijn hangt. Als het niet sneeuwt, zullen ze dan toch drogen? Leg uw antwoord uit.
- Is het mogelijk om stikstof vloeibaar te maken bij kamertemperatuur (ongeveer 25 °C)? Is het mogelijk zwaveldioxide bij kamertemperatuur vloeibaar te maken? Leg uw antwoorden uit.
- Elementaire koolstof heeft één gasfase, één vloeibare fase, en twee verschillende vaste fasen, zoals weergegeven in het fasediagram:
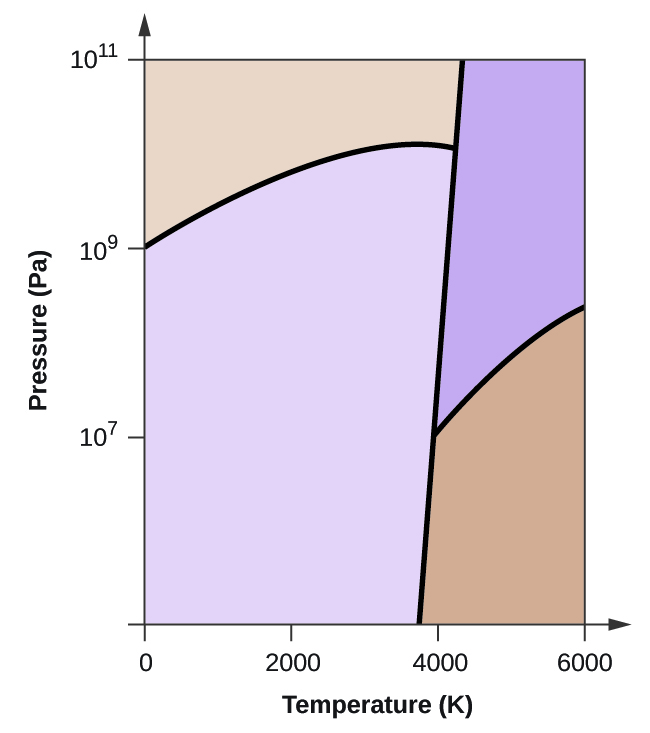
(a) Label op het fasediagram de gas- en vloeistofgebieden.
(b) Grafiet is de meest stabiele fase van koolstof onder normale omstandigheden. Geef op het fasediagram de grafietfase aan.
(c) Als grafiet onder normale omstandigheden wordt verhit tot 2500 K terwijl de druk wordt opgevoerd tot 1010 Pa, wordt het omgezet in diamant. Label de diamantfase.
(d) Omcirkel elk drievoudig punt op het fasediagram.
(e) In welke fase bestaat koolstof bij 5000 K en 108 Pa?
(f) Als de temperatuur van een koolstofmonster stijgt van 3000 K naar 5000 K bij een constante druk van 106 Pa, welke faseovergang treedt dan op, als die er is?
Glossary
kritisch punt temperatuur en druk waarboven een gas niet kan worden gecondenseerd tot een vloeistof fasediagram druk-temperatuurgrafiek die de omstandigheden samenvat waaronder de fasen van een stof kunnen bestaan superkritische vloeistof stof bij een temperatuur en druk hoger dan het kritisch punt; vertoont eigenschappen die het midden houden tussen die van de gasvormige en de vloeibare toestand drievoudig punt temperatuur en druk waarbij de dampfase, de vloeibare fase en de vaste fase van een stof in evenwicht zijn
Oplossingen
Antwoorden op scheikunde Oefeningen aan het einde van het hoofdstuk
2. Bij lage druk en 0,005 °C is het water een gas. Als de druk toeneemt tot 4,6 torr, wordt het water een vaste stof; als de druk nog meer toeneemt, wordt het een vloeistof. Bij 40 °C is water bij lage druk een damp; bij een druk hoger dan ongeveer 75 torr verandert het in een vloeistof. Bij -40 °C gaat water van een gas over in een vaste stof als de druk boven zeer lage waarden toeneemt.
4. (a) vloeibaar; (b) vast; (c) gas; (d) gas; (e) gas; (f) gas
8. Ja, ijs zal sublimeren, hoewel het enkele dagen kan duren. IJs heeft een kleine dampdruk, en sommige ijsmoleculen vormen gas en ontsnappen uit de ijskristallen. Naarmate de tijd verstrijkt, gaat steeds meer vaste stof over in gas, totdat de kleren uiteindelijk droog zijn.
10. (a)
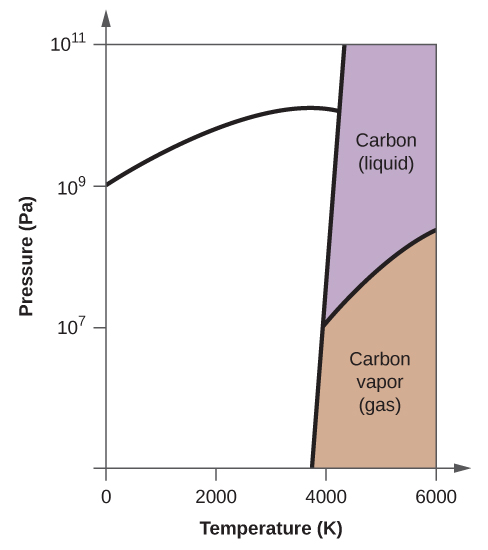
(b)
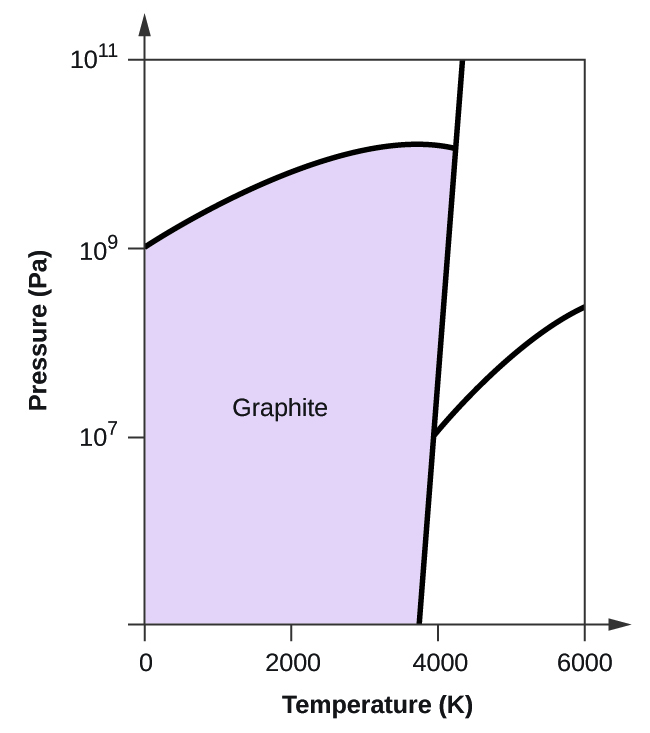
(c)
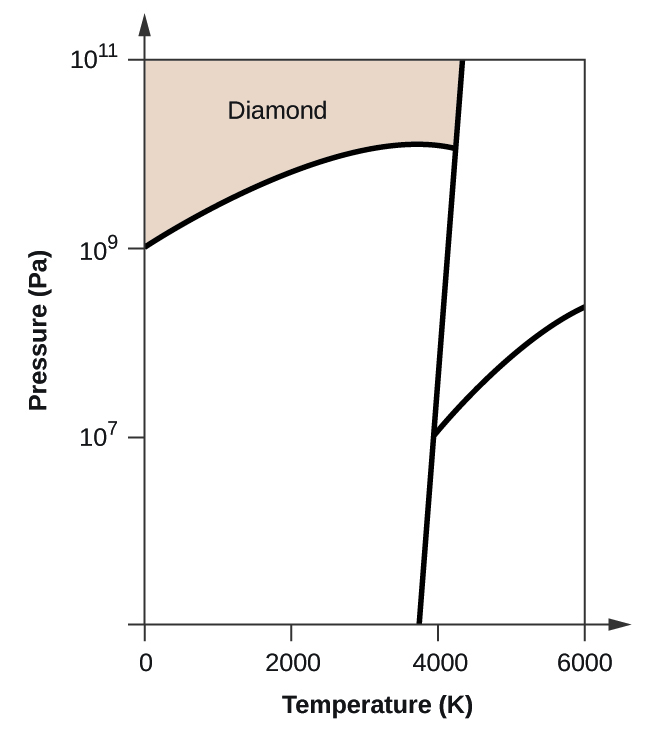
(d)
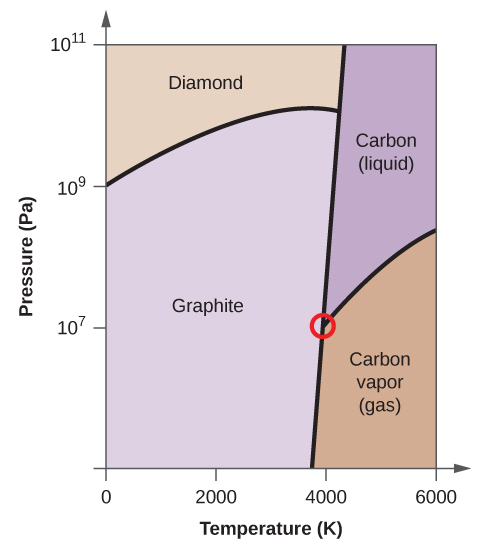
(e) vloeibare fase (f) sublimatie
