- Geschreven door Dr. Gabriel Scripcaru en Dr. Predrag Nikolic
- Patiëntgeschiedenis van de huid
- Squameus celcarcinoom (SCC)
- Klinische kenmerken
- Hoge-risico-kenmerken
- Basaalcelcarcinoom (BCC)
- Klinische kenmerken
- Hoge-risico kenmerken
- Stappen voorafgaand aan de verwijdering van SCC/BCC
- Bevestiging van de diagnose en aantekeningen op het histologieverslag
- Chirurgische excisie is de behandeling bij uitstek voor zowel SCC als BCC
- Aanvullende aspecten van de behandeling
- Nonchirurgische opties voor BCC
- Over de auteurs
- Lokale pathologen bij u in de buurt
Geschreven door Dr. Gabriel Scripcaru en Dr. Predrag Nikolic
Herkenning van de bepalende klinische kenmerken van verschillende typen huidkanker, en een juiste benadering van de biopsie, zijn essentieel voor hun diagnose en behandeling. Het belang van een tijdige diagnose kan niet genoeg worden benadrukt, met het oog op het bereiken van het best mogelijke resultaat en het minimaliseren van de complicaties.
In dit artikel worden plaveiselcelcarcinomen (SCC) en basaalcelcarcinomen (BCC) besproken, twee van de meest voorkomende vormen van kanker Basaalcelcarcinoom (BCC) in Australië.
Patiëntgeschiedenis van de huid
Het is belangrijk om de relevante huidgeschiedenis van de patiënt vast te leggen voordat een controle van de volledige lichaamshuid wordt uitgevoerd of voordat een bijzonder verontrustende nieuwe of veranderende laesie wordt onderzocht, waaronder:
- Familiegeschiedenis van huidkanker
- Vorige huidkankers
- Vorige excisies
- Opstelling
- Eerdere blootstelling aan UV-straling/zonnebrand inclusief gebruik van zonnebanken
- Frequentie van zonnebescherming
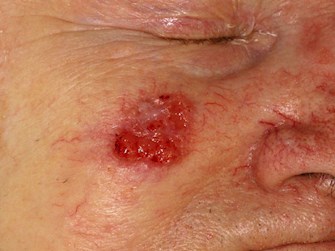
Squameus celcarcinoom (SCC)
 |
 |
| Clinische kenmerken | Histologie |
SCC is een kwaadaardige epitheliale tumor van keratinocyten die het vaakst ontstaat in door de zonbeschadigde huid. De overgrote meerderheid van de gevallen gaat gepaard met reeds bestaande actinische (zonne)keratose, plaveiselcelcarcinoom in situ, of beide. SCC’s vertegenwoordigen bijna 30% van de niet-melanome huidkankers.
Sommige SCC’s kunnen in verband worden gebracht met het humaan papillomavirus, chronische ontsteking of bestraling.
Histologisch gezien kunnen deze laesies goed gedifferentieerd, matig gedifferentieerd of slecht gedifferentieerd zijn. De differentiatiegraad is een essentiële marker voor progressie, risico van metastasering en prognose. Veel laesies vertonen gebieden met verschillende differentiatiegraden, maar het slechtste gebied moet in aanmerking worden genomen bij de uiteindelijke classificatie van de laesie. Het is het minst gedifferentieerde gebied dat uiteindelijk het beheer en de prognose bepaalt.
CC met focale basaloïde differentiatie of basosquameus carcinoom, wordt beschouwd als een matig gedifferentieerde laesie. Slecht gedifferentieerde SCC’s worden gekenmerkt door de afwezigheid van keratinisatie. SCC kunnen langzaam of snel groeien. In sommige gevallen kunnen significante klinische veranderingen binnen enkele maanden of zelfs weken duidelijk zijn.
Klinische kenmerken
- Dikke rode, schilferige vlek
- Langzaam of snel groeiende papel of nodule
- Niet-genezende ulcera of recidiverende bloedingen
- Mag pijnlijk zijn bij aanraking
- Mag gepigmenteerd zijn, wat de klinische verdenking van een gepigmenteerde laesie doet rijzen
Hoge-risico-kenmerken
- CCs die op het hoofd en in de hals worden gevonden, worden als hoog-risico beschouwd
- Voorkomen bij immuungecompromitteerde patiënten of op plaatsen van eerdere pathologie of trauma (bijv.b.v. brandwondenlittekens, bestralingslittekens, chronische ulcera/sinussen)
- De tumorgroei is snel, heeft een diameter >20mm, slecht gedefinieerde marges, veldverandering, gefixeerd op onderliggende structuren, gelokaliseerd boven belangrijke structuren of talrijke tumoren
- De patiënt ervaart symptomen die wijzen op perineurale invasie (b.v.b.v. tintelingen, pijn, paresthesie, formicatie, dysesthesie of gestoorde motoriek)
- Wanneer een biopsie is uitgevoerd, zijn de histopathologische kenmerken met een hoog risico: tumordikte >6 mm, invasie voorbij de subcutis, lymfovasculaire invasie of een hoog-risicopatroon van perineurale invasie, slecht gedifferentieerde tumoren en/of agressieve subtypes (b.v. infiltratief/desmoplastisch, sarcomatoid)
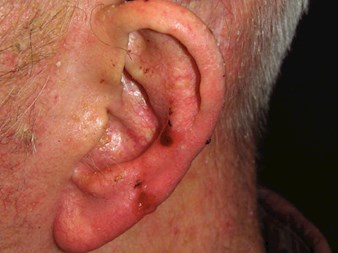
Basaalcelcarcinoom (BCC)
 |
 |
| Klinische kenmerken | Histologie |
Basaalcelcarcinoom (BCC) is een langzaamgroeiende, lokaal invasieve tumor, die meestal ontstaat in door de zon beschadigde huid vanuit de basale laag van de epidermis. De progressie van de ziekte neemt meestal de vorm aan van lokale weefselvernietiging, maar ontwikkelt zich zelden tot metastasen.
Histologisch gezien vertonen tumoren verschillende architecturale patronen: nodulair, oppervlakkig (wat een vroege fase van een nodulair patroon kan zijn), oppervlakkig multifocaal, infiltratief, micronodulair, morfoeïsch en metatypisch (d.w.z. squameuze of talgklier-differentiatie). Vaak wordt in dezelfde laesie een gemengd patroon waargenomen.
Patiëntgebonden factoren en de aanwezigheid van hoog-risicokenmerken bepalen het verloop van de behandeling. BCC is de meest voorkomende vorm van kanker bij de mens en vertegenwoordigt bijna 70% van de niet-melanome huidkankers.
Klinische kenmerken
- Paarlijke, doorschijnende papel, plaque of nodule
- Schilferige, droge plek, glanzend en bleek of helderroze van kleur
- Recidiverende bloeding of ulceratie
- Mag gepigmenteerd zijn, wat de klinische verdenking van een gepigmenteerde laesie doet rijzen
Hoge-risico kenmerken
- Hoofd en hals BCCs >10 mm worden beschouwd als hoog-risico tumoren
- Stam en extremiteiten BCCs >20 mm worden beschouwd als hoog-risico tumoren
- Angressieve histologische subtypes (bijv.b.v. micronodulair, infiltratief, morfoeïsch of basosquameus/metatypisch)
- Symptomen die wijzen op perineurale invasie (b.v. tintelingen, pijn, paresthesie, formicatie, dysesthesie verminderde motorische functie)
- Fixatie aan onderliggende structuren
- Genetische aanleg van de patiënt (b.v.b.v. Gorlin syndroom of Xeroderma pigmentosum) en gebruik van immunosuppressiva
Stappen voorafgaand aan de verwijdering van SCC/BCC
Vóór de excisie van de tumor moet de diameter worden gemeten en genoteerd. De meting van de tumor na excisie is niet nauwkeurig wegens weefselkrimp, die optreedt na excisie en tijdens het fixeren en verwerken van het specimen. Het histologisch onderzochte vlak van de doorsnede is relevant voor de afstand van de tumor tot de dichtstbijzijnde marge, en geeft dus niet noodzakelijk de grootste afmeting van de tumor weer.
Bevestiging van de diagnose en aantekeningen op het histologieverslag
In eerste instantie zijn de chirurgische opties een scheer- of ponsbiopsie voor diagnostische doeleinden, of volledige curatieve excisie zonder voorafgaande weefseldiagnose. Primaire curatieve excisie wordt gewoonlijk uitgevoerd in gevallen van hoge klinische verdenking of op verzoek van de patiënt.
Een ponsbiopsie heeft het voordeel dat ook het diepere aspect van de laesie wordt meegenomen en is gemakkelijk te verwerken met een lager risico op weefselartefacten.
Een scheerbiopsie kan, afhankelijk van de grootte, het architectuurpatroon beter onthullen en een groter deel van de laesie omvatten, maar omvat mogelijk niet het diepere aspect van de tumor en kan vatbaar zijn voor artefacten, als zij te dun is. Een dikkere scheerbeurt verdient de voorkeur om vouwen of fragmentatie te vermijden die de histologische beoordeling aanzienlijk zouden kunnen schaden. Een dikkere scheerbiopsie geeft ook een beter inzicht in de diepte en architectuur van de tumor. Het is belangrijk op te merken dat marges niet nauwkeurig kunnen worden beoordeeld in een pons- of scheerbiopsie, hoewel kleine laesies vaak volledig kunnen worden geëxcideerd met behulp van een van deze biopsietypes. De aanwezigheid van duidelijke randen kan in dergelijke gevallen in het histologische rapport worden vermeld, maar klinische correlatie is essentieel bij het bepalen van de noodzaak van verdere excisie.
Chirurgische excisie is de behandeling bij uitstek voor zowel SCC als BCC
Er is geen duidelijke, op bewijsmateriaal gebaseerde aanbeveling betreffende de minimale excisiemarge. Factoren zoals de risicostatus van de tumor, de chirurgische toegankelijkheid, de leeftijd van de patiënt, co-morbiditeiten en het vermogen tot wondgenezing moeten in overweging worden genomen bij de beslissing over de excisiemarge.
De klinische richtlijnen worden regelmatig meegedeeld en bijgewerkt in publicaties en op conferenties. Ongeacht de richtlijnen die door de clinicus worden gevolgd, is het belangrijk op te merken, dat als gevolg van weefselkrimp, de gerapporteerde histologische marges zo weinig kunnen zijn als de helft van de klinische marge gemeten op het moment van de operatie.
Het histologisch rapport geeft eerder de opruiming van de marges aan in de onderzochte vlakken van sectie dan dat het een absolute garantie van volledige excisie van de tumor vertegenwoordigt. Een nieuwe excisie, met dezelfde aanbevolen klinische marges als bij de oorspronkelijke excisie, moet worden geprobeerd wanneer betrokken marges worden gemeld.
In ongeveer 50% van de gevallen waarin een tumor aanwezig was aan de randen van de biopsie, of aan de marges van de excisie in het oorspronkelijke specimen, zal er geen verdere residuele tumor zijn in het opnieuw geëxcideerde specimen. Dit wordt verklaard door het feit dat een minimale hoeveelheid resttumor aan de rand van het initiële biopt is uitgeroeid door de immuunrespons en het regeneratieve proces dat leidt tot herstel en littekenvorming na de initiële chirurgische ingreep.
Aanvullende aspecten van de behandeling
In gevallen van SCC met perineurale invasie (PNI) of lymfovasculaire invasie (LVI) moet de patiënt worden doorverwezen naar een specialist (radiotherapeut of huidkankerafdeling van een ziekenhuis). In geval van LVI kan verder onderzoek met het oog op stadiëring aangewezen zijn, terwijl in geval van PNI een adjuvante therapie, zoals bestraling, kan worden toegepast.
Nonchirurgische opties voor BCC
In tegenstelling tot de gevallen van SCC’s bestaan er niet-chirurgische opties voor een subset van BCC’s. Cryotherapie, curettage en cauterisatie kunnen in combinatie worden toegepast bij patiënten die chirurgie niet verdragen. BCC presenteert zich zelden met LVI. Die gevallen moeten worden behandeld als een matig gedifferentieerd SCC met LVI. PNI komt vaker voor bij hoog-risico BCC. Bestralingstherapie kan in deze gevallen aangewezen zijn en de patiënt moet daarom worden doorverwezen naar een specialist (bestralingsoncoloog of huidkankereenheid van een ziekenhuis) voor verdere staging en behandeling. Oppervlakkig BCC kan worden behandeld met een niet-chirurgische benadering.
Andere behandelingsopties, voorbehouden voor oppervlakkig BCC, omvatten topische therapie zoals Imiquimod (Aldara) crème en topische fotodynamische therapie. Deze methoden zijn over het algemeen niet geschikt voor gevallen van BCC met hoog-risico kenmerken.
Over de auteurs

Dr Gabriel Scripcaru
Kwalificaties: FRCPA, MD
Lab: Clayton, Vic
Interessegebieden: Pathologie van de huid, hoofd, nek & Pathologie van weke delen
Specialisatie: Anatomische Pathologie
Telefoon: 1300 134 111
Email: [email protected]
Dr Gabriel Scripcaru studeerde geneeskunde aan de Universiteit voor Geneeskunde en Farmacie “Gr.T.Popa”, Iasi Roemenië. Na zijn afstuderen begon hij zijn opleiding in de neurochirurgie en werkte hij in Cluj, Roemenië en Newcastle, Engeland. Vervolgens werd hij lid van het Royal College of Surgeons of Edinburgh na het afleggen van de vereiste examens. Gabriel’s klinische ervaring voorafgaand aan de anatomische pathologie omvatte ook het werken in de spoedeisende geneeskunde, intensive care en chirurgie, zowel in Australië als in Schotland. Zijn opleiding in anatomische pathologie omvatte rotaties in het Royal Melbourne Hospital, The Royal Women’s en Royal Children’s Hospitals in Melbourne. Voordat hij bij Australian Clinical Labs kwam, werkte Dr. Scripcaru bij Southern Sun Pathology in Sydney, waar hij ervaring opdeed in dermatopathologie.

Dr Predrag Nikolic
Qualificaties: MBChB, MMedSci, PhD, FRCPA
Lab: Clayton, Vic
Belangrijke gebieden: Longpathologie, Borstpathologie, Huidpathologie, Moleculaire diagnostiek
Specialisatie: Anatomische Pathologie
Telefoon: 1300 134 111
Email: [email protected]
Dr Nikolic is een consultant histopatholoog met een interesse in longpathologie, borstpathologie, dermatopathologie en moleculaire diagnostiek. Dr. Nikolic voltooide zijn medische bacheloropleiding en zijn mastersopleiding (immunopathologie) in Belgrado, Servië en verhuisde vervolgens naar Nieuw-Zeeland waar hij promoveerde aan de Universiteit van Auckland, waar hij werkte aan purinerge signalering en geprogrammeerde celdood. Hij werkte als docent en als arts-assistent in Auckland en verhuisde vervolgens naar Australië voor een opleiding in de anatomische pathologie. Hij volgde zijn opleiding tot patholoog aan het Monash Medical Centre en bij Healthscope (nu Australian Clinical Labs) en behaalde zijn FRCPA in 2011. Na voltooiing van zijn opleiding bleef hij bij Australian Clinical Labs als consultant.
Lokale pathologen bij u in de buurt
 Dr Carl Bulliard
Dr Carl Bulliard
Qualificaties: BSc (Med), MBBS, Grad Dip Med (Clin Epid), FRCPA
Lab: Bella Vista, NSW
Belangstellinggebieden: Pathologie van de Huid, Hoofd & Hals en Oog, Opleiding Registrar
Specialisatie: Anatomische Pathologie
Telefoon: (02) 8887 9951
Email: [email protected]
 Dr Irani Dissanayake
Dr Irani Dissanayake
Kwalificaties: MBBS, MD, FRCPA
Lab: Luchthaven Adelaide, SA
Belangstellinggebieden: Gynaecologische Pathologie, Gastro-intestinale Pathologie
Specialisatie: Anatomische Pathologie
Telefoon: (08) 8205 5641
Email: [email protected]
 Dr Jenny Grew
Dr Jenny Grew
Kwalificaties: MBChB, FRCPA, AFRACMA
Lab: Subiaco, WA
Gebieden van interesse: Borst, Gastro-intestinale, Gynaecologische & Cutane Pathologie, Cytologie en Moleculaire Pathologie
Specialisatie: Anatomische Pathologie
Telefoon: 1300 367 674
Email: [email protected]
