- Écrit par le Dr Gabriel Scripcaru et le Dr Predrag Nikolic
- Histoire cutanée du patient
- Carcinome à cellules squameuses (CCS)
- Caractéristiques cliniques
- Caractéristiques à haut risque
- Carcinome basocellulaire (CBC)
- Caractéristiques cliniques
- Caractéristiques à haut risque
- Étapes préalables à l’ablation du SCC/BCC
- Confirmation du diagnostic et notes sur le rapport d’histologie
- L’excision chirurgicale est le traitement de choix pour le CSC et le CBC
- Aspects supplémentaires de la prise en charge
- Options non chirurgicales pour le BCC
- A propos des auteurs
- Pathologistes locaux près de chez vous
Écrit par le Dr Gabriel Scripcaru et le Dr Predrag Nikolic
La reconnaissance des caractéristiques cliniques déterminantes des différents types de cancer de la peau, et une approche appropriée de la biopsie, sont essentielles pour leur diagnostic et leur gestion. On ne saurait trop insister sur l’importance d’un diagnostic posé à temps, en vue d’obtenir le meilleur résultat possible et de minimiser les complications.
Cet article vise à discuter du carcinome épidermoïde (SCC) et du carcinome basocellulaire (BCC), deux des cancers les plus fréquents Carcinome basocellulaire (BCC) en Australie.
Histoire cutanée du patient
Il est important d’enregistrer l’histoire cutanée pertinente du patient avant de réaliser un examen cutané complet du corps ou d’examiner une lésion nouvelle ou changeante particulièrement préoccupante, notamment :
- Histoire familiale de cancers cutanés
- Cancers cutanés antérieurs
- Excisions antérieures
- Occupation
- Exposition antérieure aux UV/coups de soleil, y compris l’utilisation de solariums
- Fréquence de la protection solaire
.
Carcinome à cellules squameuses (CCS)
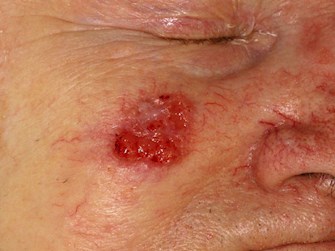 |
 |
| Caractéristiques cliniques | Histologie |
Le CCS est une tumeur épithéliale maligne des kératinocytes apparaissant le plus souvent sur une peau endommagée par le soleil.la peau endommagée par le soleil. La grande majorité des cas sont associés à une kératose actinique (solaire) préexistante, à un carcinome spinocellulaire in situ, ou aux deux. Les CSC représentent près de 30% des cancers cutanés non mélaniques.
Certains CSC peuvent être associés au papillomavirus humain, à une inflammation chronique ou à une radiothérapie.
D’un point de vue histologique, ces lésions peuvent être bien différenciées, moyennement différenciées ou peu différenciées. Le degré de différenciation est un marqueur essentiel de la progression, du risque de métastases et du pronostic. De nombreuses lésions présentent des zones de différents degrés de différenciation, cependant, la zone la plus défavorisée doit être prise en compte lors du classement final de la lésion. C’est la zone la moins différenciée qui détermine finalement la gestion et le pronostic.
Le CSC avec une différenciation basaloïde focale ou un carcinome basosquameux, est considéré comme une lésion modérément différenciée. Les CSC peu différenciés se caractérisent par l’absence de kératinisation. Les CSC peuvent avoir une croissance lente ou rapide. Dans certains cas, des changements cliniques significatifs peuvent être évidents en quelques mois, voire en quelques semaines.
Caractéristiques cliniques
- Tache rouge et squameuse épaissie
- Papule ou nodule à croissance lente ou rapide
- Ulcères ne cicatrisant pas ou saignant de façon récurrente
- Peut être sensible au toucher
- Peut être pigmenté, soulevant la suspicion clinique d’une lésion pigmentée
Caractéristiques à haut risque
- Les SCC trouvés sur la tête et le cou sont considérés comme à haut risque
- Occurrence chez les patients immunodéprimés ou sur des sites de pathologie ou de traumatisme antérieurs (par ex.ex. cicatrices de brûlure, cicatrices de radiation, ulcères/sinus chroniques)
- La croissance de la tumeur est rapide, a un diamètre >20mm, des marges mal définies, un changement de champ, fixé aux structures sous-jacentes, situé sur des structures importantes ou de nombreuses tumeurs
- Le patient présente des symptômes qui suggèrent une invasion périneurale (ex.picotement, douleur, paresthésie, formication, dysesthésie ou altération de la fonction motrice)
- Lorsqu’une biopsie a été réalisée, les caractéristiques histopathologiques à haut risque comprennent : épaisseur de la tumeur >6 mm, invasion au-delà du sous-cutané, invasion lymphovasculaire ou schéma à haut risque d’invasion périneurale, tumeurs peu différenciées et/ou sous-types agressifs (par ex. infiltrant/desmoplastique, sarcomatoïde)
Carcinome basocellulaire (CBC)
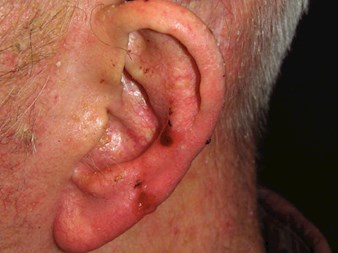 |
 |
| Caractéristiques cliniques | Histologie |
Le carcinome basocellulaire (CBC) est une tumeur invasive locale à croissance lente.tumeur invasive locale à croissance lente, survenant le plus souvent sur une peau endommagée par le soleil à partir de la couche basale de l’épiderme. La progression de la maladie prend généralement la forme d’une destruction locale des tissus, mais évolue rarement vers des métastases.
Histologiquement, les tumeurs présentent plusieurs modèles architecturaux : nodulaire, superficiel (qui peut représenter une phase précoce d’un modèle nodulaire), superficiel multifocal, infiltrant, micronodulaire, morphoïque et métatypique (c’est-à-dire une différenciation squameuse ou sébacée). Souvent, un modèle mixte est observé dans la même lésion.
Les facteurs liés au patient et la présence de caractéristiques à haut risque déterminent le cours du traitement. Le BCC est le cancer le plus fréquent chez l’homme et représente près de 70% des cancers cutanés non mélaniques.
Caractéristiques cliniques
- Papule, plaque ou nodule translucide
- Zone squameuse, sèche, brillante et de couleur pâle ou rose vif
- Saignement ou ulcération récurrents
- Peut être pigmenté, soulevant la suspicion clinique d’une lésion pigmentée
Caractéristiques à haut risque
- Les CBC de la tête et du cou >10 mm sont considérés comme des tumeurs à haut risque
- Les CBC du tronc et des extrémités >20 mm sont considérés comme des tumeurs à haut risque
- Sous-types histologiques agressifs (par ex.p. ex. micronodulaire, infiltrant, morphoïque ou basosquameux/métatypique)
- Symptômes indiquant une invasion périneurale (p. ex. fourmillement, douleur, paresthésie, formication, dysesthésie altération de la fonction motrice)
- Fixation aux structures sous-jacentes
- Disposition génétique du patient (p. ex.par exemple, syndrome de Gorlin ou Xeroderma pigmentosum) et utilisation d’immunosuppresseurs
Étapes préalables à l’ablation du SCC/BCC
Avant l’excision de la tumeur, le diamètre doit être mesuré et enregistré. La mesure de la tumeur après l’excision n’est pas précise en raison du rétrécissement des tissus, qui se produit après l’excision et pendant la fixation et le traitement du spécimen. Le plan de coupe examiné histologiquement est pertinent pour la distance de la tumeur à la marge la plus proche, par conséquent, il ne représente pas nécessairement la plus grande dimension de la tumeur.
Confirmation du diagnostic et notes sur le rapport d’histologie
En premier lieu, les options chirurgicales comprennent une biopsie par rasage ou punch à des fins de diagnostic, ou une excision curative complète sans diagnostic tissulaire préalable. L’excision curative primaire est généralement entreprise en cas de forte suspicion clinique ou à la demande du patient.
Une biopsie à l’emporte-pièce a l’avantage d’inclure l’aspect plus profond de la lésion et est facilement traitée avec un risque moindre d’artefacts tissulaires.
Selon sa taille, une biopsie par rasage peut mieux révéler le schéma architectural et elle peut inclure une plus grande partie de la lésion, cependant, elle peut ne pas inclure l’aspect plus profond de la tumeur et elle peut être sujette à des artefacts, si elle est trop fine. Il est préférable d’utiliser une lame plus épaisse pour éviter les plis ou les fragmentations qui pourraient nuire considérablement à l’évaluation histologique. Une biopsie par rasage plus épaisse donne également un meilleur aperçu de la profondeur et de l’architecture de la tumeur. Il est important de noter que les marges ne peuvent pas être évaluées avec précision dans une biopsie par poinçon ou par rasage, bien que de petites lésions puissent souvent être complètement excisées en utilisant l’un de ces types de biopsie. La présence de bords nets peut être mentionnée dans de tels cas dans le rapport histologique, cependant la corrélation clinique est essentielle pour déterminer la nécessité d’une excision supplémentaire.
L’excision chirurgicale est le traitement de choix pour le CSC et le CBC
Il n’y a pas de recommandation claire basée sur des preuves concernant la marge d’excision minimale. Des facteurs tels que le statut de risque de la tumeur, l’accessibilité chirurgicale, l’âge du patient, les comorbidités et la capacité de cicatrisation doivent être pris en compte pour décider de la marge d’excision.
Les directives cliniques sont régulièrement communiquées et mises à jour dans des publications et lors de conférences. Indépendamment des directives suivies par le clinicien, il est important de noter, qu’en raison du rétrécissement des tissus, les marges histologiques rapportées peuvent être aussi peu que la moitié de la marge clinique mesurée au moment de la chirurgie.
Le rapport histologique indique la clairance des marges dans les plans de section examinés plutôt que de représenter une garantie absolue d’excision complète de la tumeur. Une réexcision, avec les mêmes marges cliniques recommandées que pour l’excision initiale, doit être tentée lorsque des marges impliquées sont signalées.
Dans environ 50 % des cas où une tumeur était présente sur les bords de la biopsie, ou sur les marges de l’excision dans la pièce initiale, il n’y aura plus de tumeur résiduelle dans la pièce réexcisée. Ceci s’explique par le fait qu’une quantité minimale de tumeur résiduelle au niveau des bords de la biopsie initiale a été éradiquée par la réponse immunitaire et le processus régénératif conduisant à la réparation et à la cicatrisation suite à l’intervention chirurgicale initiale.
Aspects supplémentaires de la prise en charge
En cas de CSC avec invasion périneurale (PNI) ou invasion lymphovasculaire (LVI), le patient doit être adressé à un spécialiste (radio-oncologue ou unité hospitalière de cancer de la peau). En cas d’IVL, des examens complémentaires en vue d’une stadification peuvent être indiqués, tandis qu’en cas de PNI, une thérapie adjuvante, telle que la radiothérapie, peut être employée.
Options non chirurgicales pour le BCC
Contrairement aux cas de CSC, des options non chirurgicales existent pour un sous-ensemble de BCC. La cryothérapie, le curetage et le cautère peuvent être utilisés en combinaison chez les patients qui ne peuvent pas tolérer la chirurgie. Le BCC présente rarement une IVL. Ces cas doivent être traités comme un CSC modérément différencié avec une IVL. La PNI est plus fréquente dans les cas de BCC à haut risque. La radiothérapie peut être indiquée dans ces cas et le patient doit donc être adressé à un spécialiste (radio-oncologue ou unité hospitalière de cancérologie cutanée) pour une évaluation et une prise en charge plus poussées. Le BCC superficiel peut être pris en charge par une approche non chirurgicale.
Les autres options de traitement, réservées au BCC superficiel, comprennent la thérapie topique telle que la crème Imiquimod (Aldara) et la thérapie photodynamique topique. Ces méthodes ne sont généralement pas adaptées aux cas de BCC présentant des caractéristiques à haut risque.
A propos des auteurs

Dr Gabriel Scripcaru
Qualifications : FRCPA, MD
Lab : Clayton, Vic
Domaines d’intérêt : Pathologie de la peau, tête, cou &Pathologie des tissus mous
Spécialité : Anatomie pathologique
Téléphone : 1300 134 111
Email : [email protected]
Dr Gabriel Scripcaru a étudié la médecine à l’Université de Médecine et de Pharmacie « Gr.T.Popa », Iasi Roumanie. Après avoir obtenu son diplôme, il a commencé une formation en neurochirurgie en travaillant à Cluj, en Roumanie, et à Newcastle, en Angleterre. Il est ensuite devenu membre du Royal College of Surgeons of Edinburgh après avoir passé les examens requis. Avant de se consacrer à l’anatomie pathologique, Gabriel a également travaillé en médecine d’urgence, en soins intensifs et en chirurgie, en Australie et en Écosse. Sa formation en anatomie pathologique comprenait des stages au Royal Melbourne Hospital, au Royal Women’s Hospital et au Royal Children’s Hospital de Melbourne. Avant de rejoindre Australian Clinical Labs, le Dr Scripcaru a travaillé à Southern Sun Pathology à Sydney où il a acquis une expérience en dermatopathologie.

Dr Predrag Nikolic
Qualifications : MBChB, MMedSci, PhD, FRCPA
Lab : Clayton, Vic
Domaines d’intérêt : Pathologie pulmonaire, pathologie mammaire, pathologie cutanée, diagnostic moléculaire
Spécialité : Anatomie pathologique
Téléphone : 1300 134 111
Email : [email protected]
Le Dr Nikolic est un consultant histopathologiste avec un intérêt pour la pathologie pulmonaire, la pathologie mammaire, la dermatopathologie et les diagnostics moléculaires. Le Dr Nikolic a obtenu son diplôme de premier cycle en médecine et sa maîtrise (immunopathologie) à Belgrade, en Serbie, puis s’est installé en Nouvelle-Zélande où il a obtenu un doctorat à l’Université d’Auckland, travaillant sur la signalisation purinergique et la mort cellulaire programmée. Il a travaillé en tant qu’enseignant et médecin à Auckland, puis s’est rendu en Australie pour suivre une formation en anatomie pathologique. Il a suivi sa formation en pathologie au Monash Medical Centre et à Healthscope (aujourd’hui Australian Clinical Labs) et a obtenu son FRCPA en 2011. A la fin de sa formation, il est resté à Australian Clinical Labs en tant que consultant.
Pathologistes locaux près de chez vous
 Dr Carl Bulliard
Dr Carl Bulliard
Qualifications : BSc (Med), MBBS, Grad Dip Med (Clin Epid), FRCPA
Lab : Bella Vista, NSW
Domaines d’intérêt : Pathologie de la peau, de la tête &du cou et de l’oeil, formation des médecins généralistes
Spécialité : Anatomie pathologique
Téléphone : (02) 8887 9951
Email : [email protected]
 Dr Irani Dissanayake
Dr Irani Dissanayake
Qualifications : MBBS, MD, FRCPA
Lab : Adelaide Airport, SA
Domaines d’intérêt : Pathologie gynécologique, pathologie gastro-intestinale
Spécialité : Anatomie pathologique
Téléphone : (08) 8205 5641
Email : [email protected]
 Dr Jenny Grew
Dr Jenny Grew
Qualifications : MBChB, FRCPA, AFRACMA
Lab : Subiaco, WA
Domaines d’intérêt : Sein, Gastro-intestinal, Gynécologique &Pathologie cutanée, Cytologie et Pathologie Moléculaire
Spécialité : Anatomie pathologique
Téléphone : 1300 367 674
Email : [email protected]
