- Pisany przez dr Gabriela Scripcaru i dr Predrag Nikolic
- Historia skóry pacjenta
- Rak kolczystokomórkowy (SCC)
- Cechy kliniczne
- Cechy wysokiego ryzyka
- Rak podstawnokomórkowy (BCC)
- Cechy kliniczne
- Cechy wysokiego ryzyka
- Postępowanie przed usunięciem SCC/BCC
- Potwierdzenie diagnozy i uwagi w raporcie histologicznym
- Wycięcie chirurgiczne jest leczeniem z wyboru zarówno w przypadku SCC, jak i BCC
- Dodatkowe aspekty postępowania
- Opcje niechirurgiczne w przypadku BCC
- O autorach
- Lokalni patolodzy w pobliżu Ciebie
Pisany przez dr Gabriela Scripcaru i dr Predrag Nikolic
Rozpoznanie cech klinicznych definiujących różne typy raka skóry oraz odpowiednie podejście do biopsji są niezbędne do ich rozpoznania i zarządzania. Nie można przecenić znaczenia postawienia diagnozy w odpowiednim czasie, aby osiągnąć jak najlepszy wynik leczenia i zminimalizować powikłania.
Ten artykuł ma na celu omówienie raka kolczystokomórkowego (SCC) i raka podstawnokomórkowego (BCC), dwóch najczęstszych nowotworów raka podstawnokomórkowego (BCC) w Australii.
Historia skóry pacjenta
Ważne jest, aby przed wykonaniem badania skóry całego ciała lub zbadaniem szczególnie niepokojącej nowej lub zmieniającej się zmiany, zarejestrować odpowiednią historię skóry pacjenta, w tym:
- Historia rodzinna nowotworów skóry
- Poprzednie nowotwory skóry
- Poprzednie wycięcia
- Zawód
- Przebyta ekspozycja na promieniowanie UV/oparzenia słoneczne, w tym korzystanie z solariów
- Częstotliwość stosowania ochrony przeciwsłonecznej
.
Rak kolczystokomórkowy (SCC)
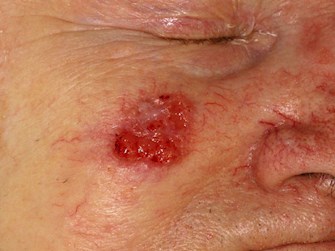 |
 |
| Cechy kliniczne | Histologia |
SCC jest złośliwym nowotworem nabłonkowym keratynocytów powstającym najczęściej w skórze uszkodzonej przez słońce.najczęściej w skórze uszkodzonej przez słońce. Zdecydowana większość przypadków związana jest z istniejącym wcześniej rogowaceniem słonecznym, rakiem kolczystokomórkowym in situ lub obiema tymi postaciami. SCC stanowią blisko 30% nieczerniakowych nowotworów skóry.
Niektóre SCC mogą być związane z wirusem brodawczaka ludzkiego, przewlekłym stanem zapalnym lub radioterapią.
Z histologicznego punktu widzenia zmiany te mogą być dobrze zróżnicowane, umiarkowanie zróżnicowane lub słabo zróżnicowane. Stopień zróżnicowania jest istotnym markerem progresji, ryzyka przerzutów i rokowania. Wiele zmian wykazuje obszary o różnym stopniu zróżnicowania, jednak przy ostatecznej klasyfikacji zmiany należy brać pod uwagę obszar najgorzej zróżnicowany. To właśnie najmniej zróżnicowany obszar ostatecznie determinuje postępowanie i rokowanie.
SCC z ogniskowym różnicowaniem bazaloidalnym lub rakiem podstawnokomórkowym jest uważany za zmianę umiarkowanie zróżnicowaną. Słabo zróżnicowane SCC charakteryzują się brakiem rogowacenia. SCC może być wolno lub szybko rosnący. W niektórych przypadkach istotne zmiany kliniczne mogą być widoczne w ciągu miesięcy, a nawet tygodni.
Cechy kliniczne
- Zgrubiała, czerwona, łuszcząca się plama
- Wolno lub szybko rosnąca grudka lub guzek
- Nie gojące się owrzodzenia lub nawracające krwawienia
- Może być tkliwy w dotyku
- Może być pigmentowany, budząc kliniczne podejrzenie zmiany barwnikowej
Cechy wysokiego ryzyka
- Raki występujące na głowie i szyi są uważane za zmiany wysokiego ryzyka
- Występowanie u pacjentów z immunosupresją lub w miejscach wcześniejszej patologii lub urazu (np.
- Gwałtowny wzrost guza, średnica >20 mm, słabo zdefiniowane marginesy, zmiana pola, przytwierdzenie do struktur leżących u podłoża, umiejscowienie nad ważnymi strukturami lub liczne guzy
- Pacjent doświadcza objawów sugerujących inwazję okołonerwową (np.np. mrowienie, ból, parestezje, mrowienie, dysestezja lub upośledzenie funkcji motorycznych)
- W przypadku wykonania biopsji, cechy histopatologiczne wysokiego ryzyka obejmują: grubość guza >6 mm, inwazja poza podskórną tkankę, inwazja limfowaskularna lub wzorzec wysokiego ryzyka inwazji okołonerwowej, słabo zróżnicowane guzy i/lub agresywne podtypy (np. naciekający/desmoplastyczny, sarkoidalny)
Rak podstawnokomórkowy (BCC)
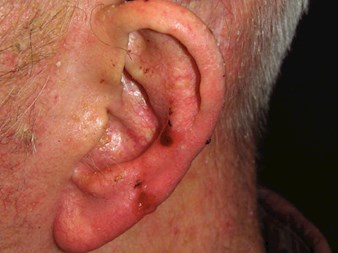 |
 |
| Cechy kliniczne | Histologia |
Rak podstawnokomórkowy (BCC) jest wolno rosnącym, miejscowo inwazyjnym nowotworem.rosnącym, miejscowo inwazyjnym nowotworem, powstający najczęściej w uszkodzonej przez słońce skórze z warstwy podstawnej naskórka. Progresja choroby zwykle przybiera postać miejscowego zniszczenia tkanek, ale rzadko dochodzi do przerzutów.
Histologicznie, guzy wykazują kilka wzorów architektonicznych: guzkowy, powierzchowny (który może reprezentować wczesną fazę wzoru guzkowego), powierzchowny wieloogniskowy, naciekowy, mikronaczynisty, morfotyczny i metatypowy (tj. zróżnicowanie płaskie lub łojowe). Często w tej samej zmianie obserwuje się wzór mieszany.
Czynniki związane z pacjentem oraz obecność cech wysokiego ryzyka determinują przebieg leczenia. BCC jest najczęstszym nowotworem u ludzi i stanowi prawie 70% nieczerniakowych nowotworów skóry.
Cechy kliniczne
- Łzawe, przeświecające grudki, blaszki lub guzki
- Łuskowaty, suchy obszar, błyszczący i o bladym lub jasnoróżowym zabarwieniu
- Powtarzające się krwawienie lub owrzodzenie
- Może być pigmentowany, budząc kliniczne podejrzenie zmiany barwnikowej
Cechy wysokiego ryzyka
- Choroby BCC głowy i szyi >10 mm są uważane za nowotwory wysokiego ryzyka
- Choroby BCC tułowia i kończyn >20 mm są uważane za nowotwory wysokiego ryzyka
- Agresywne podtypy histologiczne (np.micronodular, infiltrative, morphoeic or basosquamous/metatypical)
- Objawy wskazujące na inwazję okołonerwową (np. mrowienie, ból, parestezja, mrówczenie, dysestezja upośledzenie funkcji motorycznych)
- Utrwalenie na strukturach leżących u podłoża
- Dyspozycja genetyczna pacjenta (np.zespół Gorlina lub Xeroderma pigmentosum) i stosowanie leków immunosupresyjnych
Postępowanie przed usunięciem SCC/BCC
Przed wycięciem guza należy zmierzyć i zapisać jego średnicę. Pomiar guza po wycięciu nie jest dokładny ze względu na kurczenie się tkanki, które występuje po wycięciu oraz podczas utrwalania i obróbki materiału. Płaszczyzna przekroju badana histologicznie jest istotna dla odległości od guza do najbliższego marginesu, dlatego nie musi reprezentować największego wymiaru guza.
Potwierdzenie diagnozy i uwagi w raporcie histologicznym
W pierwszej kolejności, opcje chirurgiczne obejmują biopsję goleniową lub punkcyjną dla celów diagnostycznych lub całkowite wycięcie lecznicze bez wcześniejszej diagnostyki tkanek. Pierwotne wycięcie lecznicze jest zwykle wykonywane w przypadkach dużego klinicznego podejrzenia lub na prośbę pacjenta.
Biopsja punkcyjna ma tę zaletę, że obejmuje głębsze partie zmiany i jest łatwa do wykonania przy mniejszym ryzyku artefaktów tkankowych.
Zależnie od wielkości, biopsja shave może lepiej ujawnić wzór architektoniczny i może obejmować większą część zmiany, jednak może nie obejmować głębszego aspektu guza i może być podatna na artefakty, jeśli jest zbyt cienka. Preferowana jest grubsza strużyna, aby uniknąć pofałdowania lub fragmentacji, które mogłyby znacznie pogorszyć ocenę histologiczną. Biopsja z grubszego skrawka daje również lepszy wgląd w głębokość i architekturę guza. Ważne jest, aby pamiętać, że marginesy nie mogą być dokładnie ocenione w biopsji punch lub shave, chociaż małe zmiany mogą być często całkowicie wycięte przy użyciu jednego z tych typów biopsji. W takich przypadkach obecność wyraźnych brzegów może być wspomniana w raporcie histologicznym, jednak korelacja kliniczna jest niezbędna do określenia potrzeby dalszego wycięcia.
Wycięcie chirurgiczne jest leczeniem z wyboru zarówno w przypadku SCC, jak i BCC
Nie ma jednoznacznych, opartych na dowodach naukowych zaleceń dotyczących minimalnego marginesu wycięcia. Czynniki takie jak status ryzyka nowotworu, dostępność chirurgiczna, wiek pacjenta, choroby współistniejące i zdolność gojenia się ran powinny być brane pod uwagę przy podejmowaniu decyzji o marginesie wycięcia.
Wytyczne kliniczne są regularnie przekazywane i aktualizowane w publikacjach i na konferencjach. Niezależnie od wytycznych, którymi kieruje się klinicysta, należy pamiętać, że ze względu na kurczliwość tkanek, raportowane marginesy histologiczne mogą stanowić zaledwie połowę marginesu klinicznego zmierzonego w czasie operacji.
Raport histologiczny wskazuje raczej na oczyszczenie marginesów w badanych płaszczyznach przekroju, niż stanowi absolutną gwarancję całkowitego wycięcia guza. Ponowne wycięcie, z takimi samymi zalecanymi marginesami klinicznymi, jak w przypadku pierwotnego wycięcia, powinno być podjęte, gdy zgłaszane są zaangażowane marginesy.
W około 50% przypadków, w których guz był obecny na krawędziach biopsji lub na marginesach wycięcia w pierwotnej próbce, nie będzie dalszego resztkowego guza w ponownie wyciętej próbce. Wynika to z faktu, że minimalna ilość guza resztkowego na brzegach pierwotnej biopsji została usunięta przez odpowiedź immunologiczną i proces regeneracji prowadzący do naprawy i bliznowacenia po pierwotnej interwencji chirurgicznej.
Dodatkowe aspekty postępowania
W przypadku SCC z inwazją okołonerwową (PNI) lub limfowaskularną (LVI), pacjent powinien zostać skierowany do specjalisty (onkologa radiacyjnego lub szpitalnego oddziału zajmującego się nowotworami skóry). W przypadku LVI mogą być wskazane dalsze badania w celu ustalenia stopnia zaawansowania, natomiast w przypadku PNI można zastosować leczenie adiuwantowe, takie jak radioterapia.
Opcje niechirurgiczne w przypadku BCC
Podobnie jak w przypadku SCC, opcje niechirurgiczne istnieją dla podgrupy BCC. Krioterapia, kiretaż i kauteryzacja mogą być stosowane w połączeniu u pacjentów, którzy nie tolerują zabiegu chirurgicznego. W przypadku BCC rzadko występuje LVI. Takie przypadki powinny być traktowane jak średnio zróżnicowane SCC z LVI. PNI jest częstszym zjawiskiem w BCC wysokiego ryzyka. W takich przypadkach wskazana może być radioterapia, dlatego pacjent powinien zostać skierowany do specjalisty (onkologa radioterapeutycznego lub szpitalnego oddziału leczenia nowotworów skóry) w celu ustalenia rozpoznania i dalszego postępowania. Inne opcje leczenia, zarezerwowane dla powierzchownych BCC, obejmują terapię miejscową, taką jak krem Imiquimod (Aldara) oraz miejscową terapię fotodynamiczną. Metody te generalnie nie są odpowiednie dla przypadków BCC z cechami wysokiego ryzyka.
O autorach

Dr Gabriel Scripcaru
Kwalifikacje: FRCPA, MD
Lab: Clayton, Vic
Obszary zainteresowań: Patologia Skóry, Głowy, Szyi & Patologia Tkanek Miękkich
Specjalność: Patologia Anatomiczna
Phone: 1300 134 111
Email: [email protected]
Dr Gabriel Scripcaru studiował medycynę na University of Medicine and Pharmacy „Gr.T.Popa”, Iasi Romania. Po ukończeniu studiów rozpoczął szkolenie w zakresie neurochirurgii, pracując w Cluj, Rumunia i Newcastle, Anglia. Po zdaniu wymaganych egzaminów został członkiem Royal College of Surgeons of Edinburgh. Doświadczenie kliniczne Gabriela przed rozpoczęciem pracy w patologii anatomicznej obejmowało również pracę w medycynie ratunkowej, intensywnej terapii i chirurgii zarówno w Australii, jak i Szkocji. Jego szkolenie w zakresie patologii anatomicznej obejmowało staże w Królewskim Szpitalu Melbourne, Królewskim Szpitalu Kobiecym i Królewskim Szpitalu Dziecięcym w Melbourne. Przed dołączeniem do Australian Clinical Labs, Dr Scripcaru pracował w Southern Sun Pathology w Sydney, gdzie zdobył doświadczenie w dermatopatologii.

Dr Predrag Nikolic
Kwalifikacje: MBChB, MMedSci, PhD, FRCPA
Lab: Clayton, Vic
Obszary zainteresowań: Patologia Płuc, Patologia Piersi, Patologia Skóry, Diagnostyka Molekularna
Specjalność: Patologia Anatomiczna
Phone: 1300 134 111
Email: [email protected]
Dr Nikolic jest konsultantem histopatologiem interesującym się patologią płuc, patologią piersi, dermatopatologią i diagnostyką molekularną. Dr Nikolic ukończył studia licencjackie i magisterskie (immunopatologia) w Belgradzie, w Serbii, a następnie przeniósł się do Nowej Zelandii, gdzie uzyskał stopień doktora na Uniwersytecie w Auckland, pracując nad sygnalizacją purynergiczną i programowaną śmiercią komórki. Pracował jako wykładowca i oficer medyczny w Auckland, a następnie przeniósł się do Australii, aby szkolić się w zakresie patologii anatomicznej. Odbył szkolenie w zakresie patologii w Monash Medical Centre oraz w Healthscope (obecnie Australian Clinical Labs) i uzyskał tytuł FRCPA w 2011 roku. Po ukończeniu szkolenia pozostał w Australian Clinical Labs jako konsultant.
Lokalni patolodzy w pobliżu Ciebie
 Dr Carl Bulliard
Dr Carl Bulliard
Kwalifikacje: BSc (Med), MBBS, Grad Dip Med (Clin Epid), FRCPA
Lab: Bella Vista, NSW
Obszary zainteresowań: Patologia Skóry, Głowy & Szyi i Oczu, Registrar Training
Specjalność: Patologia Anatomiczna
Phone: (02) 8887 9951
Email: [email protected]
 Dr Irani Dissanayake
Dr Irani Dissanayake
Kwalifikacje: MBBS, MD, FRCPA
Lab: Adelaide Airport, SA
Obszary zainteresowań: Patologia ginekologiczna, Patologia przewodu pokarmowego
Specjalność: Anatomical Pathology
Phone: (08) 8205 5641
Email: [email protected]
 Dr Jenny Grew
Dr Jenny Grew
Kwalifikacje: MBChB, FRCPA, AFRACMA
Lab: Subiaco, WA
Obszary zainteresowań: Patologia piersi, przewodu pokarmowego, ginekologiczna & Patologia skórna, cytologia i patologia molekularna
Specjalność: Anatomical Pathology
Phone: 1300 367 674
Email: [email protected]
.
