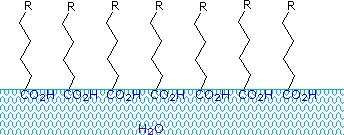
Acizii și sărurile carboxilice cu lanțuri alchilice mai lungi de opt atomi de carbon prezintă un comportament neobișnuit în apă datorită prezenței în aceeași moleculă a unor regiuni hidrofile (CO2) și hidrofobe (alchil). Astfel de molecule sunt denumite amfifile (Gk. amphi = ambele) sau amfifatice. Acizii grași compuși din zece sau mai mulți atomi de carbon sunt aproape insolubili în apă și, din cauza densității lor mai mici, plutesc la suprafață atunci când sunt amestecați cu apă. Spre deosebire de parafină sau de alți alcani, care au tendința de a se bălăci la suprafața apei, acești acizi grași se împrăștie uniform pe o suprafață extinsă de apă, formând în cele din urmă un strat monomolecular în care grupările carboxilice polare sunt legate de hidrogen la interfața cu apa, iar lanțurile de hidrocarburi sunt aliniate între ele departe de apă. Acest comportament este ilustrat în diagrama din dreapta. Substanțele care se acumulează la suprafața apei și modifică proprietățile de suprafață se numesc agenți tensioactivi.
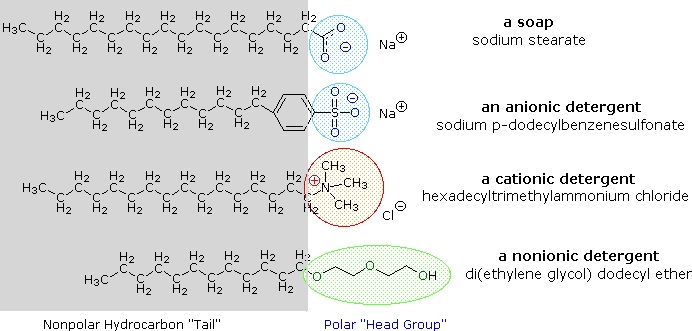
Sărurile de metal alcalin ale acizilor grași sunt mai solubile în apă decât acizii înșiși, iar caracterul amfifil al acestor substanțe le face, de asemenea, agenți tensioactivi puternici. Cele mai frecvente exemple de astfel de compuși sunt săpunurile și detergenții, dintre care patru sunt prezentate mai jos. Rețineți că fiecare dintre aceste molecule are un lanț hidrocarbonat nepolar, „coada”, și un „grup de cap” polar (adesea ionic). Utilizarea acestor compuși ca agenți de curățare este facilitată de caracterul lor tensioactiv, care scade tensiunea superficială a apei, permițându-i acesteia să pătrundă și să ude o varietate de materiale.
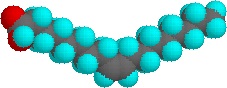
Cantități foarte mici din acești agenți tensioactivi se dizolvă în apă pentru a da o dispersie aleatorie de molecule de solut. Cu toate acestea, atunci când concentrația este crescută, apare o schimbare interesantă. Moleculele de agenți tensioactivi se asamblează în mod reversibil în agregate polimeleculare numite micle. Prin reunirea lanțurilor hidrofobe în centrul micellei, perturbarea structurii cu legături de hidrogen a apei lichide este redusă la minimum, iar grupările polare de cap se extind în apa înconjurătoare, unde participă la legături de hidrogen. Aceste micelii au adesea o formă sferică, dar pot lua, de asemenea, forme cilindrice și ramificate, așa cum este ilustrat în dreapta. Aici, grupul de cap polar este desemnat de un cerc albastru, iar coada nepolară este o linie neagră în zig-zag.
Cel mai vechi agent de curățare amfifilic cunoscut de oameni este săpunul. Săpunul este fabricat prin hidroliza (saponificarea) catalizată de baze a grăsimilor animale. Înainte ca hidroxidul de sodiu să fie disponibil în comerț, se folosea o soluție clocotită de carbonat de potasiu lichefiat din cenușa de lemn. Săpunurile moi de potasiu erau apoi transformate în săpunuri de sodiu, mai dure, prin spălare cu soluție de sare. Importanța săpunului pentru civilizația umană este documentată de istorie, dar au fost recunoscute unele probleme asociate cu utilizarea sa. Una dintre acestea este cauzată de aciditatea slabă (pKa cca. 4,9) a acizilor grași. Soluțiile de săpunuri din metale alcaline sunt ușor alcaline (pH 8-9) din cauza hidrolizei. Dacă pH-ul unei soluții de săpun este coborât de contaminanți acizi, acizii grași insolubili precipită și formează o spumă. O a doua problemă este cauzată de prezența sărurilor de calciu și magneziu în alimentarea cu apă (apă dură). Acești cationi divalenți provoacă agregarea micelilor, care se depun apoi sub forma unei spume murdare.
Aceste probleme au fost atenuate prin dezvoltarea unor amfifile sintetice numite detergenți (sau sindet). Prin utilizarea unui acid mult mai puternic pentru grupa capului polar, soluțiile de apă ale amfifilei sunt mai puțin sensibile la schimbările de pH. De asemenea, funcțiile de sulfonat utilizate pentru aproape toți detergenții anionici conferă o mai mare solubilitate micelilor care încorporează cationii alcalino-pământoși care se găsesc în apa dură. Variațiile pe tema amfifilului au dus la dezvoltarea altor clase, cum ar fi detergenții cationici și neionici prezentați mai sus. Detergenții cationici prezintă adesea proprietăți germicide, iar capacitatea lor de a modifica pH-ul suprafeței i-a făcut utili ca balsamuri pentru țesături și pentru păr. Aceste „unelte” chimice versatile au transformat dramatic piețele produselor de curățenie de uz casnic și de îngrijire personală în ultimii cincizeci de ani.
Contribuitori
-
William Reusch, profesor emerit (Michigan State U.), Virtual Textbook of Organic Chemistry
.
