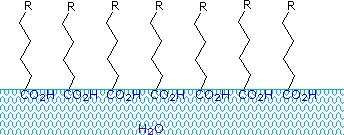
炭素数8以上のアルキル鎖を持つカルボン酸および塩は、同一分子内に親水性(二酸化炭素)と疎水性(アルキル)の両方の領域があるため、水中で異常な挙動を示します。 このような分子を両親媒性(Gk. amphi = 両方)または両親媒性と呼ぶ。 10個以上の炭素原子からなる脂肪酸は、水にほとんど溶けず、密度が低いため、水と混ぜると表面に浮いてくる。 パラフィンなどのアルカンは水面に水たまりを作るが、脂肪酸は水面に均一に広がり、最終的には水との界面で極性カルボキシル基が水素結合し、炭化水素鎖が水から離れて整列した単分子膜を形成する。 この挙動を右図に示す。 水面に集積して表面の性質を変える物質を界面活性剤といいます。
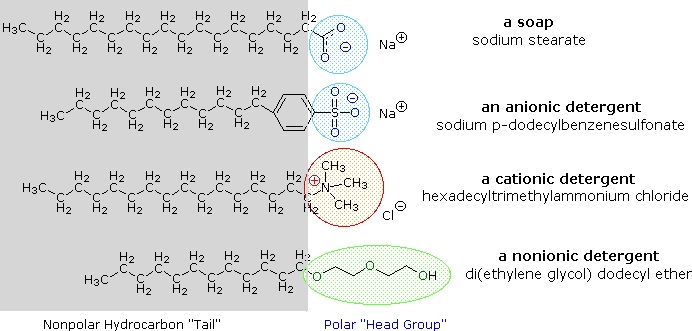
脂肪酸のアルカリ金属塩は酸そのものよりも水に溶けやすく、また両親媒性であることから強い界面活性剤になります。 このような化合物の最も一般的な例は石鹸や洗剤であり、そのうちの4つを以下に示す。 これらの分子はそれぞれ、非極性の炭化水素鎖である「尾部」と、極性(多くの場合イオン性)の「頭部基」を持っていることに注意されたい。 このような化合物の洗浄剤としての使用は、水の表面張力を低下させる界面活性剤の特性によって促進され、さまざまな材料に浸透して濡らすことができる。
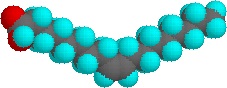
非常に少量のこれらの界面活性剤は水に溶解して、溶質分子のランダムな分散を与える。 しかし、濃度を上げると興味深い変化が起こる。 界面活性剤分子は可逆的に集合し、ミセルと呼ばれる高分子集合体を形成する。 ミセルの中心に疎水性鎖を集めることで、液体の水素結合構造の崩壊を最小限に抑え、極性頭部基が周囲の水中に伸びて水素結合に参加するのである。 このミセルは球状であることが多いが、右図のように円柱状や枝分かれした形状をしていることもある。 極性頭部は青丸で、非極性尾部はジグザグの黒線で示されている。
人類に知られる最も古い両親媒性の洗浄剤は石鹸である。 石けんは、動物性脂肪の塩基触媒による加水分解(けん化)により製造される。 水酸化ナトリウムが市販される以前は、木灰から溶出した炭酸カリウムの煮汁が使われていた。 軟らかいカリウム石鹸は、塩水で洗うことにより、硬いナトリウム石鹸に変化した。 石鹸が人類の文明にとって重要であったことは歴史に刻まれているが、その使用に伴ういくつかの問題点が認識されている。 そのひとつは、脂肪酸の弱酸性(pKa約4.9)に起因するものである。 アルカリ金属石鹸の溶液は、加水分解により弱アルカリ性(pH8~9)である。 酸性の汚染物質によって石鹸溶液のpHが低下すると、不溶性の脂肪酸が沈殿してスカムが形成される。 第二の問題は、水道水に含まれるカルシウム塩やマグネシウム塩(硬水)の存在によって引き起こされるものです。
これらの問題は、洗剤(またはシンデット)と呼ばれる合成両親媒性物質の開発によって軽減された。 極性頭部基にかなり強い酸を用いることで、両親媒性分子の水溶液はpHの変化にあまり敏感でなくなる。 また、陰イオン界面活性剤のほとんどに使われているスルホン酸塩の機能は、硬水に含まれるアルカリ土類陽イオンを取り込んだミセルに大きな溶解性を与える。 両親媒性というテーマから、カチオン系やノニオン系の洗浄剤も開発された。 カチオン洗剤は殺菌効果があり、また表面のpHを変化させることができるため、柔軟剤やヘアコンディショナーとして有用である。 これらの多用途な化学的「道具」は、過去50年間に家庭用およびパーソナルケア用の洗浄剤市場を劇的に変化させました。
寄稿
-
William Reusch、名誉教授(Michigan State U.) Virtual Textbook of Organic Chemistry
