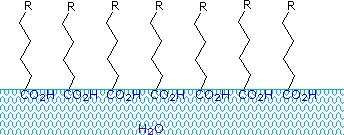
Karboxylové kyseliny a soli s alkylovými řetězci delšími než osm uhlíků vykazují ve vodě neobvyklé chování v důsledku přítomnosti hydrofilních (CO2) i hydrofobních (alkylových) oblastí v jedné molekule. Takové molekuly se označují jako amfifilní (gk. amphi = obojí) nebo amfifatické. Mastné kyseliny tvořené deseti a více atomy uhlíku jsou ve vodě téměř nerozpustné a kvůli své nižší hustotě plavou na hladině při smíchání s vodou. Na rozdíl od parafínu nebo jiných alkanů, které mají tendenci loužit se na povrchu vody, se tyto mastné kyseliny rovnoměrně rozprostírají po rozšířeném povrchu vody a nakonec vytvoří monomolekulární vrstvu, v níž jsou polární karboxylové skupiny vodíkově vázány na rozhraní vody a uhlovodíkové řetězce jsou uspořádány směrem od vody. Toto chování je znázorněno na obrázku vpravo. Látky, které se hromadí na povrchu vody a mění povrchové vlastnosti, se nazývají povrchově aktivní látky.
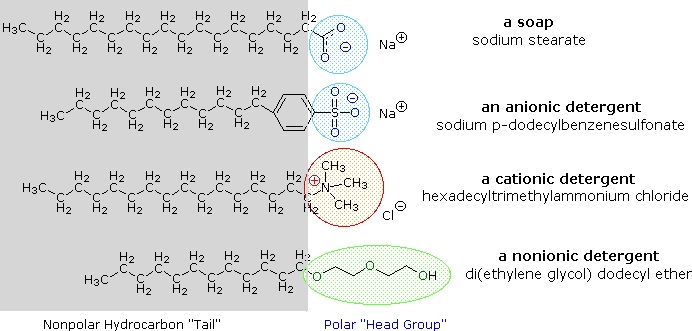
Soli alkalických kovů mastných kyselin jsou ve vodě rozpustnější než samotné kyseliny a amfifilní charakter těchto látek z nich rovněž činí silné povrchově aktivní látky. Nejběžnějšími příklady takových sloučenin jsou mýdla a detergenty, z nichž čtyři jsou uvedeny níže. Všimněte si, že každá z těchto molekul má nepolární uhlovodíkový řetězec, „ocas“, a polární (často iontovou) „hlavovou skupinu“. Použití těchto sloučenin jako čisticích prostředků usnadňuje jejich povrchově aktivní charakter, který snižuje povrchové napětí vody, což jí umožňuje pronikat do různých materiálů a smáčet je.
Velmi malá množství těchto povrchově aktivních látek se rozpouštějí ve vodě za vzniku náhodného rozptylu molekul rozpuštěné látky. Při zvýšení koncentrace však dochází k zajímavé změně. Molekuly povrchově aktivních látek se reverzibilně sdružují do polymolekulárních agregátů zvaných micely. Shromážděním hydrofobních řetězců ve středu micely se minimalizuje narušení struktury vodíkové vazby kapalné vody a polární hlavové skupiny se rozšíří do okolní vody, kde se účastní vodíkové vazby. Tyto micely mají často kulovitý tvar, ale mohou mít také válcovitý a rozvětvený tvar, jak je znázorněno na obrázku vpravo. Zde je polární hlavová skupina označena modrým kroužkem a nepolární ocas je klikatá černá čára.
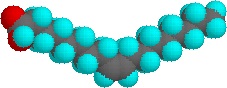
Nejstarším amfifilním čisticím prostředkem známým člověku je mýdlo. Mýdlo se vyrábí bazicky katalyzovanou hydrolýzou (zmýdelněním) živočišného tuku. Dříve než byl komerčně dostupný hydroxid sodný, používal se vařící roztok uhličitanu draselného vyluhovaného z dřevěného popela. Měkká draselná mýdla se pak promýváním roztokem soli měnila na tvrdší sodná mýdla. Význam mýdla pro lidskou civilizaci je historicky doložen, ale byly rozpoznány i některé problémy spojené s jeho používáním. Jeden z nich je způsoben slabou kyselostí (pKa cca 4,9) mastných kyselin. Roztoky mýdel alkalických kovů jsou v důsledku hydrolýzy mírně zásadité (pH 8 až 9). Pokud je pH roztoku mýdla sníženo kyselými nečistotami, nerozpustné mastné kyseliny se srážejí a tvoří pěnu. Druhý problém je způsoben přítomností vápenatých a hořečnatých solí v dodávané vodě (tvrdá voda). Tyto dvojmocné kationty způsobují agregaci micel, které se pak usazují jako špinavý pěna.
Tyto problémy byly zmírněny vývojem syntetických amfifilů zvaných detergenty (nebo syndety). Díky použití mnohem silnější kyseliny pro polární hlavovou skupinu jsou vodné roztoky amfifilů méně citlivé na změny pH. Také sulfonátové funkce používané prakticky u všech aniontových detergentů dodávají větší rozpustnost micelám obsahujícím kationty alkalických zemin, které se vyskytují v tvrdé vodě. Variace na téma amfifilů vedly k vývoji dalších tříd, jako jsou výše uvedené kationtové a neiontové detergenty. Kationtové detergenty často vykazují baktericidní vlastnosti a jejich schopnost měnit pH povrchu je učinila užitečnými jako změkčovadla tkanin a kondicionéry na vlasy. Tyto všestranné chemické „nástroje“ za posledních padesát let dramaticky proměnily trh s čisticími prostředky pro domácnost a osobní hygienu.
Přispěvatelé
-
William Reusch, emeritní profesor (Michigan State U.), Virtuální učebnice organické chemie
.
