- Rapporto annuale sulla cornea
- Cos’è il CXL e come funziona?
- Qual è il ruolo della riboflavina durante il CXL?
- Qual è lo scopo della rimozione epiteliale nel protocollo CXL standard?
- Come viene eseguito il protocollo standard CXL?
- Quali sono le raccomandazioni per la selezione dei pazienti?
- È necessaria la progressione della KCN per raccomandare il CXL?
- Dovrei considerare il CXL per i pazienti con più di 40 anni?
- Quali sono i risultati post-operatori generali del CXL e le aspettative?
- I pazienti con CXL possono aspettarsi dei cambiamenti refrattivi?
- Il CXL haze è una preoccupazione?
- È possibile eseguire il CXL senza rimuovere l’epitelio? Inoltre, gli eventi avversi sono rari dopo il CXL standard.10-13 Tuttavia, i ricercatori continuano a studiare metodi di somministrazione per aumentare il comfort durante e dopo la procedura, abbreviare il tempo di recupero visivo e ridurre i rischi di potenziali infezioni.
- 12. Quando si devono riapplicare le lenti a contatto dopo il CXL?
Rapporto annuale sulla cornea
Segui i link qui sotto per leggere altri articoli del nostro rapporto annuale sulla cornea:
Guida di un OD alle opzioni di trapianto corneale
Correggere un buco: Come guarire i difetti epiteliali persistenti
Allarme intruso: diagnosticare la malattia infiltrativa corneale
Per molti fornitori di cure oculari e pazienti, la gestione del cheratocono (KCN) può sembrare il mantenimento di uno status quo indesiderato. Grazie ai progressi nelle tecnologie delle lenti a contatto speciali, gli innesti corneali sono ora necessari solo per il 10-20% dei pazienti con KCN.1 Ciononostante, questi pazienti hanno ancora ottenuto punteggi simili a quelli dei pazienti con degenerazione maculare avanzata sul questionario della funzione visiva del National Eye Institute nel CLEK Study (Collaborative Longitudinal Evaluation of Keratoconus Study).2-5 Un altro rapporto dello stesso gruppo ha rilevato che i punteggi della qualità della vita auto-percepita dei pazienti con KCN continuano a diminuire nel tempo.6 Con una prevalenza postulata di KCN che raggiunge un individuo su 375, la stabilizzazione della malattia e il miglioramento o il mantenimento della qualità della vita sono priorità assolute.7
Dal suo sviluppo nel 2003, il crosslinking corneale (CXL) è diventato rapidamente il trattamento di scelta per il controllo della progressione della KCN.8 Sebbene il CXL abbia ricevuto l’approvazione della US Food and Drug Administration (FDA) solo nel 2016 (il sistema KXL di Avedro e due fotoendoscopi, Photrexa e Photrexa viscoso), siamo stati in grado di offrire trattamenti CXL ai pazienti per molti anni al Wills Eye Hospital sotto l’egida di studi clinici. Di conseguenza, gestiamo molti di questi pazienti con i medici della comunità.
Come per qualsiasi nuova procedura di trattamento, esiste una curva di apprendimento per i medici per perfezionare l’educazione del paziente e il processo di selezione, così come altri protocolli relativi alla gestione perioperatoria. Un canale di comunicazione aperto permette al nostro Corneal Service di aiutare i medici in comanaging ad acquisire comfort clinico con il CXL nelle loro pratiche KCN. Ecco 12 domande comuni poste dai nostri medici partner; le risposte possono aiutarvi a decidere come educare al meglio i vostri pazienti KCN sul CXL.
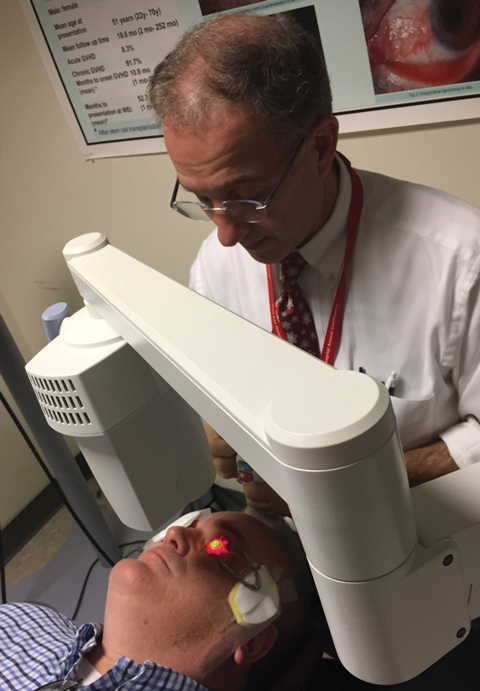
Fig. 1. Christopher Rapuano, MD, esegue un protocollo standard di crosslinking corneale con il sistema KXL approvato dalla FDA.
Cos’è il CXL e come funziona?
Il crosslinking è un processo di polimerizzazione che riorganizza i monomeri in una rete tridimensionale di polimeri per aumentare la solidità di una struttura molecolare. Questo processo avviene naturalmente nel nostro corpo quando i tessuti connettivi si irrigidiscono gradualmente nel tempo. Facilitato dall’enzima endogeno lisil ossidasi nell’avviare le reazioni ossidative necessarie, si formano ulteriori legami covalenti (o “crosslinks” tissutali) tra e all’interno delle fibrille di collagene, ottenendo una maggiore resistenza biomeccanica del tessuto.9
In genere, gli effetti cumulativi delle reazioni naturali di crosslinking si manifestano lentamente. Alla fine degli anni ’90, i ricercatori dell’Università di Dresda in Germania hanno stabilito che il processo di induzione fotochimica era il metodo clinicamente più valido per aumentare l’induzione di reticoli nella cornea, portando al CXL.8 Questo studio ha utilizzato lo 0,1% di riboflavina (con il 20% di destrano in soluzione) come fotosensibilizzatore per assorbire una dose di energia ultravioletta (UV) attentamente calibrata, convertendo così l’ossigeno disponibile nei tessuti in molecole di ossigeno singoletto. Le specie reattive di ossigeno risultanti possiedono energia sufficiente per attivare la via enzimatica della lisil ossidasi, portando alla formazione di nuovi legami covalenti all’interno dello stroma corneale.
Lo studio di Dresda ha riportato che tutti i 23 occhi progressivi KCN trattati sono stati stabilizzati, con il 70% che ha mostrato un appiattimento massimo della cheratometria di 2,01D. Da allora, molti studi hanno ottenuto un’efficacia simile con buoni profili di sicurezza nei pazienti KCN utilizzando lo stesso protocollo CXL che prevede la rimozione dell’epitelio (Figura 1).10-13
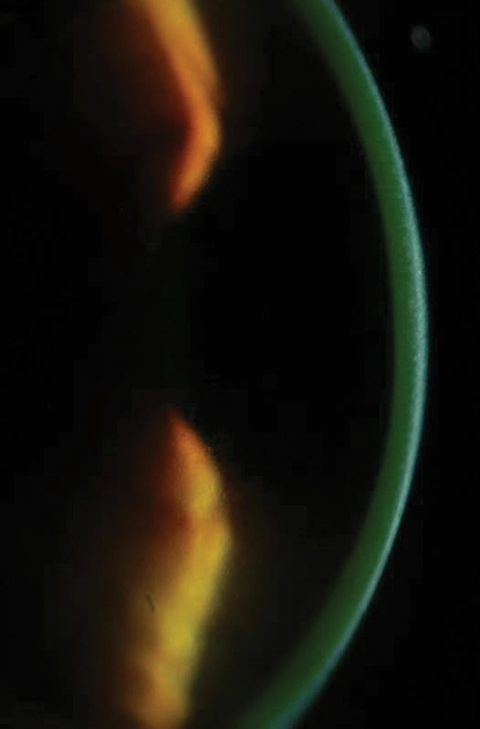
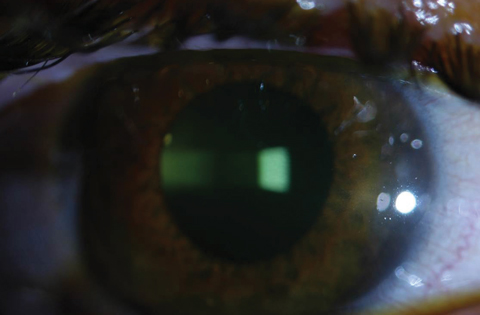
Figure 2a e 2b. Sopra, saturazione di riboflavina visto nello stroma corneale dopo il carico di riboflavina. Sotto, dopo 30 minuti di carico di riboflavina a intervalli di due minuti, i medici devono controllare la colorazione della riboflavina acquosa. Clicca sull’immagine in basso per ingrandire.
Qual è il ruolo della riboflavina durante il CXL?
Siccome le molecole di ossigeno biodisponibili nella cornea non possono essere attivate direttamente dalla luce UV, una sostanza fotosensibilizzante deve agire come agente intermedio. La riboflavina catalizza le reazioni fotochimiche del CXL trasferendo l’energia UV (in particolare, UVA da 365nm a 370nm) alle molecole di ossigeno stromale, convertendo così le molecole di ossigeno stabili in una forma singoletto più reattiva. Queste specie reattive dell’ossigeno avviano poi reazioni ossidative intrastromali.
Assumendo che l’energia UV non sia la risorsa limitante, il rifornimento continuo di ossigeno e le molecole di riboflavina attive sono essenziali per mantenere il trasferimento di energia necessario per perpetuare il processo CXL.
Inoltre, saturando la cornea con la riboflavina si crea un “effetto di schermatura” in cui i rispettivi livelli di energia UV che raggiungono l’endotelio, il cristallino e la retina sono titolati a un’intensità molto inferiore rispetto alle soglie di danno cellulare effettivo. Infatti, se una cornea satura di riboflavina ha uno spessore di almeno 400µm, l’irradiazione UV trasmessa all’endotelio è solo 0,18mW/cm2, mentre la soglia effettiva di danno endoteliale è di circa 0,35mW/cm2. Successivamente, il livello di energia proiettato per raggiungere il cristallino e la retina è ancora più basso rispetto alle rispettive soglie di danno di questi strati di tessuto.14,15
Qual è lo scopo della rimozione epiteliale nel protocollo CXL standard?
La natura lipofila dell’epitelio corneale e la piccola dimensione dei pori delle sue giunzioni strette rendono questo strato essenzialmente impermeabile alle molecole di riboflavina. Queste caratteristiche della barriera epiteliale impediscono una saturazione efficiente e omogenea della riboflavina nel tessuto stromale bersaglio.16
L’epitelio contiene anche enzimi con elevate proprietà antiossidanti come l’ascorbato e i residui di triptofano, che possono impedire la penetrazione dei raggi UV e pulire le specie reattive dell’ossigeno. Inoltre, la presenza di una barriera epiteliale rallenta il tasso di rifornimento di ossigeno durante le procedure CXL, riducendo così la quantità totale di nuovi crosslink cellulari che possono essere creati. Di conseguenza, quando lo stesso protocollo CXL standard viene eseguito con una superficie corneale intatta, l’efficacia complessiva della procedura sarà inferiore al previsto. D’altra parte, a causa della saturazione non omogenea della riboflavina e dei ridotti effetti di schermatura della riboflavina, le trasmissioni UV consegnate all’endotelio e ai tessuti oculari più profondi possono essere più elevate di quanto calcolato in precedenza.16,17
I clinici non dovrebbero dare per scontato che il CXL sia efficace solo se accompagnato da un debridement epiteliale. Sebbene le applicazioni di CXL transepiteliale (TE-CXL) non abbiano attualmente l’approvazione della FDA, sono allo studio tecniche di trattamento modificate per migliorare l’efficacia del TE-CXL.
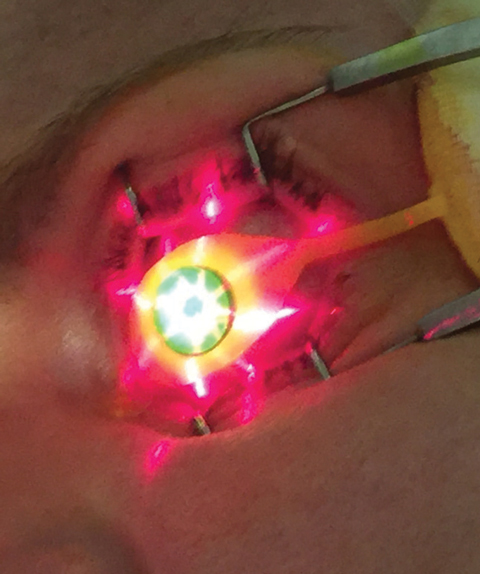
Fig. 3. La guida a croce viene proiettata dal dispositivo KXL sul sito di trattamento.
Come viene eseguito il protocollo standard CXL?
L’anestesia topica viene utilizzata durante la rimozione dei 9 mm centrali di epitelio per garantire il comfort del paziente e consentire una saturazione stromale più rapida e omogenea di Photrexa viscoso (riboflavina 5′-fosfato in soluzione oftalmica di destrano al 20%) durante il CXL. Questa fase dura 30 minuti con l’instillazione di riboflavina a intervalli di due minuti.10
Dopo 30 minuti, i pazienti vengono esaminati sotto la lampada a fessura per garantire che la riboflavina abbia saturato l’area di trattamento prevista e che sia presente nell’acquoso (Figure 2a e 2b). Secondo le indicazioni approvate dalla FDA, i medici devono eseguire la pachimetria dopo l’applicazione della riboflavina per assicurarsi che lo spessore corneale sia di almeno 400µm. Se è inferiore a 400 µm, la riboflavina ipotonica Photrexa deve essere somministrata ogni 5-10 secondi finché la cornea non è reidratata a 400 µm o più.10
Una volta verificato il livello di pachimetria appropriato, i medici utilizzano il dispositivo UV KXL (Avedro) per la seconda fase del trattamento CXL, dove 30 minuti di irradiazione UV (3mW/cm2) producono una dose di energia totale di 5,4J/cm2.8 Durante il periodo di emissione UV, il Photrexa viscoso viene instillato a intervalli di due minuti mentre l’operatore mantiene la corretta centratura e la distanza dispositivo-occhio. La corretta posizione del dispositivo KXL può essere guidata dalle proiezioni dell’immagine crosshair (Figura 3), che aiutano l’erogazione di un profilo ottimale del fascio di illuminazione alla cornea trattata.
La riboflavina in eccesso può essere risciacquata con una soluzione salina bilanciata alla fine di una sessione di trattamento. Una lente a contatto a benda (BCL) viene inserita dopo l’instillazione di agenti antibiotici e corticosteroidi topici. La BCL deve essere tenuta sull’occhio trattato per tre-cinque giorni o fino alla chiusura epiteliale (figure 4a e 4b).
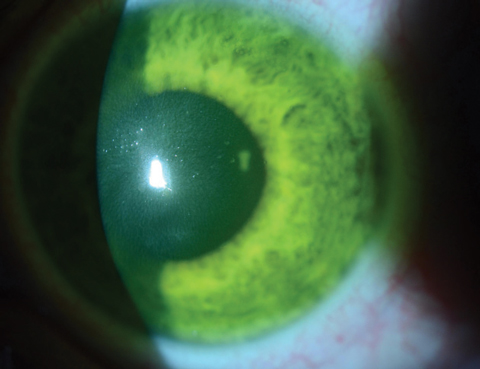
Fig. 4a. Qui, una lente a contatto morbida bendata è sull’occhio subito dopo il trattamento CXL su un paziente in cui la saturazione della riboflavina corneale è ancora evidente.
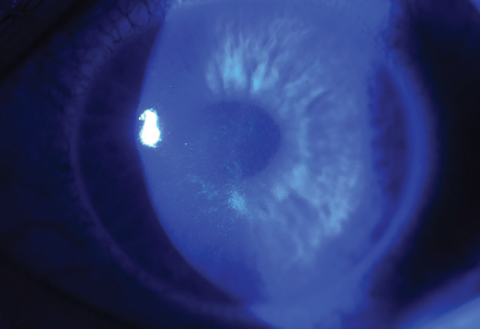
Fig. 4b. La chiusura della ferita epiteliale è per lo più completa sullo stesso paziente solo tre giorni dopo il trattamento con CXL.
Quali sono le raccomandazioni per la selezione dei pazienti?
Nel 2016, il protocollo standard CXL ha ricevuto indicazioni etichettate negli Stati Uniti per il trattamento di pazienti di età pari o superiore a 14 anni con KCN progressivo o ectasia corneale a seguito di interventi chirurgici refrattivi. Tuttavia, se non trattata, la gravità della malattia e il tasso di progressione sono noti per essere più aggressivi nei pazienti più giovani. Pertanto, il sistema KXL e Photrexa/Photrexa viscoso possono essere considerati per un uso off-label nei pazienti più giovani con uno spessore corneale minimo di 400µm o superiore. Pazienti con KCN a partire da otto anni sono stati riportati da studi clinici, ma in questi casi è necessario ottenere uno speciale consenso informato dai pazienti e dai loro tutori.18
Anche se la FDA non ha specificato alcuna controindicazione, i medici dovrebbero esercitare il loro giudizio prima di offrire il CXL alle madri in allattamento e ai pazienti con più di 65 anni di età. Inoltre, i ricercatori raccomandano vivamente di evitare il CXL durante il corso di una gravidanza. Uno studio recente ha trovato prove topografiche, pachimetriche e biomeccaniche di progressione del KCN nel 100% della sua coorte di pazienti incinte.19 Questo ha portato i ricercatori a raccomandare di discutere il CXL profilattico con le pazienti donne prima della pianificazione familiare. Alcuni paesi europei hanno iniziato a offrire proattivamente il CXL a pazienti donne con KCN che stanno pianificando una gravidanza nonostante la mancanza di progressione della malattia.20
È necessaria la progressione della KCN per raccomandare il CXL?
Anche se la progressione della KCN fa parte dell’indicazione on-label per il trattamento CXL, alcune circostanze non richiedono la progressione prima di una consultazione CXL. Le pazienti KCN di sesso femminile che stanno pianificando una gravidanza e i pazienti ad alto rischio di progressione sono solo due potenziali esempi clinici.19,21
Secondo il modello convenzionale di cura della KCN, una certa quantità di cambiamenti significativi nei parametri clinici deve manifestarsi prima di iniziare un nuovo ciclo di trattamento. Tuttavia, una progressione significativa si verifica spesso prima che venga intrapresa un’azione a causa della mancanza di consenso sull’esatto indicatore clinico e sulla corrispondente entità del cambiamento che costituisce la progressione della malattia. Molti studi CXL definiscono la progressione della KCN come cambiamenti in un periodo di 12 mesi in una qualsiasi delle seguenti misure: 1D o più nella cheratometria massima; 0,5D o più nella miopia; 1D o più nell’astigmatismo; o una perdita di 10µm o più nel punto pachimetrico più sottile.10-12,20,22 Tuttavia, con la limitata accuratezza dei topografi tradizionali nell’imaging della superficie corneale irregolare e la variabilità refrattiva dei pazienti con KCN, queste linee guida possono comportare un tasso più elevato di falsi positivi.
In alternativa, un gruppo di esperti ha recentemente raccomandato che la presenza di almeno due dei tre criteri può stabilire la progressione: aumento della curvatura corneale anteriore; aumento della curvatura corneale posteriore; o assottigliamento quando si confronta il profilo della distribuzione pachimetrica dalla periferia al punto più sottile.21 Anche se utili, queste linee guida richiedono l’accesso alla tomografia corneale in grado di tracciare i cambiamenti nel tempo, presentando una possibile sfida per alcuni clinici di comanaging.
Dati questi ostacoli clinici, il gruppo di esperti riunito da quattro società corneali sovranazionali ha concluso che le raccomandazioni CXL possono essere fatte ai pazienti KCN con profili ad alto rischio, anche se la progressione non è stata documentata.21
Dovrei considerare il CXL per i pazienti con più di 40 anni?
La risposta breve è sì. I pazienti con KCN tendono a mostrare un tasso di progressione più lento o persino una stabilizzazione nella loro quarta o quinta decade di vita, probabilmente un sottoprodotto della reticolazione associata all’età. Tuttavia, l’espressione della KCN è molto variabile e l’età da sola non è sempre un punto finale ben definito per la KCN. Una revisione retrospettiva delle cartelle cliniche del Wills Eye Hospital ha rilevato che il 24% dei 186 occhi con nuova diagnosi di KCN apparteneva a pazienti di 40 anni o più.23
Inoltre, dato che l’ectasia post-chirurgica può verificarsi in un momento successivo della vita rispetto ad un tipico paziente con KCN, il consenso clinico non ha definito un intervallo di età per quando l’ectasia si verifica tipicamente e quando la progressione può rallentare. Pertanto, i medici dovrebbero astenersi dall’utilizzare l’età come una controindicazione assoluta per la candidatura al CXL.
Quali sono i risultati post-operatori generali del CXL e le aspettative?
La fase iniziale di recupero dal CXL standard è molto simile a qualsiasi procedura che comporta la rimozione dell’epitelio corneale. Anche se le BCL offrono una protezione terapeutica e un maggiore comfort per il paziente, la maggior parte dei pazienti sperimenta ancora un certo disagio oculare o dolore fino alla chiusura del difetto epiteliale, che di solito avviene in tre-cinque giorni.24
Dopo la chiusura epiteliale, l’acuità visiva generalmente peggiora o oscilla notevolmente durante il primo mese prima di tornare lentamente alla linea di base entro il terzo mese. I pazienti possono sperimentare un lieve miglioramento della vista tra il terzo e il sesto mese o tra il sesto e il dodicesimo mese. Inoltre, una tendenza alla stabilizzazione emerge tipicamente come nuova linea di base tra i mesi sei e 12.10-12
Dopo il CXL standard, anche le misurazioni di cheratometria, pachimetria e foschia transitoria CXL seguono un modello temporale simile, con un ulteriore irripidimento, assottigliamento e riduzione della trasparenza corneale durante il primo mese. Queste tendenze tipicamente si invertono nei due mesi successivi, a quel punto i pazienti tornano lentamente alle caratteristiche di base. A volte questi pazienti sperimentano anche lievi miglioramenti prima di raggiungere un plateau di stabilizzazione (Figura 5).10-12
È importante evitare di interpretare erroneamente queste tendenze post-operatorie immediate come un peggioramento della malattia KCN o un fallimento del CXL. Nel complesso, nonostante un protocollo CXL epi-off, esiste solo un breve periodo durante l’immediato recupero post-operatorio in cui i pazienti possono sentirsi compromessi visivamente. Questo perché i pazienti vengono riadattati con lenti a contatto o possono riprendere l’uso delle lenti a contatto prima di raggiungere la stabilizzazione post-CXL.
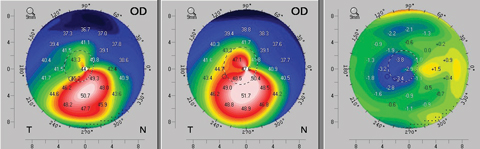
Fig. 5. Un esempio di appiattimento topografico visto già tre mesi dopo il protocollo standard (epi-off) di crosslinking corneale. La mappa di sinistra mostra la topografia assiale pre-operatoria del paziente. La mappa centrale è la topografia postoperatoria al terzo mese e la mappa di destra fornisce un calcolo delle differenze che rivela il miglioramento topografico al terzo mese. Clicca sull’immagine per ingrandirla.
I pazienti con CXL possono aspettarsi dei cambiamenti refrattivi?
Gli studi hanno riportato risultati variabili per sfera, cilindro ed equivalente sferico a 12 mesi dal trattamento CXL. Alcuni mostrano cambiamenti refrattivi statisticamente significativi, mentre altri non hanno registrato differenze degne di nota.25-27 I ricercatori hanno riportato miglioramenti nell’aberrazione totale di ordine superiore, nell’aberrazione sferica e nel coma, nonché un appiattimento topografico medio di 1,6D.10,28 Tuttavia, la letteratura non fornisce correlazioni coerenti tra i cambiamenti in questi parametri clinici e il trattamento CXL.
Di conseguenza, la stabilizzazione della KCN dovrebbe rimanere l’obiettivo primario dei protocolli CXL attualmente disponibili. Prima di raccomandare il CXL, i pazienti dovrebbero essere informati che le lenti a contatto o gli occhiali saranno ancora necessari dopo il CXL, e questo approccio di gestione può migliorare la qualità della vita dei pazienti, riducendo la frustrazione spesso associata a frequenti cambiamenti ottici quando la KCN non viene trattata.
Il CXL haze è una preoccupazione?
L’haze CXL transitorio può apparire simile all’haze corneale post-PRK. Con l’esperienza, tuttavia, i medici possono differenziare le due entità sotto la lampada a fessura. L’haze CXL crea un cambiamento di tessuto simile alla polvere nei livelli anteriori e medio-stromali, mentre l’haze PRK si manifesta con un modello di proliferazione fibrotica reticolare che è localizzato agli strati stromali subepiteliali e anteriori. Date le diverse apparenze anatomiche e la natura auto-risolutiva del CXL haze, è improbabile che abbia le stesse implicazioni visive del PRK haze.24
Immediatamente dopo il trattamento CXL, la microscopia confocale rivelerà l’apoptosi dei cheratociti e l’edema lacunare nell’area anteriore e medio-stromale. Quando le aree di foschia CXL e l’edema stromale iniziano a mostrare miglioramenti entro la fine del primo mese, i medici vedranno zone di discontinuità ottica – o linee di demarcazione – con una sezione ottica durante l’esame con lampada a fessura (Figura 6).24
Anche se l’abbagliamento è una possibilità durante le prime sei-otto settimane, la foschia CXL transitoria e la profondità delle linee di demarcazione sono spesso utilizzate come indicatori per riflettere la penetrazione del trattamento e il conseguente rimodellamento del collagene stromale. Con il lento ripopolamento dei cheratociti, la retrodiffusione della luce inizia a risolversi e le aree di foschia CXL iniziano a svanire tra i tre e i sei mesi. La foschia diventerà spesso impercettibile entro un anno dopo il CXL. Gli steroidi topici sono spesso interrotti dopo le prime settimane dopo la procedura, ma la maggior parte dei casi di foschia CXL si risolve da sola nel tempo senza ulteriori interventi terapeutici; quindi, i ricercatori suggeriscono gli steroidi topici non mitigano la foschia CXL e il loro uso a lungo termine non è necessario dopo il CXL standard. Tuttavia, uno studio ha proposto che gli steroidi topici possono essere giustificati se si osserva un haze persistente o una cicatrice stromale dopo il marchio di un anno.24,29
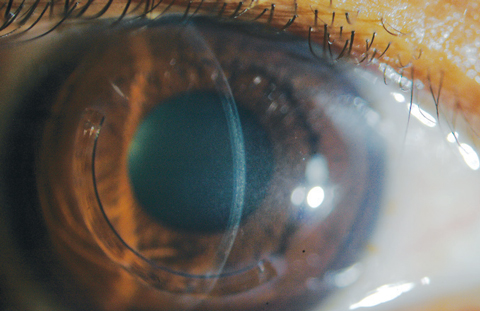
Fig. 6. Le linee di demarcazione sono visualizzate con sezione ottica in un paziente che ha ricevuto un trattamento off-label di CXL e impianto corneale Intacs (AJL Ophthalmic).
È possibile eseguire il CXL senza rimuovere l’epitelio? Inoltre, gli eventi avversi sono rari dopo il CXL standard.10-13 Tuttavia, i ricercatori continuano a studiare metodi di somministrazione per aumentare il comfort durante e dopo la procedura, abbreviare il tempo di recupero visivo e ridurre i rischi di potenziali infezioni.
Mantenere l’epitelio intatto riduce i tassi di diffusione di riboflavina, luce UV e ossigeno, che sono tutti essenziali per le reazioni fotochimiche durante il CXL. I ricercatori sono stati in grado di aggirare la funzione di barriera epiteliale interrompendo le giunzioni strette con stimolatori chimici come il cloruro di benzalconio (BAK) e l’acido etilendiamminotetraacetico (EDTA). Questi stimolatori corneali sono incorporati nella soluzione di riboflavina per aiutare la penetrazione nello stroma corneale. Tuttavia, alcuni studi hanno riportato linee di demarcazione meno profonde e ridotti effetti di irrigidimento corneale dopo il TE-CXL.30,31
Anche se diversi studi hanno riportato tassi di regressione più elevati con il TE-CXL, i suoi tassi di eventi avversi sono anche inferiori a quelli del CXL standard epi-off. Inoltre, la minore profondità del trattamento CXL può essere vantaggiosa in occhi con cornee più sottili al basale. I pazienti con un basso rischio di progressione e quelli che sono preoccupati per il tempo di recupero visivo possono essere candidati ragionevoli per il TE-CXL.24,30,31
Fino a quando l’efficacia del TE-CXL non migliorerà, continueremo a raccomandare il CXL standard epi-off per i pazienti KCN con un’alta probabilità di progressione o una progressione clinica aggressiva.
12. Quando si devono riapplicare le lenti a contatto dopo il CXL?
Uno studio che ha utilizzato la microscopia confocale ha dimostrato che lo spessore epiteliale ritorna gradualmente alla normalità tra i tre e i sei mesi dopo il CXL standard.24 Tuttavia, molti pazienti richiedono la riabilitazione delle lenti a contatto per funzionare e non possono aspettare sei mesi prima di riprendere l’uso delle lenti a contatto.
L’emergere del CXL ha inaugurato una nuova era di gestione del KCN in cui i medici non devono più assumere un approccio gestionale passivo reattivo e offrire ai pazienti solo una scelta forzata tra lenti a contatto e innesti corneali. Con un intervento CXL precoce per i candidati appropriati e un monitoraggio continuo post-CXL, i medici possono aiutare i pazienti a mantenere la loro migliore funzione visiva e a differire al massimo le possibili necessità di cheratoplastiche. L’attenzione clinica di oggi dovrebbe andare oltre la semplice sostituzione delle lenti a contatto con il progredire del KCN. Con la diagnosi precoce del KCN, l’accesso al CXL e i progressi nelle geometrie delle lenti speciali, i medici possono aiutare i loro pazienti con KCN a vivere la vita al massimo.
Il dottor Chang è direttore delle lenti speciali per la cornea al Wills Eye Hospital-Cornea Service e direttore dei servizi clinici alla TLC Vision. È membro del consiglio consultivo dell’Accademia Internazionale del Cheratocono, del Gas Permeable Lens Institute e della Optometric Cornea, Cataract and Refractive Society.
Il Dott. Rapuano è capo del Servizio di Cornea al Wills Eye Hospital. Ha pubblicato diversi libri, numerosi capitoli di libri e oltre 175 articoli sottoposti a revisione paritetica, tra cui il Wills Eye Manual di cui è coautore.
1. Godefrooij DA, Gans R, Imhof SM, Wisse RP. Riduzione a livello nazionale del numero di trapianti di cornea per il cheratocono dopo l’implementazione del cross-linking. Acta Ophthalmol. 2016;94(7):675-8.
2. Davidson AE, Hayes S, Hardcastle AJ, et al. The pathogenesis of keratoconus. Occhio (Lond). 2014;28(2):189-95.
3. Tuft SJ, Moodaley LC, Gregory WM, et al. Fattori prognostici per la progressione del cheratocono. Oftalmologia. 1994;101(3):439-47.
4. Gordon MO, Steger-May K, Szczotka-Flynn L, et al. Baseline factors predictive of incident penetrating keratoplasty in keratoconus. Am J Ophthalmol. 2006;142(6):923-30.
5. Kymes SM, Walline JJ, Zadnik K, Gordon MO. Qualità della vita nel cheratocono. Am J Ophthalmol. 2004;138(4):527-35.
6. Kymes SM, Walline JJ, Zadnik K, et al. Changes in the quality-of-life of people with keratoconus. Am J Ophthalmol. 2008;145(4):611-7.
7. Godefrooij DA, de Wit GA, Uiterwaal CS, et al. Incidenza e prevalenza specifica per età del cheratocono: uno studio di registrazione nazionale. Am J Ophthalmol. 2017;175:169-72.
8. Wollensak G, Spoerl E, Seiler T. Riboflavin/ultraviolet-a-induced collagen crosslinking for the treatment of keratoconus. Am J Ophthalmol 2003;135(5):620-7.
9. Schumacher S, Mrochen M, Wernli J, et al. Modello di ottimizzazione per il cross-linking corneale UV-riboflavina. Invest Ophthalmol Vis Sci. 2012;53(2):762-9.
10. Chang CY, Hersh PS. Cross-linking del collagene corneale: una revisione dei risultati a 1 anno. Occhio lente a contatto. 2014;40(6):345-52.
11. Hersh PS, Stulting RD, Muller D, et al. Studio clinico multicentrico degli Stati Uniti di cross-linking del collagene corneale per il trattamento del cheratocono. Ophthalmology. 2017;124(9):1259-70.
12. Hersh PS, Stulting RD, Muller D, et al. US multicenter clinical trial of corneal collagen crosslinking for treatment of corneal ectasia after refractive surgery. Ophthalmology. 2017;124(10):1475-84.
13. Raiskup F, Theuring A, Pillunat LE, Spoerl E. Crosslinking del collagene corneale con riboflavina e luce ultravioletta-a nel cheratocono progressivo: risultati a dieci anni. J Cataract Refract Surg. 2015;41(1):41-6.
14. Spoerl E, Mrochen M, Sliney D, Trokel S, Seiler T. Sicurezza del cross-linking UVA-riboflavina della cornea. Cornea. 2007 maggio;26(4):385-9.
15. Schumacher S, Mrochen M, Wernli J, et al. Modello di ottimizzazione per il cross-linking corneale UV-riboflavina. Invest Ophthalmol Vis Sci. 2012;53(2):762-9.
16. Bottós KM, Schor P, Dreyfuss JL, et al. Effetto dell’epitelio della cornea sull’assorbimento degli ultravioletti e della riboflavina. Arq Bras Oftalmol. 2011;74(5):348-51.
17. Richoz O, Hammer A, Tabibian D, et al. L’effetto biomeccanico del cross-linking del collagene corneale (CXL) con riboflavina e UV-A è ossigeno dipendente. Transl Vis Sci Technol. 2013;2(7):6.
18. Padmanabhan P, Rachapalle Reddi S, Rajagopal R, et al. Collagene corneale cross-linking per cheratocono in pazienti pediatrici – risultati a lungo termine. Cornea. 2017;36(2):138-43.
19. Naderan M, Jahanrad A. Cambiamenti topografici, tomografici e biomeccanici della cornea durante la gravidanza in pazienti con cheratocono: uno studio di coorte. Acta Ophthalmol. 2017;95(4):e291-e296.
20. Sandvik GF, Thorsrud A, Råen M, et al. Does corneal collagen cross-linking reduce the need for keratoplasties in patients with keratoconus? Cornea. 2015;34(9):991-5.
21. Gomes JA, Tan D, Rapuano CJ, et al. Consenso globale sul cheratocono e le malattie ectatiche. Cornea. 2015;34(4):359-69.
22. Nordström M, Schiller M, Fredriksson A, Behndig A. Miglioramenti refrattivi e sicurezza con il crosslinking corneale guidato dalla topografia per il cheratocono: risultati a 1 anno. Br J Ophthalmol. 2017;101(7):920-5.
23. Yildiz EH, Diehl GF, Cohen EJ, et al. Demografia dei pazienti con più di 50 anni con cheratocono. Occhio lente a contatto. 2009;35(6):309-11.
24. Mazzotta C, Hafezi F, Kymionis G, et al. Microscopia confocale in vivo dopo il crosslinking del collagene corneale. Ocul Surf. 2015;13(4):298-314.
25. Cınar Y, Kürs¸at Cingü A, Turkcu FM, et al. Accelerato collagene cross-linking corneale per cheratocono progressivo. Cutan Ocul Toxicol. 2014;33:168-71.
26. Kanellopoulos AJ. Risultati a lungo termine di uno studio prospettico randomizzato di confronto bilaterale dell’occhio di più alta fluenza, più breve durata di radiazione ultravioletta a, e riboflavina collagene cross-linking per il cheratocono progressivo. Clin Ophthalmol. 2012;6:97-101.
27. Cummings AB, McQuaid R, Naughton S, et al. Ottimizzazione del cross-linking corneale nel trattamento del cheratocono: un confronto dei risultati dopo protocolli standard e ad alta intensità. Cornea. 2016;35(6):814-22.
28. Vinciguerra P, Albè E, Trazza S, et al. Analisi refrattiva, topografica, tomografica e aberrometrica di occhi cheratoconici sottoposti a cross-linking corneale. Ophthalmology. 2009;116(3):369-78.
29. Kim BZ, Jordan CA, McGhee CN, Patel DV. Storia naturale dell’haze corneale dopo il crosslinking del collagene corneale nel cheratocono usando l’analisi di Scheimpflug. J Cataract Refract Surg. 2016;42(7):1053-9.
30. Wollensak G, Iomdina E. Cambiamenti biomeccanici e istologici dopo crosslinking corneale con e senza debridement epiteliale. J Cataract Refract Surg. 2009;35(3):540-6.
31. Caporossi A, Mazzotta C, Paradiso AL, et al. Crosslinking transepiteliale del collagene corneale per il cheratocono progressivo: risultati clinici a 24 mesi. J Cataract Refract Surg. 2013;39(8):1157-63.
