- o-Xylene Właściwości chemiczne, zastosowania, produkcja
- Xylene
- Destylacja precyzyjna do rozdzielania O-ksylenu i p-ksylenu
- Właściwości chemiczne
- Zastosowanie
- Metoda produkcji
- Kategoria
- Klasyfikacja toksyczności
- Toksyczność ostra
- WYBUCHOWOŚĆ I CHARAKTERYSTYKA NIEBEZPIECZNA
- Zapalność i charakterystyka zagrożeń
- Charakterystyka magazynowania i transportu
- Środki gaśnicze
- Norma zawodowa
- Właściwości chemiczne
- Właściwości fizyczne
- Definicja
- Opis syntezy
- Opis ogólny
- Powietrze &Reakcje z wodą
- Profil reaktywności
- Zagrożenie dla zdrowia
- Zagrożenie pożarowe
- Reaktywność chemiczna
- Profil bezpieczeństwa
- Postać w środowisku
- Metody oczyszczania
o-Xylene Właściwości chemiczne, zastosowania, produkcja
Xylene
Ksylen odnosi się do węglowodoru aromatycznego z dwoma atomami wodoru na pierścieniu benzenowym zastąpionymi przez dwie grupy metylowe. Posiada trzy izomery: o-ksylen (1,2-dimetylobenzen), m-ksylen i p-ksylen. Produktami przemysłowymi są mieszaniny tych trzech izomerów o zawartości 10% o-10%, 70% m- i 20% p-. W przemyśle koksowniczym jest to jeden z surowych produktów rafinacji benzenu.
Ksylen jest rodzajem bezbarwnej cieczy palnej; temperatura topnienia o-, m-i p-ksylenu wynosi-25.2 ℃,-47.9 ℃ i 13.3 ℃; temperatury wrzenia wynoszą odpowiednio 144.4 ℃, 139.1 ℃ i 138.3 ℃, podczas gdy gęstość względna jest 0.8802, 0.8642 i 0.8611, odpowiednio; To nie jest rozpuszczalny w wodzie, ale miesza się z wielu rodzajów rozpuszczalników organicznych immiscibility. Po katalitycznym utlenianiu, odpowiednio, generują bezwodnik ftalowy, kwas izoftalowy i kwas tereftalowy.
Ksylen jest jednym z rodzajów ważnych surowców chemikaliów organicznych, naturalnie występujących w smole węglowej i niektórych rodzajach ropy naftowej. Można go uzyskać poprzez frakcjonowanie lekkiej części oleju ze smoły węglowej lub katalitycznego reformowania lekkiej benzyny. Przemysł głównie prowadzi ekstrakcję przy użyciu frakcji C8 w reformatach benzyny ciężkiej. Alternatywnie może być wytwarzany w reakcji dysproporcjonowania toluenu w obecności katalizatora, w wysokiej temperaturze i pod wysokim ciśnieniem. W chwili obecnej przemysł stosuje głównie metodę krystalizacji kriogenicznej, adsorpcji i tworzenia kompleksów lub sit molekularnych w celu ich oddzielenia. O-ksylen ma stosunkowo wysoką temperaturę wrzenia i może być oddzielony za pomocą destylacji. p-ksylen ma również wysoką temperaturę topnienia i może być oczyszczony poprzez frakcyjną krystalizację. Mieszanina ksylenów bez rozdzielania może być bezpośrednio stosowana jako rozpuszczalnik, a dodanie jej do benzyny może poprawić jej właściwości przeciwwybuchowe. Są one składnikami benzyny lotniczej. O-ksylen jest stosowany głównie do przygotowania bezwodnika ftalowego, który jest ważnym surowcem do produkcji różnych barwników i wskaźników (takich jak fenoloftaleina). Ponadto, o-ksylen może być również stosowany do przygotowania żywicy poliestrowej, środka odstraszającego owady, plastyfikatorów i barwników. M-ksylen, poprzez nitrowanie i redukcję, może wytworzyć 4,6-dimetylo-1,3-fenylenodiaminę, która jest półproduktem dla barwników syntetycznych. M-ksylen może być również wykorzystywany jako surowiec do produkcji syntetycznych substancji zapachowych (takich jak piżmo ksylenowe). P-ksylen jest stosowany głównie do wytwarzania kwasu tereftalowego, który jest ważnym surowcem do produkcji syntetycznych włókien poliestrowych (poliestru).
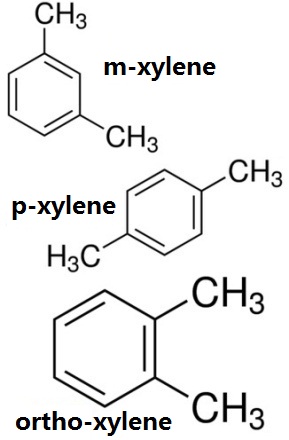
Rysunek 1 przedstawia strukturę chemiczną trzech izomerów ksylenu, orto-ksylenu, m-ksylenu, p-ksylenu.
Powyższe informacje zostały zredagowane przez Chemicalbook.
Destylacja precyzyjna do rozdzielania O-ksylenu i p-ksylenu
Ksylen występuje w koksowanym surowym benzenie i krakowanej ropie naftowej. Surowy benzen, po wstępnej destylacji, przemyciu kwasem siarkowym i destylacji w celu oddzielenia benzenu i toluenu, a następnie destylacji, możemy otrzymać ksylen, znany również jako koksowany ksylen. Jakość koksowanego ksylenu zależy od zdolności rozdzielczej kolumny destylacyjnej, temperatury na szczycie kolumny i współczynnika refluksu. Chiny sklasyfikowały produkty z ksylenu koksowniczego na trzech poziomach. Ksylen koksowniczy zawiera zazwyczaj 16% o-ksylenu, 50% m-ksylenu, 21% p-ksylenu i 7% etylobenzenu. Ksylen produkowany w przemyśle naftowym charakteryzuje się niską zawartością m-ksylenu i wysoką zawartością etylobenzenu. Ksylen przemysłowy jest nie tylko rozpuszczalnikiem i dodatkiem w przemyśle gumowym i lakierniczym, ale także dodatkiem do paliw lotniczych i energetycznych. O-ksylen, m-ksylen i p-ksylen oddzielone od ksylenu przemysłowego są surowcami odpowiednio do produkcji kwasu ftalowego, kwasu izoftalowego i kwasu tereftalowego. Kwas ftalowy i kwas tereftalowy są stosowane w produkcji plastyfikatorów, żywic poliestrowych i włókien poliestrowych. M-ksylen może być stosowany samodzielnie jako rozpuszczalnik i dodatek do paliw. O-ksylen zawarty w przemysłowym ksylenie ma ponad 5,2 ℃ różnicy z innymi izomerami. Dzięki precyzyjnej destylacji możemy uzyskać o-ksylen o czystości ponad 95%, a następnie użyć sulfonowania i destylacji do oczyszczania, dzięki czemu możemy uzyskać dalsze czystsze o-ksylen.
ksylen należy do zasad Lewisa, które mogą tworzyć polarny kompleks z HF-BF3 (kwas Lewisa). Zasadowość M-ksylenu jest około 100 razy silniejsza niż innych aromatów C8. Kiedy mieszanina izomerów ksylenu wchodzi w kontakt z rozpuszczalnikiem HF-BF3, m-ksylen może tworzyć kompleks z fluorem i jest preferencyjnie ekstrahowany do fazy fluorkowej. Faza fluorkowa zawierająca m-ksylen jest ogrzewana pod niższym ciśnieniem w celu rozłożenia kompleksu, co powoduje oddzielenie m-ksylenu od mieszaniny. Rozpuszczalnik HF-BF3 może być odzyskany w procesie destylacji w celu recyklingu. Jeżeli surowiec jest mieszaniną orto-ksylenu, m-ksylenu i p-ksylenu, po wyekstrahowaniu m-ksylenu możemy dalej stosować destylację precyzyjną w celu oddzielenia o-ksylenu i p-ksylenu.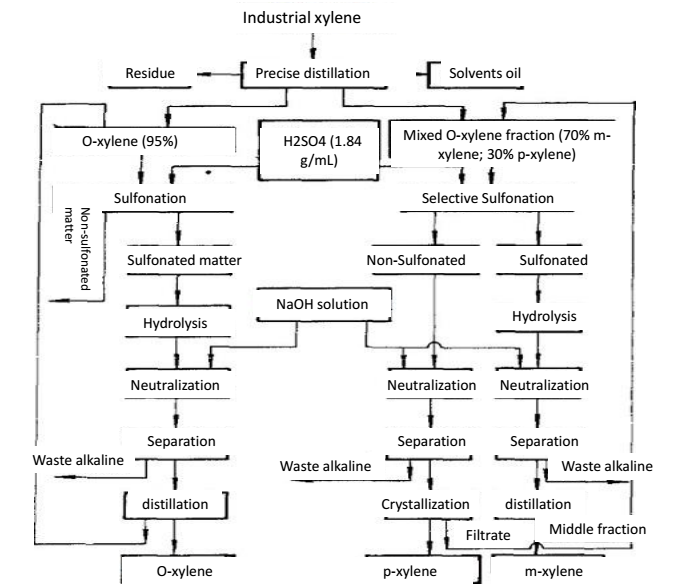
Rysunek 2: Metoda destylacji precyzyjnej do rozdzielania o-ksylenu i p-ksylenu.
Właściwości chemiczne
Występuje jako bezbarwna, przezroczysta ciecz o zapachu aromatycznym. Jest mieszalny z etanolem, eterem etylowym, acetonem i benzenem, ale nie rozpuszcza się w wodzie.
Zastosowanie
(1) Stosowany głównie w produkcji bezwodnika ftalowego
(2) O-ksylen jest surowcem do produkcji środka bakteriobójczego fenraminy, peptydu tetrachlorofenylu i herbicydu bensulfuronu metylowego. Jest stosowany jako półprodukt do produkcji kwasu o-metylobenzoesowego.
(3) Jest stosowany głównie jako surowce chemiczne i rozpuszczalniki. Może być stosowany do produkcji bezwodnika ftalowego, barwników, pestycydów i leków, takich jak witaminy. Może być również stosowany jako dodatki do benzyny lotniczej.
(4) Stosowany jako wzorce chromatograficzne i rozpuszczalniki
(5) Jako surowce do syntezy bezwodnika i innych syntez organicznych;
Metoda produkcji
Przemysł zastosował metodę superdestylacji w celu oddzielenia o-ksylenu od mieszanego ksylenu. O-ksylen ma ponad 5 ℃ różnicy w temperaturze wrzenia w porównaniu z innymi składnikami w mieszanym ksylenie. Do destylacji, wymagany numer tacy jest około 150; współczynnik refluksu jest 5-8 i zużywają stosunkowo dużo energii.
O-ksylen był pierwotnie produkowany głównie ze smoły węglowej. Obecnie większość krajowej i zagranicznej produkcji o-ksylenu odbywa się głównie poprzez ekstrakcję z ropy naftowej w procesie reformingu katalitycznego i krakingu termicznego węglowodorów aromatycznych. Ze względu na to, że struktury o-ksylenu, p-ksylenu i m-ksylenu w ksylenie są bardzo podobne, ich parametry fizyczne są również dość podobne. Przemysłowa separacja o-ksylenu głównie przyjmuje metodę superdestylacji; najpierw należy oddzielić o-ksylen i etylobenzen od mieszanego ksylenu, co wymaga użycia 100~150 tacek wieży destylacyjnej; następnie należy oddzielić o-ksylen i etylobenzen, aby uzyskać czysty o-ksylen.
Kategoria
Ciecze łatwopalne
Klasyfikacja toksyczności
Zatrucie
Toksyczność ostra
Toksyczność doustna- szczur LDL0: 5000 mg/kg; wstrzyknięcie do jamy brzusznej- mysz LD50: 1364 mg/kg
WYBUCHOWOŚĆ I CHARAKTERYSTYKA NIEBEZPIECZNA
bycie wybuchowym po zmieszaniu z powietrzem
Zapalność i charakterystyka zagrożeń
bycie łatwopalnym pod wpływem płomienia, ciepła, utleniacza łatwopalny przy spalaniu wydzielający drażniący dym
Charakterystyka magazynowania i transportu
magazyn: wentylowany, w niskiej temperaturze i suchy; delikatnie ładować i rozładowywać; przechowywać oddzielnie od utleniaczy i kwasów.
Środki gaśnicze
mgła wodna, piana, piasek, dwutlenek węgla, 1211 środek gaśniczy
Norma zawodowa
TLV-TWA 100 PPM (440 mg/m 3); STEL 150; PPM (655 mg/m 3)
Właściwości chemiczne
bezbarwna ciecz
Właściwości fizyczne
Klarowna, bezbarwna ciecz o zapachu aromatycznym. Nagata i Takeuchi (1990) stwierdzili, że stężenie progowe zapachu wynosi 380 ppbv.
Definicja
ChEBI: Ksylen podstawiony grupami metylowymi w pozycjach 1 i 3.
Opis syntezy
Journal of the American Chemical Society, 97, str. 7262, 1975 DOI: 10.1021/ja00858a011
The Journal of Organic Chemistry, 44, str. 2185, 1979 DOI: 10.1021/jo01327a032
Opis ogólny
Bezbarwna, wodnista ciecz o słodkim zapachu. Gęstość mniejsza niż wody. Nierozpuszczalny w wodzie. Opary drażniące.
Powietrze &Reakcje z wodą
Wysoce łatwopalna. Nierozpuszczalny w wodzie.
Profil reaktywności
1,2-Dimetylobenzen może reagować z materiałami utleniającymi. .
Zagrożenie dla zdrowia
Opary powodują bóle i zawroty głowy. Ciecz działa drażniąco na oczy i skórę. W przypadku dostania się do płuc, powoduje silny kaszel, niepokój i szybko rozwijający się obrzęk płuc. W przypadku spożycia powoduje mdłości, wymioty, skurcze, ból głowy i śpiączkę. Może być śmiertelny. Może wystąpić uszkodzenie nerek i wątroby.
Zagrożenie pożarowe
Zachowanie podczas pożaru: Opary są cięższe od powietrza i mogą pokonać znaczną odległość do źródła zapłonu i cofnąć się.
Reaktywność chemiczna
Reaktywność z wodą Brak reakcji; Reaktywność z materiałami powszechnego użytku: Brak reakcji; Stabilność podczas transportu: Stabilny; Środki neutralizujące dla kwasów i substancji żrących: Nie dotyczy; Polimeryzacja: Nie dotyczy; Inhibitor polimeryzacji: Nie dotyczy.
Profil bezpieczeństwa
Umiarkowanie toksyczny bj7drogą dootrzewnową. Działa silnie toksycznie przez drogi pokarmowe i oddechowe. Teratogen doświadczalny. Powszechnie występujące zanieczyszczenie powietrza. Bardzo niebezpieczne zagrożenie pożarowe w kontakcie z gorącem lub płomieniem. Wybuchowy w postaci oparów w kontakcie z ciepłem lub płomieniem. Do gaszenia pożaru należy używać piany, CO2, suchej chemii. Niekompatybilny z materiałami utleniającymi. Po podgrzaniu do rozkładu wydziela ostry dym i drażniące opary. Emitowany z nowoczesnych materiałów budowlanych (CENEAR69,22,91). Zobacz również inne wpisy dotyczące ksylenu.
Thomas i Delfino (1991) zrównoważyli wolne od zanieczyszczeń wody gruntowe pobrane z Gainesville, FL z poszczególnymi frakcjami trzech pojedynczych produktów naftowych w temperaturze 24-25 °C przez 24 h. Faza wodna była analizowana pod kątem związków organicznych metodą testową602 zatwierdzoną przez U.S. EPA. Średnie stężenia m+p-ksylenu odnotowane w rozpuszczalnych w wodzie frakcjach benzyny bezołowiowej, nafty i oleju napędowego wynosiły odpowiednio 8,611, 0,658 i 0,228 mg/L. Kiedy autorzy przeanalizowali fazę wodną za pomocą zatwierdzonej przez U.S. EPA metody badawczej 610, średnie stężenia m+p-ksylenu we frakcjach rozpuszczalnych w wodzie benzyny bezołowiowej, nafty i oleju napędowego były niższe, tj. odpowiednio 6,068, 0,360 i 0,222 mg/L. Na podstawie analizy laboratoryjnej 7 próbek smoły węglowej, stężenia o-ksylenu wahały się od 2 do 2000 ppm (EPRI, 1990). Wysokotemperaturowa smoła węglowa zawierała o-ksylen w średnim stężeniu 0,04 % mas. (McNeil, 1983).
Schauer et al. (2001) zmierzyli wskaźniki emisji lotnych związków organicznych, półlotnych związków organicznych w fazie gazowej i związków organicznych w fazie cząsteczkowej ze spalania sosny, dębu i eukaliptusa w budynkach mieszkalnych (kominek). Wskaźnik emisji o-ksylenu w fazie gazowej wynosił 18,1 mg/kg spalonej sosny. Wskaźniki emisji o-ksylenu nie były mierzone podczas spalania dębu i eukaliptusa.
Standard wody pitnej (ostateczny): Dla wszystkich ksylenów, MCLG i MCL wynoszą zarówno 10 mg/L. Dodatkowo zalecono DWEL równy 70 mg/L (U.S. EPA, 2000).
Postać w środowisku
Biologiczne. Zgłoszone produkty biodegradacji komercyjnego produktu zawierającego ksylen obejmują kwas α-hydroksy-p-toluowy, alkohol p-metylobenzylowy, alkohol benzylowy, 4-metylokatechol, kwasy mandp-toluowe (Fishbein, 1985). o-ksylen był również kometabolizowany, w wyniku czego powstawał kwas o-toluowy (Pitter i Chudoba, 1990). W beztlenowych wodach gruntowych w pobliżu Bemidji, MI, o-ksylenanaerobowo biodegradował do pośredniego kwasu o-toluowego (Cozzarelli et al., 1990). W wodach gruntowych zanieczyszczonych benzyną, kwas metylobenzylobursztynowy został zidentyfikowany jako pierwszy półprodukt podczas beztlenowej degradacji ksylenów (Reusser i Field, 2002).
Fotolityczne. Cox et al. (1980) podali stałą szybkości 1,33 x 10-11 cm3/molekułę? s dla reakcji gazowego o-ksylenu z rodnikami OH w oparciu o wartość 8 x 10-12 cm3/molekułę? s dla reakcji etylenu z rodnikami OH.
Woda powierzchniowa. Okres półtrwania parowania o-ksylenu w wodach powierzchniowych (głębokość 1 m) w temperaturze 25 °C szacuje się na 5,18 h (Mackay i Leinonen, 1975).
Wody gruntowe. Nielsen et al. (1996) badali degradację o-ksylenu w płytkiej, glacjofluwialnej, nie ograniczonej piaszczystej warstwie wodonośnej w Jutlandii, Dania. W ramach badań mikrokosmosu in situ, cylinder otwarty u dołu i ekranowany u góry został zainstalowany w otworze orurowanym około 5 m poniżej poziomu. Pięć litrów wody napowietrzano powietrzem atmosferycznym, aby zapewnić utrzymanie warunków tlenowych. Wody gruntowe analizowano co tydzień przez około 3 miesiące w celu określenia stężenia o-ksylenu w czasie. Doświadczalnie określona stała szybkości biodegradacji pierwszego rzędu i odpowiadający jej okres półtrwania po 7-dniowej fazie opóźnienia wynosiły odpowiednio 0,1/d i 6,93 d.
Fotolityczne. Kiedy syntetyczne powietrze zawierające gazowy kwas azotowy i o-ksylen zostało wystawione na działanie sztucznego światła słonecznego (λ = 300-450 nm), biacetyl, azotan nadtlenoacetalu i azotan metylu tworzyły produkty uboczne (Cox et al., 1980). Roztwór n-heksanu zawierający o-ksylen i rozprowadzony w postaci cienkiej warstwy (4 mm) na zimnej wodzie (10 °C) napromieniowano rtęciową lampą średniociśnieniową. W ciągu 3 h 13,6% o-ksylenu uległo fotoutlenieniu do o-metylobenzaldehydu, alkoholu o-benzylowego, kwasu o-benzoesowego i ometyloacetofenonu (Moza i Feicht, 1989). Napromieniowanie o-ksylenu w temperaturze ≈ 2537 ? w temperaturze 35 °C i pod ciśnieniem 6 mmHg ulega izomeryzacji do m-ksylenu (Calvert i Pitts, 1966). Glioksal, metyloglioksal i biacetyl powstały w wyniku fotoutleniania o-ksylenu przez rodniki OH w powietrzu w temperaturze 25 °C (Tuazon et al.,1986a).
Chemiczne/fizyczne. W warunkach atmosferycznych reakcja o-ksylenu w fazie gazowej z rodnikami OH i tlenkami azotu prowadzi do powstania o-tolualdehydu, azotanu o-metylobenzylu, nitro-o-ksylenów, 2,3- i 3,4-dimetylofenolu (Atkinson, 1990). Kanno et al. (1982) badali reakcję wodną o-ksylenu i innych węglowodorów aromatycznych (benzenu, toluenu, m- i p-ksylenu oraz naftalenu) z kwasem podchlorawym w obecności jonu amonowego. Stwierdzono, że pierścień aromatyczny nie ulega chlorowaniu, jak oczekiwano, lecz zostaje rozszczepiony przez chloraminę, tworząc chlorek cyjanogenu. Ilość powstałego chlorku cyjanogenu wzrastała przy niższych pH (Kanno i in., 1982). W fazie gazowej o-ksylen reagował z rodnikami azotanowymi w oczyszczonym powietrzu, tworząc następujące produkty: 5-nitro-2-metylotoluen i 6-nitro-2-metylotoluen, o-metylobenzaldehyd i azotan arylu (Chiodini i in., 1993).
Metody oczyszczania
o-Xylen (4,4 kg) jest sulfonowany przez mieszanie przez 4 godziny z 2,5 l stężonego H2SO4 w temperaturze 95o. Po schłodzeniu i oddzieleniu niesulfonowanego materiału, produkt rozcieńcza się 3L wody i zobojętnia 40% NaOH. Po schłodzeniu oddziela się sulfonian oksylenowo-sodowy, który rekrystalizuje się z połowy masy wody. Sól rozpuszcza się w minimalnej ilości zimnej wody, następnie miesza się ją z taką samą ilością zimnej wody i z taką samą objętością stężonego H2SO4 i ogrzewa do temperatury 110o. o-ksylen jest regenerowany i destylowany z parą wodną. Destylat nasyca się NaCl, oddziela się warstwę organiczną, suszy i ponownie destyluje.
