- Jaarlijks hoornvliesverslag
- Wat is CXL en hoe werkt het?
- Wat is de rol van riboflavine tijdens CXL?
- Wat is het doel van epitheliale verwijdering in het standaard CXL protocol?
- Hoe wordt het standaard CXL-protocol uitgevoerd?
- Wat zijn de aanbevelingen voor patiëntselectie?
- Is KCN-progressie noodzakelijk om CXL aan te bevelen?
- Moet ik CXL overwegen voor patiënten ouder dan 40?
- Wat zijn de algemene CXL postoperatieve bevindingen en verwachtingen?
- Kunnen CXL-patiënten refractieveranderingen verwachten?
- Is waas door CXL een probleem?
- Kan men CXL uitvoeren zonder het epitheel te verwijderen?
- 12. Wanneer moet ik contactlenzen vervangen na CXL?
Jaarlijks hoornvliesverslag
Volg de onderstaande links om andere artikelen uit ons jaarlijkse hoornvliesverslag te lezen:
De gids van een OD voor hoornvliestransplantatieopties
Een gaatje dichten: How to Heal Persistent Epithelial Defects
Intruder Alert: Diagnosing Corneal Infiltrative Disease
Voor veel oogzorgverleners en patiënten kan de behandeling van keratoconus (KCN) aanvoelen als het handhaven van een ongewenste status-quo. Dankzij de vooruitgang in gespecialiseerde contactlenstechnologieën zijn hoornvliestransplantaties nu nog maar nodig voor 10% tot 20% van de KCN-patiënten.1 Desondanks scoren deze patiënten nog steeds vergelijkbaar met patiënten met gevorderde maculadegeneratie op de vragenlijst voor visuele functie van het National Eye Institute in de CLEK-studie (Collaborative Longitudinal Evaluation of Keratoconus Study).2-5 Uit een ander rapport van dezelfde groep bleek dat de zelf waargenomen scores voor de kwaliteit van leven van KCN-patiënten in de loop der tijd blijven dalen.6 Met een veronderstelde KCN prevalentie van één op de 375 personen, zijn stabilisatie van de ziekte en verbetering of behoud van de kwaliteit van leven topprioriteiten.7
Sinds de ontwikkeling in 2003 is corneale crosslinking (CXL) snel uitgegroeid tot de behandeling bij uitstek voor de beheersing van de progressie van KCN.8 Hoewel CXL pas in 2016 goedkeuring kreeg van de Amerikaanse Food and Drug Administration (FDA) (Avedro’s KXL System en twee photoenhancers, Photrexa en Photrexa viscous), kunnen we in het Wills Eye Hospital al vele jaren CXL-behandelingen aanbieden aan patiënten onder auspiciën van klinische trials. Als gevolg daarvan behandelen we veel van deze patiënten samen met artsen in de gemeenschap.
Zoals bij elke nieuwe behandelingsprocedure moeten artsen leren hoe ze de voorlichting aan de patiënt en het selectieproces kunnen verfijnen, evenals andere protocollen met betrekking tot het perioperatieve beheer. Een open communicatiekanaal stelt onze Corneal Service in staat om comanaging artsen te helpen klinisch comfort te krijgen met CXL in hun KCN-praktijk. Hier zijn 12 veel voorkomende vragen die onze partner-artsen stellen; de antwoorden kunnen u helpen beslissen hoe u uw KCN-patiënten het beste kunt voorlichten over CXL.
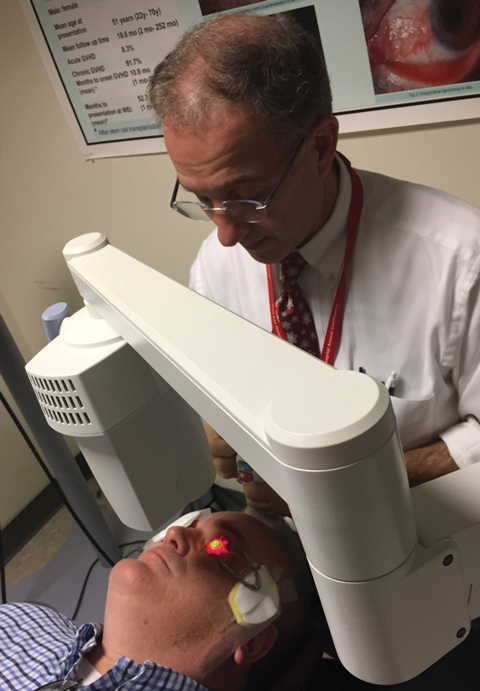
Fig. 1. Christopher Rapuano, MD, voert standaard een corneale crosslinking-protocol uit met het door de FDA goedgekeurde KXL-systeem.
Wat is CXL en hoe werkt het?
Crosslinking is een polymerisatieproces waarbij monomeren worden herschikt tot een driedimensionaal netwerk van polymeren om de soliditeit van een moleculaire structuur te vergroten. Dit proces vindt van nature in ons lichaam plaats wanneer bindweefsels na verloop van tijd stijf worden. Gefaciliteerd door het endogene enzym lysyloxidase bij het lanceren van de vereiste oxidatiereacties, worden extra covalente bindingen (of weefsel “crosslinks”) gevormd tussen en binnen collageenfibrillen – wat een verhoogde biomechanische sterkte van het weefsel oplevert.9
Typisch gezien manifesteren de cumulatieve effecten van natuurlijke crosslinking-reacties zich traag. Eind jaren negentig stelden onderzoekers van de Universiteit van Dresden in Duitsland vast dat het fotochemische inductieproces de klinisch meest haalbare methode was om de inductie van crosslinks in het hoornvlies te stimuleren en zo CXL tot stand te brengen.8 In deze studie werd 0,1% riboflavine (met 20% dextraan in oplossing) als fotosensibilisator gebruikt om een zorgvuldig gekalibreerde ultraviolette (UV) energiedosis te absorberen, waardoor beschikbare weefselzuurstof wordt omgezet in singletzuurstofmoleculen. De resulterende reactieve zuurstofspecies bezitten voldoende energie om de enzymatische route van lysyloxidase te activeren, wat leidt tot de vorming van nieuwe covalente bindingen binnen het hoornvliesstroma.
De studie uit Dresden rapporteerde dat alle 23 behandelde progressieve KCN ogen gestabiliseerd waren, waarbij 70% een maximale keratometrische afvlakking vertoonde van 2.01D. Sindsdien is in veel studies een vergelijkbare werkzaamheid met een goed veiligheidsprofiel bereikt bij KCN-patiënten, waarbij gebruik werd gemaakt van hetzelfde CXL-protocol waarbij epitheelcellen werden verwijderd (figuur 1).10-13
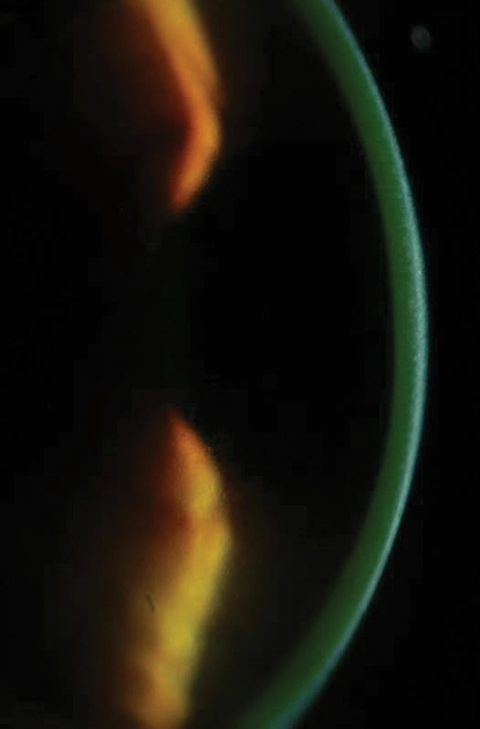
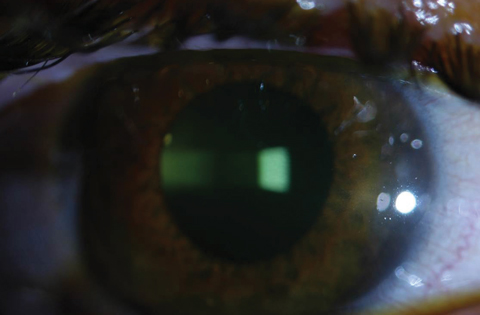
Figuren 2a en 2b. Boven, verzadiging van riboflavine gezien in het hoornvlies stroma na riboflavine laden. Onder, na 30 minuten riboflavine-belasting met tussenpozen van twee minuten, moeten clinici controleren op waterige riboflavine-kleuring. Klik op de onderste afbeelding voor een vergroting.
Wat is de rol van riboflavine tijdens CXL?
Omdat de biobeschikbare zuurstofmoleculen in het hoornvlies niet rechtstreeks door UV-licht kunnen worden geactiveerd, moet een fotosensibiliserende stof als tussenstof fungeren. Riboflavine katalyseert de fotochemische reacties van CXL door UV-energie (met name UVA van 365 nm tot 370 nm) over te brengen op stromale zuurstofmoleculen, waardoor stabiele zuurstofmoleculen worden omgezet in een meer reactieve singletvorm. Deze reactieve zuurstofsoorten zetten vervolgens intrastromale oxidatieve reacties in gang.
Aannemende dat UV-energie niet de beperkende bron is, zijn voortdurende zuurstofaanvulling en actieve riboflavine moleculen essentieel voor het in stand houden van de energieoverdracht die nodig is om het CXL-proces te laten voortduren.
Daarnaast creëert verzadiging van het hoornvlies met riboflavine een “afschermingseffect”, waarbij de respectieve UV-energieniveaus die het endotheel, de lens en het netvlies bereiken, worden getitreerd tot een veel lagere intensiteit dan de feitelijke cellulaire schadedrempels. Als een met riboflavine verzadigd hoornvlies ten minste 400 µm dik is, bedraagt de UV-straling die het endotheel bereikt slechts 0,18mW/cm2 , terwijl de werkelijke schadedrempel voor het endotheel ongeveer 0,35mW/cm2 bedraagt. Daarna is het energieniveau dat wordt geprojecteerd om de kristallijne lens en het netvlies te bereiken nog lager in vergelijking met de respectieve schadedrempels van deze weefsellagen.14,15
Wat is het doel van epitheliale verwijdering in het standaard CXL protocol?
De lipofiele aard van het hoornvliesepitheel en de kleine poriegrootte van zijn tight junctions maken deze laag in wezen ondoordringbaar voor riboflavine moleculen. Deze epitheliale barrière-eigenschappen verhinderen een efficiënte en homogene verzadiging van riboflavine in het beoogde stromale weefsel.16
Epitheel bevat ook enzymen met hoge antioxiderende eigenschappen, zoals ascorbaat en tryptofaanresiduen, die UV-penetratie kunnen verhinderen en reactieve zuurstofsoorten kunnen wegvangen. Bovendien vertraagt de aanwezigheid van een epitheliale barrière de snelheid van de zuurstofaanvulling tijdens CXL-procedures, waardoor de totale hoeveelheid nieuwe cellulaire crosslinks die kan worden gecreëerd, wordt verminderd. Bijgevolg zal, wanneer hetzelfde standaard CXL-protocol wordt uitgevoerd met een intact hoornvliesoppervlak, de algehele doeltreffendheid van de procedure lager zijn dan verwacht. Aan de andere kant, als gevolg van niet-homogene riboflavine verzadiging en verminderde riboflavine afschermingseffecten, kunnen UV transmissies die worden afgegeven aan het endotheel en dieper gelegen oogweefsels hoger zijn dan eerder berekend.16,17
Cliniciens moeten er niet van uitgaan dat CXL alleen effectief is wanneer het gepaard gaat met epitheliaal debridement. Hoewel transepitheliale CXL-toepassingen (TE-CXL) momenteel geen goedkeuring van de FDA hebben, worden aangepaste behandelingstechnieken onderzocht om de doeltreffendheid van TE-CXL te vergroten.
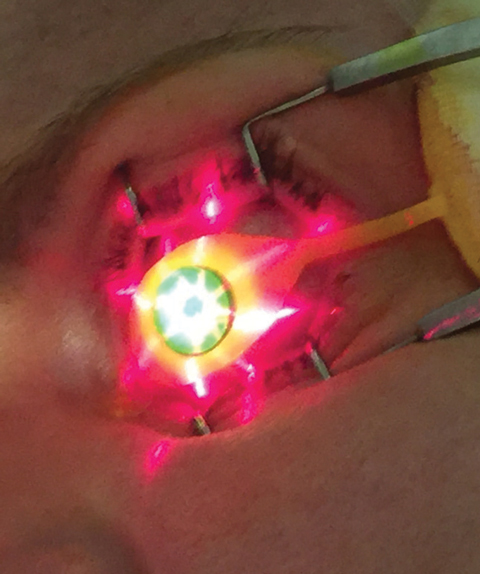
Fig. 3.
Hoe wordt het standaard CXL-protocol uitgevoerd?
Topische anesthesie wordt gebruikt bij het verwijderen van de centrale 9 mm epitheel om het comfort van de patiënt te waarborgen en een snellere, homogenere stromale verzadiging van Photrexa viscous (riboflavine 5′-fosfaat in 20% dextran oogheelkundige oplossing) tijdens CXL mogelijk te maken. Deze fase duurt 30 minuten met riboflavine-instillatie in intervallen van twee minuten.10
Na 30 minuten worden de patiënten onder de spleetlamp onderzocht om te verzekeren dat de riboflavine het beoogde behandelingsgebied heeft verzadigd en dat het aanwezig is in het waterige (figuren 2a en 2b). Volgens de door de FDA goedgekeurde indicaties moeten artsen na het aanbrengen van riboflavine een pachymetrie uitvoeren om er zeker van te zijn dat de dikte van het hoornvlies ten minste 400 µm bedraagt. Als de dikte minder is dan 400 µm, moet hypotone Photrexa riboflavine om de vijf tot 10 seconden worden toegediend totdat de cornea is gerehydrateerd tot 400 µm of meer.10
Als het juiste pachymetrieniveau is vastgesteld, gebruiken artsen het KXL UV-apparaat (Avedro) voor de tweede fase van de CXL-behandeling, waarbij 30 minuten UV-straling (3mW/cm2) een totale energiedosis van 5,4 J/cm2 oplevert.8 Tijdens de UV-emissieperiode wordt met tussenpozen van twee minuten Photrexa viscous toegediend, terwijl de operator de juiste centrering en afstand tussen apparaat en oog handhaaft. De juiste positie van het KXL-apparaat kan worden bepaald door de projecties van het dradenkruis (figuur 3), die helpen bij het afgeven van een optimaal verlichtingsstraalprofiel aan de behandelde cornea.
Overtollige riboflavine kan aan het eind van een behandelingssessie worden afgespoeld met een uitgebalanceerde zoutoplossing. Een bandage contactlens (BCL) wordt ingebracht na instillatie van topische antibiotica en corticosteroïden. De BCL moet op het behandelde oog worden gehouden gedurende drie tot vijf dagen of totdat het epitheel zich sluit (Figuren 4a en 4b).
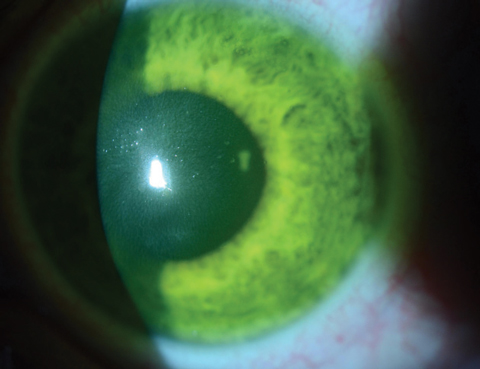
Fig. 4a. Hier is een verband zachte contactlens op het oog onmiddellijk na CXL behandeling op een patiënt waar cornea riboflavine saturatie nog steeds duidelijk is.
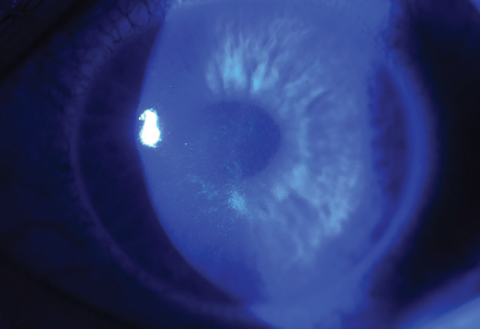
Fig. 4b. Epitheliale wondsluiting is grotendeels voltooid bij dezelfde patiënt slechts drie dagen na de behandeling met CXL.
Wat zijn de aanbevelingen voor patiëntselectie?
In 2016 kreeg het standaard CXL-protocol in de Verenigde Staten gelabelde indicaties voor de behandeling van patiënten van 14 jaar of ouder met progressieve KCN of corneale ectasie na refractieve operaties. Het is echter bekend dat wanneer de ziekte onbehandeld blijft, de ernst ervan en de mate van progressie agressiever zijn bij jongere patiënten. Daarom kunnen het KXL systeem en Photrexa/Photrexa viscous worden overwogen voor off-label gebruik bij jongere patiënten met een minimale corneale dikte van 400µm of meer. KCN patiënten zo jong als acht zijn gerapporteerd door klinische studies, maar speciale geïnformeerde toestemming moet worden verkregen van de patiënten en hun voogden in deze gevallen.18
Hoewel de FDA geen contra-indicaties heeft gespecificeerd, moeten clinici oordeelkundig te werk gaan alvorens CXL aan te bieden aan zogende moeders en patiënten ouder dan 65 jaar. Ook bevelen onderzoekers sterk aan CXL te vermijden tijdens een zwangerschap. Een recente studie vond topografische, pachymetrische en biomechanische aanwijzingen van KCN progressie in 100% van het zwangere patiënten cohort.19 Dit bracht onderzoekers ertoe aan te bevelen profylactische CXL te bespreken met vrouwelijke patiënten voorafgaand aan gezinsplanning. Sommige Europese landen zijn begonnen met het proactief aanbieden van CXL aan vrouwelijke KCN-patiënten die van plan zijn zwanger te worden, ondanks het ontbreken van ziekteprogressie.20
Is KCN-progressie noodzakelijk om CXL aan te bevelen?
Hoewel KCN-progressie deel uitmaakt van de on-label indicatie voor CXL-behandeling, is in bepaalde omstandigheden progressie niet noodzakelijk voor een CXL-consult. Vrouwelijke KCN-patiënten die van plan zijn zwanger te worden en patiënten met een hoog risico op progressie zijn slechts twee mogelijke klinische voorbeelden.19,21
Volgens het conventionele KCN-zorgmodel moet er enige mate van betekenisvolle veranderingen in klinische parameters optreden voordat een nieuwe behandelingskuur kan worden gestart. Er treedt echter vaak significante progressie op voordat actie wordt ondernomen, vanwege het gebrek aan consensus over de exacte klinische indicator en de bijbehorende grootte van verandering die ziekteprogressie vormt. Veel CXL studies definiëren KCN progressie als veranderingen over een periode van 12 maanden in een van de volgende metingen: 1D of meer in maximale keratometrie; 0,5D of meer in myopie; 1D of meer in astigmatisme; of 10µm of meer verlies in dunste pachymetrische punt.10-12,20,22 Echter, met de beperkte nauwkeurigheid van de traditionele topografen bij het imagen van het onregelmatige hoornvliesoppervlak en de refractieve variabiliteit van KCN-patiënten, kunnen deze richtlijnen resulteren in een hoger percentage vals-positieven.
Als alternatief heeft een panel van deskundigen onlangs aanbevolen dat de aanwezigheid van ten minste twee van drie criteria progressie kan vaststellen: steilheid van de anterieure corneale kromming; steilheid van de posterieure corneale kromming; of dunner worden bij vergelijking van het pachymetrische distributieprofiel van de periferie tot het dunste punt.21 Hoewel deze richtlijnen nuttig zijn, vereisen ze toegang tot corneatomografie die in staat is om veranderingen in de tijd te volgen, wat een mogelijke uitdaging vormt voor sommige comanagerende clinici.
Gezien deze klinische hindernissen concludeerde het panel van deskundigen, samengesteld uit vier supranationale corneaverenigingen, dat aanbevelingen voor CXL kunnen worden gedaan aan KCN-patiënten met een hoog risicoprofiel, zelfs als progressie niet is gedocumenteerd.21
Moet ik CXL overwegen voor patiënten ouder dan 40?
Het korte antwoord is ja. KCN-patiënten hebben de neiging een langzamere progressie te vertonen of zelfs een stabilisatie in hun vierde of vijfde levensdecennium – waarschijnlijk een bijproduct van leeftijdsgebonden crosslinking. De expressie van KCN is echter zeer variabel, en leeftijd alleen is niet altijd een goed gedefinieerd eindpunt voor KCN. Uit een retrospectief onderzoek van het Wills Eye Hospital bleek dat 24% van de 186 nieuw gediagnosticeerde ogen met KCN toebehoorden aan patiënten van 40 jaar of ouder.23
Bovendien, gezien het feit dat postchirurgische ectasie op latere leeftijd kan optreden dan bij een typische KCN-patiënt, heeft de klinische consensus geen leeftijdsbereik gedefinieerd voor wanneer ectasie typisch optreedt en wanneer de progressie kan vertragen. Daarom moeten artsen leeftijd niet als een absolute contra-indicatie voor CXL gebruiken.
Wat zijn de algemene CXL postoperatieve bevindingen en verwachtingen?
De beginfase van herstel na standaard CXL is vergelijkbaar met elke andere procedure waarbij hoornvliesepitheel wordt verwijderd. Hoewel BCL’s therapeutische bescherming bieden en het comfort van de patiënt verhogen, ervaren de meeste patiënten nog steeds enig oculair ongemak of pijn totdat het epitheeldefect sluit, wat gewoonlijk na drie tot vijf dagen gebeurt.24
Na epitheelsluiting verslechtert de gezichtsscherpte over het algemeen of fluctueert deze sterk gedurende de eerste maand, voordat deze tegen de derde maand langzaam terugkeert naar het basisniveau. Patiënten kunnen een lichte verbetering van het gezichtsvermogen ervaren tussen de derde en de zesde maand of tussen de zesde en de twaalfde maand. Bovendien ontstaat er gewoonlijk een stabilisatietrend als de nieuwe basislijn tussen de zes en twaalf maanden.10-12
Na standaard CXL volgen keratometrie, pachymetrie en voorbijgaande CXL waasmetingen ook een vergelijkbaar temporaal patroon, met verdere steilheid, verdunning en vermindering van de corneatransparantie gedurende de eerste maand. Deze trends keren gewoonlijk in de loop van de volgende twee maanden om, waarna de patiënten langzaam terugkeren naar hun basiskenmerken. Soms ondervinden deze patiënten zelfs lichte verbeteringen alvorens een stabilisatieplateau te bereiken (afbeelding 5).10-12
Het is belangrijk om deze onmiddellijke postoperatieve trends niet verkeerd te interpreteren als verslechtering van de KCN ziekte of CXL mislukking. Over het geheel genomen is er, ondanks een epi-off CXL-protocol, slechts een korte periode tijdens het onmiddellijke postoperatieve herstel waarin patiënten zich visueel gecompromitteerd kunnen voelen. Dit komt doordat patiënten worden omgebouwd in contactlenzen of weer contactlenzen kunnen gaan dragen voordat zij post-CXL stabilisatie bereiken.
Fig. 5. Een voorbeeld van topografische afvlakking die al drie maanden na het standaard (epi-off) corneale crosslinking protocol wordt gezien. De linker kaart toont de pre-operatieve axiale topografie van de patiënt. De middelste kaart is de postoperatieve topografie op maand drie, en de rechter kaart geeft een verschil berekening onthult de topografische verbetering op maand drie. Klik op de afbeelding om te vergroten.
Kunnen CXL-patiënten refractieveranderingen verwachten?
Er zijn in studies uiteenlopende resultaten gerapporteerd voor bol, cilinder en sferisch equivalent na 12 maanden na de CXL-behandeling. Sommige laten statistisch significante refractieveranderingen zien, terwijl andere geen opmerkelijke verschillen lieten zien.25-27 Onderzoekers hebben verbeteringen gemeld in de totale hogere-orde aberratie, sferische aberratie en coma, evenals een gemiddelde topografische afvlakking van 1,6D.10,28 Toch geeft de literatuur geen consistente correlaties tussen veranderingen in deze klinische parameters en de CXL-behandeling.
Dientengevolge moet KCN stabilisatie het primaire doel blijven van de momenteel beschikbare CXL protocollen. Alvorens CXL aan te bevelen, moeten patiënten worden geïnformeerd dat contactlenzen of een bril nog steeds nodig zullen zijn na CXL, en deze aanpak kan de kwaliteit van leven van patiënten verbeteren door de frustratie te verminderen die vaak gepaard gaat met frequente optische veranderingen wanneer KCN onbehandeld blijft.
Is waas door CXL een probleem?
Transiente CXL waas kan vergelijkbaar lijken met post-PRK corneale waas. Met ervaring kunnen artsen de twee entiteiten echter van elkaar onderscheiden onder de spleetlamp. CXL waas creëert een stof-achtige weefselverandering in de anterieure tot mid-stromale niveaus, terwijl PRK waas zich manifesteert in een gereticuleerd fibrotisch proliferatiepatroon dat gelokaliseerd is in de subepitheliale tot anterieure stromale lagen. Gezien de verschillende anatomische verschijningsvormen en de zelfoplossende aard van CXL waas, is het onwaarschijnlijk dat het dezelfde visuele implicaties heeft als PRK waas.24
Onmiddellijk na de CXL behandeling zal confocale microscopie keratocyt apoptose en lacunair oedeem aantonen in het anterieure tot midden-stromale gebied. Als aan het eind van de eerste maand de gebieden met CXL-waas en stromaal oedeem beginnen te verbeteren, zien artsen bij spleetlamponderzoek zones van optische discontinuïteit – of demarcatielijnen – met een optische doorsnede (figuur 6).24
Hoewel verblinding gedurende de eerste zes tot acht weken een mogelijkheid is, worden voorbijgaande CXL-waas en diepte van demarcatielijnen vaak gebruikt als indicatoren om de penetratie van de behandeling en de resulterende stromale collageenvernieuwing te weerspiegelen. Naarmate de keratocyten zich langzaam repopuleren, begint de lichtverstrooiing op te lossen en beginnen de gebieden met CXL waas tussen drie en zes maanden te vervagen. Een jaar na de CXL is de waas vaak niet meer te zien. Topische steroïden worden vaak gestaakt na de eerste paar weken na de procedure, maar de meeste gevallen van CXL waas verdwijnen vanzelf na verloop van tijd zonder verdere therapeutische interventies; daarom suggereren onderzoekers dat topische steroïden CXL waas niet verminderen en dat langdurig gebruik ervan niet nodig is na standaard CXL. In één studie werd echter voorgesteld dat het gebruik van topische steroïden gerechtvaardigd kan zijn als er na een jaar aanhoudende waas of stromale littekenvorming wordt waargenomen.24,29
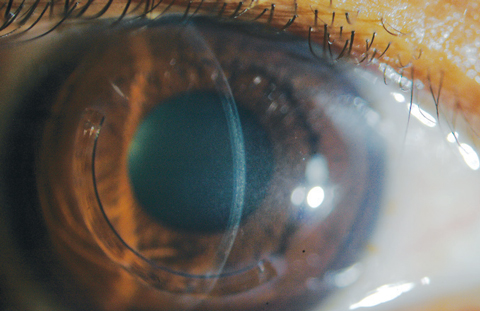
Fig. 6. De demarcatielijnen worden gevisualiseerd met een optische doorsnede bij een patiënt die een off-label behandeling van CXL en Intacs hoornvliesimplantaat (AJL Ophthalmic) kreeg.
Kan men CXL uitvoeren zonder het epitheel te verwijderen?
Standaard epi-off CXL is minimaal invasief en zeer effectief in het tot stilstand brengen van de progressie van KCN. Bovendien zijn bijwerkingen zeldzaam na standaard CXL.10-13 Onderzoekers blijven echter onderzoek doen naar toedieningsmethoden om het comfort tijdens en na de procedure te verhogen, de visuele hersteltijd te verkorten en de risico’s van mogelijke infectie te verminderen.
Het intact houden van het epitheel vermindert de diffusiesnelheid van riboflavine, UV-licht en zuurstof, die allemaal essentieel zijn voor de fotochemische reacties tijdens CXL. Onderzoekers zijn erin geslaagd de epitheliale barrièrefunctie te omzeilen door de tight junctions te verstoren met chemische versterkers zoals benzalkoniumchloride (BAK) en ethyleendiaminetetraazijnzuur (EDTA). Deze hoornvliesversterkers worden in de riboflavineoplossing opgenomen om het doordringen in het hoornvliesstroma te bevorderen. Sommige studies hebben echter ondiepere demarcatielijnen en verminderde corneale verstijvingseffecten gemeld na TE-CXL.30,31
Hoewel verschillende studies hogere regressiepercentages meldden met TE-CXL, zijn de percentages van bijwerkingen ook lager dan die van standaard epi-off CXL. Bovendien kan de geringere diepte van de CXL-behandeling voordelig zijn bij ogen met dunnere cornea’s bij aanvang. Patiënten met een laag risico op progressie en diegenen die bezorgd zijn over de visuele hersteltijd kunnen redelijke kandidaten zijn voor TE-CXL.24,30,31
Tot de werkzaamheid van TE-CXL verbetert, zullen wij standaard epi-off CXL blijven aanbevelen voor KCN-patiënten met een hoog risico op progressie of agressieve klinische progressie.
12. Wanneer moet ik contactlenzen vervangen na CXL?
Een onderzoek met confocale microscopie toonde aan dat de epitheliale dikte geleidelijk weer normaal wordt tussen drie en zes maanden na standaard CXL.24 Veel patiënten hebben echter contactlensrevalidatie nodig om te kunnen functioneren en kunnen niet zes maanden wachten alvorens het dragen van contactlenzen te hervatten.
Onze persoonlijke benadering is om een lensaanpasstrategie te hanteren die minimale tot geen interactie toestaat tussen het achterste lensoppervlak en het corneale epitheel, gezien de mogelijkheid van aanhoudende waas bij vertraagde epitheliale genezing of verstoorde epitheliale remodellering. Verschillende lensontwerpen kunnen helpen dit doel te bereiken, waaronder die met corneale vaulting capaciteiten, zoals hybride, scleral, piggyback en zelfs op maat gemaakte zachte lenzen. Uit klinische ervaring weten we dat het ideale moment om een lens te vervangen ongeveer vier tot zes weken is na standaard CXL of twee weken na TE-CXL. Het is ook verstandig om patiënten, vooral na standaard CXL, erop te wijzen dat zij in de komende zes tot twaalf maanden regelmatig refractiewijzigingen in hun contactlenzen kunnen verwachten.
De opkomst van CXL heeft een nieuw tijdperk ingeluid van KCN management, waarin clinici niet langer een passieve reactieve management benadering hoeven aan te nemen en patiënten slechts een geforceerde keuze hoeven te bieden tussen contactlenzen en corneatransplantaten. Met vroegtijdige CXL interventie voor geschikte kandidaten en voortdurende controle na CXL, kunnen clinici patiënten helpen hun beste visuele functie te behouden en de mogelijke noodzaak van keratoplastieken maximaal uit te stellen. De klinische focus van vandaag de dag moet verder gaan dan alleen het vervangen van contactlenzen wanneer KCN voortschrijdt. Met vroegtijdige detectie van KCN, toegang tot CXL en vooruitgang in speciale lensontwerpen, kunnen artsen hun KCN-patiënten helpen het leven ten volle te leven.
Dr. Chang is directeur van Cornea Specialty Lenses bij Wills Eye Hospital-Cornea Service en directeur van klinische diensten bij TLC Vision. Hij is lid van de adviesraad van de International Keratoconus Academy, het Gas Permeable Lens Institute en de Optometric Cornea, Cataract and Refractive Society.
Dr. Rapuano is hoofd van de Cornea Service in het Wills Eye Hospital. Hij heeft verschillende boeken gepubliceerd, talrijke boekhoofdstukken en meer dan 175 peer-reviewed artikelen, waaronder mede-auteur van The Wills Eye Manual.
1. Godefrooij DA, Gans R, Imhof SM, Wisse RP. Nationwide reduction in the number of corneal transplantations for keratoconus following the implementation of cross-linking. Acta Ophthalmol. 2016;94(7):675-8.
2. Davidson AE, Hayes S, Hardcastle AJ, et al. De pathogenese van keratoconus. Eye (Lond). 2014;28(2):189-95.
3. Tuft SJ, Moodaley LC, Gregory WM, et al. Prognostische factoren voor de progressie van keratoconus. Oogheelkunde. 1994;101(3):439-47.
4. Gordon MO, Steger-May K, Szczotka-Flynn L, et al. Baseline factors predictive of incident penetrating keratoplasty in keratoconus. Am J Ophthalmol. 2006;142(6):923-30.
5. Kymes SM, Walline JJ, Zadnik K, Gordon MO. Kwaliteit van leven in keratoconus. Am J Ophthalmol. 2004;138(4):527-35.
6. Kymes SM, Walline JJ, Zadnik K, et al. Changes in the quality-of-life of people with keratoconus. Am J Ophthalmol. 2008;145(4):611-7.
7. Godefrooij DA, de Wit GA, Uiterwaal CS, et al. Age-specific incidence and prevalence of keratoconus: a nationwide registration study. Am J Ophthalmol. 2017;175:169-72.
8. Wollensak G, Spoerl E, Seiler T. Riboflavine/ultraviolet-a-geïnduceerde collageen crosslinking voor de behandeling van keratoconus. Am J Ophthalmol 2003;135(5):620-7.
9. Schumacher S, Mrochen M, Wernli J, et al. Optimalisatiemodel voor UV-riboflavine corneale cross-linking. Invest Ophthalmol Vis Sci. 2012;53(2):762-9.
10. Chang CY, Hersh PS. Corneal collagen cross-linking: a review of 1-year outcomes. Eye Contact Lens. 2014;40(6):345-52.
11. Hersh PS, Stulting RD, Muller D, et al. United States multicenter clinical trial of corneal collagen crosslinking for keratoconus treatment. Ophthalmology. 2017;124(9):1259-70.
12. Hersh PS, Stulting RD, Muller D, et al. Amerikaanse multicenter klinische trial van corneale collageen crosslinking voor de behandeling van corneale ectasie na refractieve chirurgie. Ophthalmology. 2017;124(10):1475-84.
13. Raiskup F, Theuring A, Pillunat LE, Spoerl E. Corneal collagen crosslinking with riboflavin and ultraviolet-a light in progressive keratoconus: ten-year results. J Cataract Refract Surg. 2015;41(1):41-6.
14. Spoerl E, Mrochen M, Sliney D, Trokel S, Seiler T. Veiligheid van UVA-riboflavine cross-linking van de cornea. Cornea. 2007 May;26(4):385-9.
15. Schumacher S, Mrochen M, Wernli J, et al. Optimalisatiemodel voor UV-riboflavine corneale cross-linking. Invest Ophthalmol Vis Sci. 2012;53(2):762-9.
16. Bottós KM, Schor P, Dreyfuss JL, et al. Effect of cornea epithelium on ultraviolet-a and riboflavin absorption. Arq Bras Oftalmol. 2011;74(5):348-51.
17. Richoz O, Hammer A, Tabibian D, et al. Het biomechanische effect van corneale collageen cross-Linking (CXL) met riboflavine en UV-A is zuurstofafhankelijk. Transl Vis Sci Technol. 2013;2(7):6.
18. Padmanabhan P, Rachapalle Reddi S, Rajagopal R, et al. Corneal collagen cross-linking for keratoconus in pediatric patients-long-term results. Cornea. 2017;36(2):138-43.
19. Naderan M, Jahanrad A. Topografische, tomografische en biomechanische veranderingen van het hoornvlies tijdens de zwangerschap bij patiënten met keratoconus: een cohortstudie. Acta Ophthalmol. 2017;95(4):e291-e296.
20. Sandvik GF, Thorsrud A, Råen M, et al. Does corneal collagen cross-linking reduce the need for keratoplasties in patients with keratoconus? Cornea. 2015;34(9):991-5.
21. Gomes JA, Tan D, Rapuano CJ, et al. Wereldwijde consensus over keratoconus en ectatische aandoeningen. Cornea. 2015;34(4):359-69.
22. Nordström M, Schiller M, Fredriksson A, Behndig A. Refractieve verbeteringen en veiligheid met topografie-geleide corneale crosslinking voor keratoconus: 1-jarige resultaten. Br J Ophthalmol. 2017;101(7):920-5.
23. Yildiz EH, Diehl GF, Cohen EJ, et al. Demographics of patients older than 50 years with keratoconus. Eye Contact Lens. 2009;35(6):309-11.
24. Mazzotta C, Hafezi F, Kymionis G, et al. In vivo confocale microscopie na corneale collageen crosslinking. Ocul Surf. 2015;13(4):298-314.
25. Cınar Y, Kürs¸at Cingü A, Turkcu FM, et al. Versnelde corneale collageen cross-linking voor progressieve keratoconus. Cutan Ocul Toxicol. 2014;33:168-71.
26. Kanellopoulos AJ. Lange termijn resultaten van een prospectieve gerandomiseerde bilaterale oog vergelijkingsstudie van hogere fluentie, kortere duur ultraviolet a straling, en riboflavine collageen cross linking voor progressieve keratoconus. Clin Ophthalmol. 2012;6:97-101.
27. Cummings AB, McQuaid R, Naughton S, et al. Optimizing corneal cross-linking in the treatment of keratoconus: a comparison of outcomes after standard- and high-intensity protocols. Cornea. 2016;35(6):814-22.
28. Vinciguerra P, Albè E, Trazza S, et al. Refractive, topographic, tomographic, and aberrometric analysis of keratoconic eyes undergoing corneal cross-linking. Ophthalmology. 2009;116(3):369-78.
29. Kim BZ, Jordan CA, McGhee CN, Patel DV. Natural history of corneal haze after corneal collagen crosslinking in keratoconus using Scheimpflug analysis. J Cataract Refract Surg. 2016;42(7):1053-9.
30. Wollensak G, Iomdina E. Biomechanische en histologische veranderingen na corneale crosslinking met en zonder epitheliaal debridement. J Cataract Refract Surg. 2009;35(3):540-6.
31. Caporossi A, Mazzotta C, Paradiso AL, et al. Transepithelial corneal collagen crosslinking for progressive keratoconus: 24-month clinical results. J Cataract Refract Surg. 2013;39(8):1157-63.
