Clinicienii au fost mult timp frustrați de rolul disproporționat pe care presiunea intraoculară (PIO) îl joacă în îngrijirea glaucomului. Fiind singurul factor susceptibil de intervenție medicală sau chirurgicală, rolul său este vital. Cu toate acestea, tonometria este în mod inerent limitată: O singură citire efectuată la câteva luni nu reușește să descrie fluxul și refluxul diurn al PIO. Chiar și aducerea pacienților pentru mai multe citiri tonometrice nu oferă o imagine ideală a caracteristicilor PIO ale pacientului.

|
|
| Acest senzor micro-fluidic implantabil de monitorizare a PIO pe 24 de ore este în prezent în curs de dezvoltare la Universitatea Stanford. Foto: Ishmail E. Araci |
Experții cred că, în cele din urmă, le veți monta pacienților un senzor minuscul adăpostit pe o lentilă de contact sau pe o pereche de ochelari, sau îi veți trimite la un oftalmolog pentru a li se implanta unul în ochi. Acesta ar măsura continuu PIO, crescând exponențial cantitatea – și, sperăm, valoarea – datelor pe care le primiți. Dacă abordarea actuală a documentării PIO este ca și cum ar fi o fotografie instantanee, monitorizarea continuă a PIO timp de 24 de ore se aseamănă mai mult cu capturarea unui videoclip care înregistrează schimbările în timp, în loc să ofere doar o citire statică.
Aceste gadgeturi sunt încă în curs de dezvoltare. Sunt ele pregătite pentru ora de vârf? Să aruncăm o privire asupra modului în care fluctuează PIO, a provocărilor clinice pe care le creează și a tehnologiilor actuale de ultimă generație care încearcă să urmărească mai bine PIO pentru a permite o mai bună înțelegere clinică.
O țintă în mișcare
Stabilirea unui plan de tratament bazat pe atingerea unei PIO țintă este complicată atunci când ținta însăși este în mișcare. PIO fluctuează pe parcursul zilei – de la oră la oră, de la minut la minut, chiar și de la secundă la secundă – pe baza unei varietăți de factori endogeni și exogeni.
În cadrul sistemului ocular, PIO poate depinde de echilibrul dintre producția de umoare apoasă, ușurința de ieșire (cât de ușor părăsește umoarea apoasă ochiul), presiunea venoasă episclerală (presiunea din venele de la suprafața ochiului) și ieșirea uveosclerală (o cale secundară prin care umoarea apoasă părăsește ochiul).
De exemplu, o creștere a facilității de ieșire sau o scădere a producției de umor apos ar scădea PIO, spune Arthur J. Sit, MD, cercetător în domeniul glaucomului la Clinica Mayo din Rochester, Minn. Salturile pe termen scurt ale PIO pot apărea, de asemenea, din cauza presiunii asupra ochiului din cauza clipitului sau frecării ochiului sau chiar în timpul mișcării oculare sau a pulsațiilor tensiunii arteriale.
Presiunea intraoculară fluctuează, de asemenea, din cauza poziției corpului, a momentului zilei (vârfuri pe timp de noapte, depresiuni în timpul zilei), a tensiunii arteriale și a conceptului aferent de presiune de perfuzie oculară (OPP), a nivelului de stres sau de durere, a consumului de apă și cofeină.
În plus, activitatea viguroasă și stresul pot face ca tensiunea arterială, PIO și OPP să atingă cote maxime, spune Kaweh Mansouri, MD, MPH, oftalmolog la Universitatea din Geneva și la Universitatea din Colorado Denver. Măsurarea tensiunii arteriale împreună cu PIO are valoare pentru a determina modul în care tensiunea arterială afectează PIO, spune Dr. Mansouri. Cercetătorii folosesc în prezent dispozitive de monitorizare a PIO timp de 24 de ore pentru a explora aceste efecte asupra progresiei glaucomului.
|
Dos and Don’ts of IOP Measurement Nu diagnosticați sau tratați după o singură măsurătoare. Dr. Sowka îi sfătuiește pe optometriști să nu înceapă imediat tratamentul decât dacă presiunea este excesiv de mare sau dacă nervii optici sunt deja grav afectați și vulnerabili; în schimb, măsurați presiunea de mai multe ori. De asemenea, este o idee bună să obțineți mai multe măsurători ale presiunii după inițierea tratamentului pentru a determina dacă medicația funcționează, spune Dr. Sowka. O singură citire a PIO după începerea unui medicament este într-adevăr insuficientă pentru a judeca adevărata eficacitate. Spuneți-le pacienților să se relaxeze. Așa cum am menționat mai devreme, pacienții se pot încorda sau își pot ține respirația în timpul tonometriei. Spuneți-le în mod regulat să se relaxeze și să respire normal în timpul procesului, îndeamnă Dr. Mansouri. Nu renunțați la suspiciune. Dacă măsurătorile PIO ale pacientului nu par să se potrivească cu evaluările dvs. ale câmpului vizual și ale nervului optic, este posibil să se întâmple mai multe lucruri cu PIO a pacientului decât v-ați dat seama, spune Dr. Hartwick. Cereți-i să revină și să își măsoare PIO la un alt moment al zilei, adaugă el. Luați în considerare o curbă diurnă la anumiți pacienți. Înregistrarea tonometrică a unei curbe diurne este nepractică și plictisitoare pentru majoritatea pacienților. Dar dacă nivelul PIO și gradul de afectare par incongruente – de exemplu, când suspectați un glaucom de tensiune normală – luați în considerare această posibilitate, spune Dr. Davey. Dacă pacientul este de acord, aduceți-l dimineața devreme și înregistrați PIO la fiecare oră timp de opt până la 10 ore. „Acest lucru vă oferă curba diurnă de la birou, care s-ar putea să nu fie pe deplin reprezentativă pentru valorile de zi/noapte, dar cel puțin vă oferă mai mult de o măsurătoare”, spune el. |
Iată cum aceste variabile afectează PIO:
– Poziția corpului. În funcție de poziția pacientului pe scaun, presiunea poate crește sau scădea. De exemplu, PIO este cea mai mică atunci când pacientul este așezat într-o poziție neutră. „Aproape orice altceva face ca PIO să crească, inclusiv aplecarea gâtului în față, aplecarea capului în spate, întoarcerea capului într-o parte, culcarea, aplecarea, clipitul sau frecarea ochilor”, spune Dr. Sit.
– Consumul de apă. Consumul unui volum mare de apă face ca volumul de sânge al pacientului să crească pentru o perioadă scurtă de timp. Presiunea venoasă crește, de asemenea, atunci când pacientul consumă mai multă apă. „Tot ce trebuie să facă este să consume între 16 și 32oz, ceea ce reprezintă una sau două sticle mici de apă, și în cinci minute presiunea va crește cu 6 mm Hg”, spune Pinakin Gunvant Davey, PhD, OD, profesor și expert în glaucom la Colegiul de Optometrie de la Western University of Health Sciences din Pomona, California.
– Momentul din zi. Literatura de specialitate a arătat că vârful PIO apare noaptea la două treimi dintre pacienți. Motivul: substanța apoasă este sub-secretată noaptea, spune Joseph Sowka, OD, profesor de optometrie la Nova Southeastern University College of Optometry din Ft. Lauderdale, Florida.
De exemplu, Dr. Mansouri a observat pacienții timp de 24 de ore în laboratoarele de somn și a constatat că cele mai mari PIO au fost înregistrate noaptea. Chiar dacă pacienții dvs. nu vor fi supuși unor studii de somn, este posibil ca ei să vină la cabinetul dvs. seara – dacă este așa, așteptați-vă să vedeți PIO-uri ridicate în raport cu alte momente ale zilei.
– Tensiunea arterială. IOP de bază se bazează pe ciclul cardiac, tensiunea arterială sistolică și diastolică. Forța folosită pentru a aduce sângele în ochi este presiunea de perfuzie oculară, explică James L. Fanelli, OD, de la Cape Fear Eye Institute din Wilmington, NC.
Dacă tensiunea arterială este scăzută, există mai puțină forță pentru a „împinge” sângele în ochi și, prin urmare, mai puțină presiune de perfuzie la nivelul ochiului. Factorii care determină creșterea PIO vor avea un efect asupra scăderii presiunii de perfuzie, iar factorii care scad tensiunea arterială vor duce, de asemenea, la scăderea presiunii de perfuzie – sau o combinație a oricăruia dintre acești factori poate juca un rol, spune Dr. Fanelli. Tensiunea arterială tinde să scadă în timpul orelor de somn, la primele ore ale dimineții, care este, de asemenea, momentul din zi în care PIO tinde să fie cel mai ridicat.1 Acești doi factori opuși pot avea un efect duplicitar în reducerea PPO în timpul orelor nocturne, ceea ce poate permite o deteriorare mai mare a capului nervului ocular.
– Stresul. O creștere sau o scădere a stresului determină modificări hormonale care împing nivelul PIO în sus sau în jos. Unul dintre pacienții doctorului Mansouri – studiat cu ajutorul unui senzor de monitorizare a PIO pe 24 de ore pe o lentilă de contact – avea vârfuri de presiune ori de câte ori câinele ei avea crize epileptice noaptea.
– „Nervi” generali. Este posibil ca, la unii pacienți, stresul provocat de examenul oftalmologic în sine – de exemplu, dacă sunt îngrijorați că vor fi diagnosticați cu glaucom – să determine creșterea PIO, spune Andrew Hartwick, OD, PhD, profesor asociat la Ohio State University College of Optometry din Columbus. De exemplu, aceștia își pot strânge ochii pentru că sunt stresați în legătură cu examenul, iar valorile PIO cresc brusc.
– Durerea cauzează, de asemenea, creșteri bruște ale PIO, deoarece provoacă stres. Una dintre pacientele doctorului Mansouri s-a lovit rău la picior într-o parcare. A existat un vârf în nivelul PIO în momentul exact în care și-a amintit că a avut loc accidentul, conform datelor de monitorizare pe 24 de ore.
Consecințele citirilor inexacte ale PIO
Studiile au indicat că vârfurile PIO ar putea contribui la progresia glaucomului.2,3 Dar dacă examinați un pacient atunci când PIO este la cel mai scăzut sau cel mai ridicat nivel, este posibil să supraestimați sau să subestimați diagnosticul de glaucom sau tratamentul necesar pentru pacient.
„Dacă surprindem un pacient la o depresiune, unde PIO este cea mai scăzută, ne poate îndepărta de la luarea în considerare a glaucomului”, mai ales dacă citirea se încadrează într-un interval normal din punct de vedere statistic, spune Dr. Sowka. „Alteori, îl putem prinde la un vârf al PIO, unde este puțin peste normal – un scenariu care tinde să îi facă pe practicieni să se îngrijoreze inutil.”
|
|
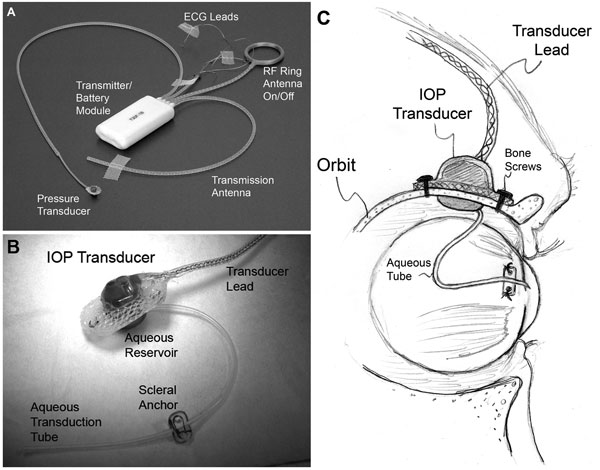
| (A) Un sistem tipic de implant total T30F (Konigsberg Instruments). (B) Suprafața extraorbitală a carcasei transductorului IOP personalizat. (C) Un tub de silicon de calibru 23 livrează lichidul apos din camera anterioară către un rezervor de lichid de pe partea intraorbitală a transductorului (parțial ascuns la vedere în B); Tubul (cu un joc adecvat pentru a permite mișcarea ochiului) a fost tăiat și introdus în camera anterioară. |
Înregistrarea unui interval de PIO ar permite, potențial, îmbunătățirea diagnosticului și a managementului glaucomului. „Dacă cercetătorii ar putea demonstra că anumite modele de PIO pe 24 de ore sunt legate de progresia glaucomului, atunci există speranța că detectarea acestor modele ar putea ajuta la identificarea pacienților cu risc crescut de progresie și ne-ar permite să le adaptăm tratamentul în consecință”, spune Dr. Mansouri.
Glaucomul ar putea fi identificat mai devreme, permițând începerea mai rapidă a intervenției chirurgicale sau a tratamentului medicamentos, adaugă el. Medicii oftalmologi ar putea, de asemenea, să determine dacă medicamentele pentru scăderea PIO sunt eficiente pe timp de noapte sau în timpul unor activități specifice care cresc PIO.
Stabilirea unui interval real al PIO ar necesita o monitorizare continuă a PIO timp de 24 de ore. Aceasta este o provocare, deoarece o singură măsurătoare a PIO colectată în timpul orelor normale de consultație nu surprinde intervalul de PIO al unui pacient, vârfurile sale sau schimbările din timpul zilei.4
În momentul de față, determinarea intervalului de PIO este posibilă folosind tonometria de aplanație Goldman (GAT) prin intermediul unei curbe de tensiune diurnă (DTC), în care citirile PIO sunt capturate la diferite momente de timp în timpul orelor de consultație. Dar acest lucru este problematic atât pentru practician, cât și pentru pacient. Curbele nocturne nu sunt înregistrate și mai puțin de 1% dintre pacienți sunt supuși DTC sau monitorizării PIO într-un laborator de somn.4
De fapt, cercetătorii au măsurat PIO timp de 24 de ore și au documentat nu numai că PIO atinge vârfuri nocturne, ci și că fluctuația PIO a fost mult mai mare în afara orelor de consultație.5 Într-un studiu efectuat pe 35 de pacienți a căror PIO a fost înregistrată cu ajutorul unui pneumatonometru într-un laborator de somn timp de 24 de ore, cele mai multe vârfuri ale PIO au fost înregistrate noaptea la pacienții cu glaucom mai în vârstă în comparație cu persoanele sănătoase, indiferent dacă erau așezate sau întinse.6
Mai recent, cercetătorii care au folosit monitorizarea pe 24 de ore au aflat că PIO medie nu numai că crește noaptea, dar de fapt crește în mod constant – și mai mult în timpul zilei decât noaptea.7 Cercetătorii de la Devers Eye Institute din Portland, Oregon, au folosit un sistem de telemetrie implantat în ochii maimuțelor pentru a înregistra 500 de măsurători ale PIO pe secundă.
Ei au descoperit că PIO fluctuează mult mai mult decât se credea anterior. „Clipirile și mișcările ochilor generează vârfuri mari de PIO care apar de aproximativ 12.000 de ori pe oră și constituie aproximativ 12% din energia totală a PIO pe care ochiul trebuie să o absoarbă în timpul orelor de veghe”, au constatat cercetătorii. Aceștia cred că aceste date la maimuțe vor fi aproximativ aceleași și la oameni. „PIO trebuie privită acum ca fiind dinamică și în continuă schimbare, iar fluctuațiile PIO se pot dovedi a fi un factor important care contribuie la glaucom. „8
Ei au constatat, de asemenea, că ciclul diurn nu se repetă de la o zi la alta. De aici necesitatea unei monitorizări continue a PIO. Prototipurile actuale includ senzori implantați și dispozitive bazate pe lentile de contact.
Inteligent Implantables
Câteva companii start-up au dezvoltat senzori telemetrici de presiune care pot fi implantați în timpul operației de cataractă sau glaucom. „Telemetric înseamnă că citirile de presiune sunt captate de la distanță (adică din interiorul ochiului) și transmise fără fir către un cititor extern”, spune Dr. Sit.
Dispozitivele implantabile studiate în prezent includ:

|
||
|
Senzorul Pro-IOP este un dispozitiv telemetric care este implantat ca o IOL. Foto: Implandata Ophthalmic Products GmbH |
– Pro-IOP. Compania germană Implandata Ophthalmic Products lucrează la Pro-IOP, un transductor de presiune intraoculară fără fir (WIT) care este alimentat telemetric de un dispozitiv portabil. Semănând cu un mic inel de plastic, WIT măsoară 11,3 mm în diametru.9 Acesta încorporează senzori de presiune, un senzor de temperatură, un codificator de identificare, un codificator analog-digital și o unitate de telemetrie într-un singur sistem microelectromecanic.9
Un cip RFID cu o antenă încorporată transmite citirile IOP de 24 de ore către un cititor portabil extern. Pacientul și medicul pot avea, de asemenea, în cele din urmă, posibilitatea de a primi datele prin intermediul unei aplicații pentru smartphone. Pacientul ar putea, de asemenea, să comunice cu medicul cu privire la citirile PIO pe aplicație.
Dispozitivul nu a primit încă marcajul CE în Europa sau aprobarea FDA în SUA, dar cercetătorii din Germania au introdus recent Pro-IOP în primul subiect uman, o femeie în vârstă de 60 de ani; încă nu au fost publicate date.9
– AcuMEMs. Un dispozitiv implantabil în curs de dezvoltare de către o companie americană cu același nume, AcuMEMs funcționează în mod similar cu Pro-IOP. Senzorul este un senzor de presiune capacitiv care își schimbă forma în funcție de fluctuațiile IOP. „Când își schimbă forma, capacitatea electrică este modificată, iar acest lucru poate fi detectat în exterior cu ajutorul cititorului”, spune Dr. Sit.
Senzorul poate fi implantat în camera anterioară ca o procedură de sine stătătoare sau ca parte a operației de glaucom; de asemenea, poate fi introdus în sacul capsular în timpul operației de cataractă.
– Implant IOL microfluidic. Cercetătorii de la Universitatea Stanford și de la Universitatea Bar-Ilan din Israel dezvoltă împreună un senzor microfluidic implantabil. PIO ar fi măsurată „pe baza unei interfețe de presiune de echilibru stabilită între un lichid intraocular și un gaz” conținute în camerele din senzor, conform brevetului dispozitivului. Pacienții și medicii ar putea folosi smartphone-urile lor sau un cititor extern pentru a-și verifica PIO.10 Inventatorii așteaptă aprobarea brevetului pentru senzor.
Semnalul transmis de dispozitivele implantate în ochi poate fi mai precis decât cele atașate la lentilele de contact, în teorie, spune Dr. Davey. Puterea semnalului depinde de cantitatea de energie pe care o emite dispozitivul. „Am implantat ambele dispozitive (Pro-IOP și AcuMEMs) și nu au funcționat atât de bine”, spune Dr. Davey.
Atât cititoarele Pro-IOP, cât și cele AcuMEMs ar putea fi eventual atașate la o pereche de ochelari, iar datele ar fi colectate în același mod, spune Dr. Sit.
Lentile de contact inteligente
Cercetătorii au investigat pentru prima dată senzorii pentru lentile de contact în anii 1970, dar lentilele de contact dure disponibile erau prea incomode și modificau integritatea structurală a ochiului pacientului, potrivit Dr. Davey.
|
|
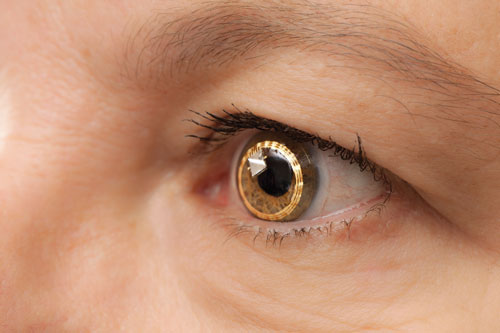
| Sensimed Triggerfish pe ochi. Este încă în curs de testare clinică în SUA. |
Senzorii nu au fost, de asemenea, suficient de sensibili. „Persoana cu un ochi mai „moale” a avut citiri mai precise decât o persoană cu un ochi mai rigid”, spune Dr. Davey. „Tehnologia nu era suficient de bună pentru a obține valori IOP”. O cornee mai groasă răspunde mai puțin ușor la modificările PIO, făcând tonometria (și senzorii pentru lentile de contact) mai puțin precisă.
Senzorii PIO pe bază de lentile de contact includ:
– The Triggerfish (Sensimed). La Universitatea din Geneva, Elveția, oftalmologii au efectuat primele cercetări ale unei lentile de contact denumite Triggerfish, conduse de Dr. Mansouri și alții.
The Triggerfish este o lentilă de contact moale hidrofilă dotată cu un senzor pentru lentile de contact (CLS). CLS are două tensiometre amplasate în jurul limbusului care detectează schimbările în circumferința oculară. „Se crede că aceste modificări ale circumferinței oculare sunt legate de modificările PIO și ale volumului intraocular, iar acest lucru a fost dovedit în cazul ochilor enucleați”, spune Dr. Mansouri. Dispozitivul măsoară un amestec de PIO, volum intraocular și modificări ale proprietăților biomecanice (o combinație de histerezis și rigiditate corneală și sclerală) care se corelează cu fluctuațiile PIO. Un cititor extern captează datele pe o perioadă de 24 de ore.
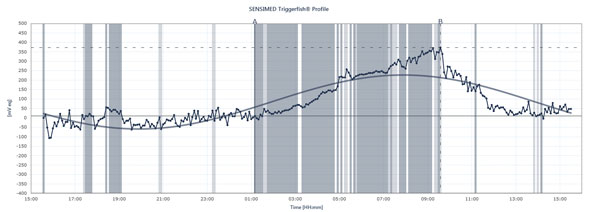
Diagrama de flux arată vârfurile și coborâșurile PIO la un pacient care poartă Sensimed Triggerfish pe o perioadă de 24 de ore.
Triggerfish este omologat cu marcaj CE în Europa. Aprobarea FDA nu a fost obținută în SUA, iar dispozitivul este încă în curs de testare clinică.
|
Triggerfish urmărește diferit IOP Datele afișate pe cititorul extern sunt o combinație de presiune intraoculară, volum intraocular și proprietăți biomecanice ale ochiului, explică Dr. Mansouri. „Este util pentru a vă da o idee despre schimbările calitative pe parcursul a 24 de ore mai mult decât despre schimbările cantitative, deoarece nu le putem traduce în milimetri de mercur”, spune el. Peștele declanșator oferă totuși informații valoroase. Studiile viitoare care utilizează dispozitivul ar putea ajuta să explice cât de instabilă sau stabilă a fost presiunea pe parcursul a 24 de ore, când apar vârfurile de PIO pe timp de noapte, cum introducerea unui tratament sau a unor modificări de tratament afectează modelele de PIO pe 24 de ore și cum afectează activitățile specifice modelele de PIO pe 24 de ore, cum ar fi pozițiile de yoga, consumul de cofeină, situațiile stresante și alte cauze ale vârfurilor de PIO descrise mai sus. Dr. Mansouri face, de asemenea, ca pacienții cu glaucom normal sau cu tensiune scăzută să fie supuși unei monitorizări simultane a tensiunii arteriale de 24 de ore și a PIO de 24 de ore, deoarece vârfurile pot afecta OPP. Dar va arăta Triggerfish o corelație între modelele de PIO de 24 de ore și evoluția glaucomului? Multe studii sunt în curs de desfășurare pentru a răspunde la această întrebare esențială.
|
– Lentile de contact cu senzor cu circuit de rezonanță. Un alt dispozitiv inteligent CLS în curs de dezvoltare este un circuit de rezonanță alcătuit dintr-un condensator cu peliculă subțire combinat cu o bobină senzorială care detectează deformarea curburii corneei. Acesta se află în primele etape de dezvoltare sub conducerea lui David C.C. Lam de la Departamentul de Inginerie Mecanică și Aerospațială de la Universitatea de Știință și Tehnologie din Hong Kong.
Într-un studiu din septembrie 2014, CLS a fost testat pe un model de ochi din cauciuc siliconat. S-a constatat că senzorul a urmărit cu acuratețe fluctuațiile PIO.11
Ca și cum ar fi măsurarea nivelului de glucoză o dată pe zi pentru pacienții cu diabet sau a tensiunii arteriale o dată pe zi pentru pacienții cu boli de inimă, încrederea într-o singură măsurare a PIO ar putea duce la date eronate privind PIO. Dar poate că, într-un viitor nu prea îndepărtat, dispozitive desprinse parcă dintr-un film SF – lentile de contact și senzori implantabili – v-ar putea permite să urmăriți PIO cu mai multă înțelegere și cu mai puține bătăi de cap pentru dumneavoastră și pentru pacienții dumneavoastră.
1. Liu JH1, Gokhale PA, Loving RT, Kripke DF, Weinreb RN. Evaluarea de laborator a presiunilor de perfuzie oculară diurnă și nocturnă la om. J Ocul Pharmacol Ther. 2003 Aug;19(4):291-7.
2. Zeimer RC, Wilensky JT, Gieser DK, Viana MA. Asocierea dintre vârfurile de presiune intraoculară și progresia pierderii câmpului vizual. Ophthalmology. 1991 Jan;98(1):64-69.
3. Konstas AG, Quaranta L, Mikropoulos DG, et al. Peak Intraocular Pressure and Glaucomatous Progression in Primary Open-Angle Glaucoma. J Ocul Pharmacol Ther. 2012 Feb;28(1):26-32.
4. Mansouri K, Weinreb RN, Medeiros FA. Este necesară monitorizarea presiunii intraoculare de 24 de ore în glaucom? Semin Opthalmol. Mai 2013: 28(3):157-164.
5. Barkana Y, Anis S, Liebmann J, Tello C, Ritch R. Utilitatea clinică a monitorizării presiunii intraoculare în afara orelor normale de consultație la pacienții cu glaucom. Arch Ophthalmol. 2006 Jun;124(6):793-7.
6. Mosaed S, Liu H, Weinreb RN. Corelația dintre presiunile intraoculare nocturne maxime la subiecții sănătoși și pacienții cu glaucom. Am J Ophthalmol. 2005; Feb;139(2):320-4.
7. Downs JC, Burgoyne CF, Seigfreid WP, et al. 24-hour IOP telemetry in the nonhuman primate: implant system performance and initial characterization of IOP at multiple timescales. Invest Ophthalmol Vis Sci. 2011 Sep 21;52(10):7365-75.
8. Association for Research in Vision and Ophthalmology: Tendințe emergente și subiecte fierbinți. Prezentat luni, 5 mai 2014, la reuniunea anuală a ARVO. Disponibil la: www.arvo.org/About_ARVO/Press_Room/Emerging_Trends_and_hot_topics__Presented_Monday,_May_5_at_the_ARVO_Annual_Meeting. Accesat la 19 noiembrie 2014.
9. Melki S, Todani A, Cherfan G. An Implantable Intraocular Pressure Transducer Initial Safety Outcomes. JAMA Ophthalmol. 2014 Oct 1;132(10):1221-5.
10. Mandel Y, Araci IE, Quake SR. Google Patents. Dispozitiv micro-fluidic implantabil pentru monitorizarea presiunii intraoculare. Disponibil la: www.google.com/patents/WO2014137840A1?cl=en. Accesat la 17 octombrie 2014.
11. Chen GZ, Chan IS, Chan IS, Leung LK, Lam DC. Senzor de lentilă de contact moale portabilă pentru monitorizarea continuă a presiunii intraoculare. Med Eng Phys. 2014 Sep;36(9):1134-9.
12. Mottet B, Aptel F, Romanet JP, et al. 24-hour intraocular pressure rhythm in young healthy subjects evaluated with continuous monitoring using a contact lens sensor. JAMA Ophthalmol. 2013 Dec;131(12):1507-16.
