- o-Xileno Propiedades Químicas,Usos,Producción
- Xileno
- Destilación de precisión para la separación de O-xileno y p-xileno
- Propiedades químicas
- Usos
- Método de producción
- Categoría
- Grado de toxicidad
- Toxicidad aguda
- EXPLOSIVOS y CARACTERÍSTICAS PELIGROSAS
- Inflamabilidad y características peligrosas
- Características de almacenamiento y transporte
- Agente extintor
- Normativa laboral
- Propiedades químicas
- Propiedades físicas
- Usos
- Definición
- Referencia(s) de síntesis
- Descripción general
- Aire &Reacciones en el agua
- Perfil de reactividad
- Peligro para la salud
- Peligro de incendio
- Reactividad química
- Perfil de seguridad
- Fuente
- Fato ambiental
- Métodos de purificación
o-Xileno Propiedades Químicas,Usos,Producción
Xileno
El xileno se refiere al hidrocarburo aromático con los dos átomos de hidrógeno del anillo de benceno sustituidos por dos grupos metilo. Tiene tres isómeros: o-xileno (1, 2-dimetilbenceno), m-xileno y p-xileno. Los productos industriales son las mezclas de los tres isómeros con un 10% de o-, un 70% de m- y un 20% de p-. En la industria de la coquización, es uno de los productos refinados del benceno crudo.
El xileno es un tipo de líquido inflamable incoloro; el punto de fusión del o-, m- y p-xileno es de 25,2 ℃,-47,9 ℃ y 13,3 ℃; los puntos de ebullición son, respectivamente, 144.4 ℃, 139,1 ℃ y 138,3 ℃, mientras que la densidad relativa es de 0,8802, 0,8642 y 0,8611, respectivamente; no es soluble en agua pero es miscible con muchos tipos de disolventes orgánicos inmiscibles. Tras la oxidación catalítica, generan respectivamente anhídrido ftálico, ácido isoftálico y ácido tereftálico.
El xileno es un tipo de materia prima importante de los productos químicos orgánicos, que existe de forma natural en el alquitrán de hulla y en algunos tipos de petróleo. Puede obtenerse a través del fraccionamiento de la parte de aceite ligero del alquitrán de hulla o del reformado catalítico de la gasolina ligera. La industria realiza principalmente la extracción utilizando la fracción C8 en los reformados de nafta. También se puede fabricar mediante la reacción de desproporción del tolueno en presencia de un catalizador y a alta temperatura y presión. En la actualidad, la industria aplica principalmente el método de cristalización criogénica, adsorción y formación de complejos o tamices moleculares para separarlos. El O-xileno tiene un punto de ebullición relativamente alto, pudiendo separarse mediante destilación. El p-xileno también tiene un punto de fusión alto y puede purificarse mediante purificación por cristalización fraccionada. El xileno mixto sin separación puede utilizarse directamente como disolvente, pudiendo complementar la gasolina para mejorar las propiedades antiexplosivas. Son componentes de la gasolina de aviación. El o-xileno se utiliza principalmente para la preparación de anhídrido ftálico, que es una importante materia prima para la fabricación de diversos tintes e indicadores (como la fenolftaleína). Además, el o-xileno también puede utilizarse para la preparación de resina de poliéster, repelente de insectos, plastificantes y tintes. El M-xileno, a través de la nitración y la reducción, puede generar 4, 6-dimetil-1, 3-fenilendiamina que es el intermedio para los tintes sintéticos. El M-xileno también puede utilizarse como materia prima para fragancias sintéticas (como el almizcle de xileno). El P-xileno se utiliza principalmente en la fabricación de ácido tereftálico, que es una importante materia prima para la fibra de poliéster sintética (poliéster).
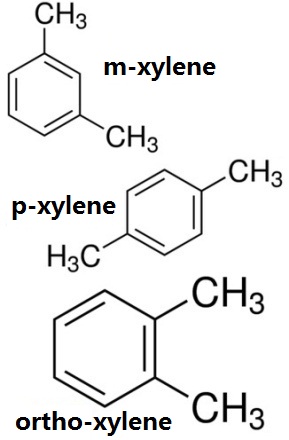
Figura 1 la estructura química de los tres isómeros del xileno, orto-xileno, m-xileno, p-xileno estructura química.
La información anterior está editada por Chemicalbook.
Destilación de precisión para la separación de O-xileno y p-xileno
El xileno se presenta en el benceno crudo cocido y en el aceite craqueado de petróleo. El benceno crudo, después de la destilación inicial, el lavado con ácido sulfúrico y la destilación para la separación del benceno y el tolueno, seguido de la destilación, podemos obtener xileno, también conocido como xileno coquizado. La calidad del xileno coquizado depende de la capacidad de separación de la columna de destilación, de la temperatura en la parte superior de la columna y de la relación de reflujo. China ha clasificado los productos de xileno de coque en tres niveles. El xileno de coque contiene generalmente un 16% de o-xileno, un 50% de m-xileno, un 21% de p-xileno y un 7% de etilbenceno. El xileno producido en la industria petrolera tiene un bajo contenido de m-xileno y un alto contenido de etilbenceno. El xileno industrial no sólo es el disolvente y el aditivo de la industria del caucho y los revestimientos, sino también los aditivos del combustible para la aviación y la energía. El O-xileno, el m-xileno y el p-xileno separados del xileno industrial son las materias primas del ácido ftálico, el ácido isoftálico y el ácido tereftálico, respectivamente. El ácido ftálico y el ácido tereftálico se utilizan en la producción de plastificantes, resinas de poliéster y fibras de poliéster. El M-xileno puede utilizarse solo como disolvente y como aditivo para combustibles. El o-xileno contenido en el xileno industrial tiene una diferencia de más de 5,2 ℃ con otros isómeros. Con la destilación de precisión, podemos obtener o-xileno con una pureza de más del 95%, seguido por el uso de la sulfonación y la destilación para la purificación por lo que podemos obtener o-xileno más puro.
El xileno pertenece a las bases de Lewis, que pueden formar un complejo polar con HF-BF3 (ácido de Lewis). La alcalinidad del M-xileno es unas 100 veces más fuerte que la de otros aromáticos C8. Cuando la mezcla de isómeros de xileno entra en contacto con el disolvente HF-BF3, el m-xileno puede formar un complejo con el fluoruro y se extrae preferentemente en la fase fluorada. La fase fluorada que contiene m-xileno se calienta a una presión más baja para descomponer el complejo, separando así el m-xileno de la mezcla. El disolvente HF-BF3 puede recuperarse por destilación para su reciclaje. Si la materia prima es una mezcla de ortoxileno, m-xileno y p-xileno, después de extraer el m-xileno, podemos seguir utilizando la destilación de precisión para separar el o-xileno y el p-xileno.
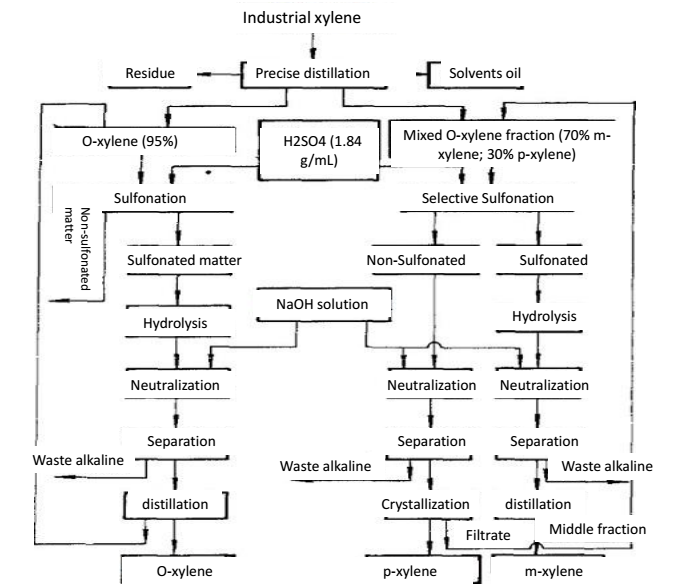
Figura 2 el método de destilación de precisión para la separación de o-xileno y p-xileno.
Propiedades químicas
Se presenta como un líquido transparente incoloro con olor aromático. Es miscible con etanol, éter etílico, acetona y benceno pero insoluble en agua.
Usos
(1) Se utiliza principalmente en la producción de anhídrido ftálico
(2) El O-xileno es la materia prima para la producción del germicida fenramina, el péptido tetraclorofenilo y el herbicida bensulfurón-metilo. Se utiliza como intermedio para la fabricación de ácido o-metil benzoico.
(3) Se utiliza principalmente como materia prima química y disolvente. Puede utilizarse para producir anhídrido ftálico, tintes, pesticidas y medicamentos, como las vitaminas. También se puede utilizar como aditivo para la gasolina de aviación.
(4) Se utiliza como estándares cromatográficos y disolventes
(5) Como materia prima de síntesis de anhídrido y otras síntesis orgánicas;
Método de producción
La industria aplicó el método de superdestilación para separar el o-xileno del xileno mixto. El o-xileno tiene una diferencia de más de 5 ℃ en el punto de ebullición en comparación con otros componentes del xileno mixto. Para la destilación, el número de bandejas necesario es de unos 150; la relación de reflujo es de 5-8 y consume relativamente mucha energía.
El o-xileno se producía originalmente sobre todo a partir del alquitrán de hulla. En la actualidad, la mayor parte de la producción nacional y extranjera de o-xileno se realiza principalmente mediante la extracción del reformado catalítico del petróleo y el craqueo térmico del hidrocarburo aromático. Debido a que las estructuras del o-xileno, el p-xileno y el m-xileno en el xileno son muy similares, sus parámetros físicos también son bastante parecidos. La separación industrial del o-xileno adopta principalmente el método de superdestilación; primero se separa el o-xileno y el etilbenceno del xileno mezclado, lo que exige el uso de una torre de destilación de 100~150 bandejas; seguido de la separación del o-xileno y el etilbenceno para obtener el o-xileno puro.
Categoría
Líquidos inflamables
Grado de toxicidad
Intoxicación
Toxicidad aguda
LDL0 oral-rata: 5000 mg/kg; LD50 inyección abdominal-ratón: 1364 mg/kg
EXPLOSIVOS y CARACTERÍSTICAS PELIGROSAS
siendo explosivo al mezclarse con el aire
Inflamabilidad y características peligrosas
siendo inflamable a la llama, al calor, al oxidante Inflamable con combustión liberando humo irritante
Características de almacenamiento y transporte
almacén: ventilado, a baja temperatura y seco; cargar y descargar con cuidado; almacenarlo separado de oxidantes y ácidos.
Agente extintor
agua nebulizada, espuma, arena, dióxido de carbono, agente extintor 1211
Normativa laboral
TLV-TWA 100 PPM (440 mg/m 3); STEL 150; PPM (655 mg/m 3)
Propiedades químicas
Líquido incoloro
Propiedades físicas
Líquido claro e incoloro con olor aromático. Una concentración umbral de olor de 380 ppbv fue reportada por Nagata y Takeuchi (1990).
Usos
Preparación de ácido ftálico, anhídrido ftálico, ácido tereftálico, ácido isoftálico; disolvente para resinas alquídicas, lacas, esmaltes, cementos de caucho; fabricación de tintes, productos farmacéuticos e insecticidas; combustibles para motores.
Definición
ChEBI: Un xileno sustituido por grupos metilo en las posiciones 1 y 3.
Referencia(s) de síntesis
Journal of the American Chemical Society, 97, p. 7262, 1975 DOI: 10.1021/ja00858a011
The Journal of Organic Chemistry, 44, p. 2185, 1979 DOI: 10.1021/jo01327a032
Descripción general
Líquido acuoso incoloro con olor dulce. Menos denso que el agua. Insoluble en agua. Vapor irritante.
Aire &Reacciones en el agua
Altamente inflamable. Insoluble en agua.
Perfil de reactividad
El 1,2-Dimetilbenceno puede reaccionar con materiales oxidantes. .
Peligro para la salud
Los vapores provocan dolor de cabeza y mareos. El líquido irrita los ojos y la piel. Si entra en los pulmones, causa tos severa, angustia y edema pulmonar de rápido desarrollo. Si se ingiere, provoca náuseas, vómitos, calambres, dolor de cabeza y coma. Puede ser mortal. Pueden producirse daños renales y hepáticos.
Peligro de incendio
Comportamiento en caso de incendio: El vapor es más pesado que el aire y puede recorrer una distancia considerable hasta una fuente de ignición y retroceder.
Reactividad química
Reactividad con el agua Ninguna reacción; Reactividad con materiales comunes: Ninguna reacción; Estabilidad durante el transporte: Estable; Agentes neutralizadores de ácidos y cáusticos: No pertinente; Polimerización: No pertinente; Inhibidor de la polimerización: No pertinente.
Perfil de seguridad
Moderadamente tóxico por vía intraperitoneal. Moderadamente tóxico por ingestión e inhalación. Un teratógeno experimental. Un contaminante común del aire. Un riesgo de incendio muy peligroso cuando se expone al calor o a las llamas. Explosivo en forma de vapor cuando se expone al calor o a las llamas. Para luchar contra el fuego, utilice espuma, CO2, productos químicos secos.Incompatible con materiales oxidantes.Cuando se calienta hasta su descomposición emite un humo acre y humos irritantes. Emitido por materiales de construcción modernos (CENEAR69,22,91). Ver también otras entradas de xileno.
Fuente
Detectado en fracciones solubles en agua destilada de gasolina de 87 octanos (3,83 mg/L), gasolina de 94 octanos (11,4 mg/L), Gasohol (8,49 mg/L), fuel oil Nº 2 (1,73 mg/L), jet fuel A (0.87 mg/L), combustible diésel (1,75 mg/L), combustible militar JP-4 (1,99 mg/L) (Potter, 1996), aceite de motor nuevo (16,2 a 17,5 μg/L) y aceite de motor usado (294 a 308 μg/L) (Chen et al., 1994). El porcentaje de volumen promedio y la fracción molar estimada en la gasolina PS-6 del Instituto Americano del Petróleo son 2,088 y 0,01959, respectivamente (Poulsen et al., 1992). Schauer et al. (1999) informaron de la presencia de o-xileno en los gases de escape de un camión de servicio mediano con motor diésel con una tasa de emisión de 830 μg/km. El combustible diésel obtenido de una estación de servicio en Schlieren, Suiza, contenía o-xileno en una concentración de 223 mg/L (Schluep etal., 2001).
La gasolina reformulada Fase II de California contenía o-xileno en una concentración de 19,7 g/kg.Los índices de emisión del tubo de escape en fase de gas de los automóviles de gasolina con y sin convertidores catalíticos fueron de 5,41 y 562 mg/km, respectivamente (Schauer et al., 2002).
Thomas y Delfino (1991) equilibraron aguas subterráneas libres de contaminantes recogidas en Gainesville, FL, con fracciones individuales de tres productos petrolíferos individuales a 24-25 °C durante 24 horas. Las concentraciones medias de m+p-xileno registradas en las fracciones solubles en agua de la gasolina sin plomo, el queroseno y el gasóleo fueron de 8,611, 0,658 y 0,228 mg/L, respectivamente. Cuando los autores analizaron la fase acuosa mediante el método de prueba 610 aprobado por la EPA de EE.UU., las concentraciones promedio de m+p-xileno en las fracciones solubles en agua de la gasolina sin plomo, el queroseno y el combustible diesel fueron menores, es decir, 6,068, 0,360 y 0,222 mg/L, respectivamente.Sobre la base del análisis de laboratorio de 7 muestras de alquitrán de hulla, las concentraciones de o-xileno oscilaron entre 2 y 2.000 ppm (EPRI, 1990). Un alquitrán de hulla de alta temperatura contenía o-xileno en una concentración media de 0,04 % en peso (McNeil, 1983).
Schauer et al. (2001) midieron las tasas de emisión de compuestos orgánicos volátiles, compuestos orgánicos semivolátiles en fase gaseosa y compuestos orgánicos en fase de partículas procedentes de la combustión residencial (chimenea) de pinos, robles y eucaliptos. La tasa de emisión de o-xileno en fase gaseosa fue de 18,1 mg/kg de pino quemado. Las tasas de emisión de o-xileno no se midieron durante la combustión de roble y eucalipto.
Norma de agua potable (final): Para todos los xilenos, el MCLG y el MCL son ambos de 10 mg/L. Además, se recomendó un DWEL de 70 mg/L (U.S. EPA, 2000).
Fato ambiental
Biológico. Los productos de biodegradación notificados del producto comercial que contiene xileno incluyen el ácido α-hidroxi-p-toluico, el alcohol p-metilbencílico, el alcohol bencílico, el 4-metilcatecol y los ácidos mandp-toluicos (Fishbein, 1985). El o-xileno también se cometabolizó dando lugar a la formación de ácido o-toluico (Pitter y Chudoba, 1990). En aguas subterráneas anóxicas cerca de Bemidji, MI, el o-xileno se biodegradó en forma intermedia al ácido o-toluico (Cozzarelli et al., 1990). En aguas subterráneas contaminadas con gasolinas, se identificó el ácido metilbenzilsuccínico como el primer intermediario durante la degradación anaeróbica de los xilenos (Reusser y Field, 2002).
Fotolítica. Cox et al. (1980) informaron de una constante de velocidad de 1,33 x 10-11 cm3/molécula/segundo para la reacción del o-xileno gaseoso con los radicales OH, basándose en un valor de 8 x 10-12 cm3/molécula/segundo para la reacción del etileno con los radicales OH.
Agua superficial. La vida media de evaporación del o-xileno en el agua superficial (1 m de profundidad) a 25 °C se estima en 5,18 h (Mackay y Leinonen, 1975).
Agua subterránea. Nielsen et al. (1996) estudiaron la degradación del o-xileno en un acuífero arenoso poco profundo, glaciofluvial y no confinado en Jutlandia, Dinamarca. Como parte del estudio de microcosmos in situ, se instaló un cilindro abierto en la parte inferior y tamizado en la parte superior a través de un pozo entubado a unos 5 m de profundidad. Se airearon cinco litros de agua con aire atmosférico para asegurar que se mantenían las condiciones aeróbicas. El agua subterránea se analizó semanalmente durante aproximadamente 3 meses para determinar las concentraciones de o-xileno con el tiempo. La constante de velocidad de biodegradación de primer orden determinada experimentalmente y la correspondiente vida media tras una fase de retardo de 7 días fueron de 0,1/d y 6,93 d, respectivamente.
Fotolítica. Cuando el aire sintético que contenía ácido nitroso gaseoso y o-xileno se expuso a la luz solar artificial (λ = 300-450 nm), se formaron como productos biacetilo, nitrato de peroxiacetal y nitrato de metilo (Cox et al., 1980). Una solución de n-hexano que contenía o-xileno y extendida en forma de película fina (4 mm) sobre agua fría (10 °C) fue irradiada por una lámpara de mercurio de media presión. En 3 horas, el 13,6% del o-xileno se fotooxidó en o-metilbenzaldehído, alcohol o-benzílico, ácido o-benzoico y ometilacetofenona (Moza y Feicht, 1989). La irradiación de o-xileno a ≈ 2537 ? a 35 °C y 6mmHg se isomeriza en m-xileno (Calvert y Pitts, 1966). El glioxal, el metilglioxal y el biacetilo se produjeron a partir de la fotooxidación del o-xileno por radicales OH en el aire a 25 °C (Tuazon et al.,1986a).
Química/Física. En condiciones atmosféricas, la reacción en fase gaseosa del o-xileno con los radicales OH y los óxidos de nitrógeno dio lugar a la formación de o-tolualdehído, nitrato de o-metilo, nitro-o-xilenos, 2,3 y 3,4-dimetilfenol (Atkinson, 1990). Kanno et al. (1982) estudiaron la reacción acuosa del o-xileno y otros hidrocarburos aromáticos (benceno, tolueno, m- y p-xileno, y naftaleno) con ácido hipocloroso en presencia de ion amonio. Informaron de que el anillo aromático no se cloraba como se esperaba, sino que era escindido por la cloramina formando cloruro de cianógeno. La cantidad de cloruro de cianógeno formada aumentó a pHs más bajos (Kanno et al., 1982). En la fase gaseosa, el o-xileno reaccionó con radicales de nitrato en aire purificado formando los siguientes productos: 5-nitro-2-metiltolueno y 6-nitro-2-metiltolueno, o-metilbenzaldehído y un nitrato de arilo (Chiodini et al., 1993).
Métodos de purificación
El o-xileno (4,4Kg) se sulfonó agitando durante 4 horas con 2,5L de H2SO4 conc a 95o. Tras enfriar y separar el material no sulfonado, el producto se diluye con 3L de agua y se neutraliza con NaOH al 40%. Al enfriar, el o-xileno sulfonato de sodio se separa y se recristaliza a partir de la mitad de su peso de agua. La sal se disuelve en la cantidad mínima de agua fría, luego se mezcla con la misma cantidad de agua fría y con el mismo volumen de H2SO4 conc y se calienta a 110o. Se regenera el o-xileno y se destila al vapor. El destilado se satura con NaCl, se separa la capa orgánica, se seca y se vuelve a destilar.
