一般名:塩酸リドカイン
剤形:外用ゼリー
医薬品のレビューはDrugs.comで行っています。 最終更新日:2020年10月1日。
- 概要
- 副作用
- 用法用量
- その他
医薬品のみ
説明
Lidocaine HCI 2% Jelly is a sterile, 局所麻酔剤を含有する水性製剤で、局所的に投与されます。 (具体的な用途は「効能・効果」をご参照ください。)
リドカインHCI 2%ゼリーは、化学的にアセトアミド、2-(ジエチルアミノ)-N-(2,6-ジメチルフェニル)-、モノヒドロクロライドとして指定されており、次の構造式を有するリドカインHCIを含みます:
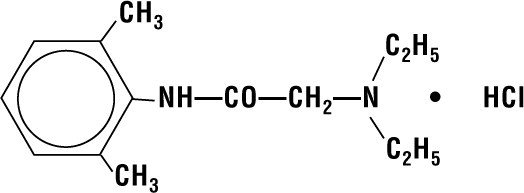
その分子式はC14H22N2O ・ HCI、その分子量は270であり、その分子式は、C14H22NH2O・HCIです。80.
リドカインHCI2%ゼリーにはヒプロメロースも含まれており、得られた混合物は粘膜との接触を最大化し、器具装着時の潤滑性を提供します。
リドカインHCI2%ゼリーの組成 30mL、5mLチューブ。 1mLあたり20mgのリドカインHCIが含まれています。 また、メチルパラベン、プロピルパラベン、ヒプロメロース、およびpHを6.0~7.0に調整するための水酸化ナトリウムおよび/または塩酸が含まれています。
CLINICAL PHARMACOLOGY
Mechanism of Action.リドカインHCIの作用機序は以下のとおりです。 リドカインは、インパルスの開始と伝導に必要なイオン流束を阻害することにより神経膜を安定化させ、局所麻酔作用を発揮します。 作用の発現は3~5分である。 無傷の皮膚に適用しても効果はない。
血行動態。 過度の血中濃度は、心拍出量、全末梢抵抗及び平均動脈圧の変化を引き起こす可能性がある。 これらの変化は、心血管系の様々な構成要素に対する局所麻酔薬の直接的な抑圧作用に起因すると考えられる。 リドカインは粘膜への局所投与後に吸収されることがあり、その速度と範囲は投与された濃度および総量、特定の適用部位、および曝露時間に依存する。 一般に、局所麻酔薬の吸収速度は、気管内投与後に最も速く起こる。 リドカインはまた、消化管からよく吸収されるが、肝臓での生体内変換のため、無傷の薬物はほとんど循環に現れない。
リドカインは肝臓で急速に代謝され、代謝産物と未変化体は腎臓から排泄される。 生体内変換には、酸化的N-脱アルキル化、環状水酸化、アミド結合の開裂、および抱合などが含まれる。 N-脱アルキル化により、モノエチルグリシネキシルイミドおよびグリシネキシルイミドが生成される。 これらの代謝物の薬理・毒性作用は、リドカインと類似しているが、リドカインより作用が弱くなる。 投与されたリドカインの約90%が様々な代謝物の形で排泄され、未変化体は10%未満です。 尿中の主な代謝物は4-ヒドロキシ-2、6-ジメチルアニリンの抱合体である。
リドカインの血漿結合は薬剤濃度に依存し、結合率は濃度の上昇とともに減少する。 1mLあたり1~4mcgの遊離基の濃度では、リドカインの60~80%がタンパク質と結合する。
リドカインは、おそらく受動拡散によって血液脳関門および胎盤関門を通過する。
静脈内ボーラス注射後のリドカイン代謝の研究により、この薬剤の消失半減期は通常1.5~2.0時間であることが示されている。 リドカインの代謝速度は速いため、肝機能に影響を与えるいかなる状態もリドカインの動態を変化させる可能性があります。 肝機能障害のある患者では、半減期が2倍以上延長されることがあります。
アシドーシス、中枢神経刺激剤および抑制剤の使用などの要因は、明白な全身性効果をもたらすために必要なリドカインの中枢神経レベルに影響を及ぼします。 客観的な有害事象は、静脈血漿濃度が1mLあたり6mcg遊離塩基を超えると次第に明らかになる。
INDICATIONS AND USAGE
リドカインHCI 2%ゼリーは、男性および女性の尿道を含む処置における痛みの予防と制御、痛みを伴う尿道炎の局所治療、気管内挿管(口腔および鼻)の麻酔潤滑油として適応されています。
禁忌
リドカインは、アミド型局所麻酔薬またはリドカインHCI 2%ゼリーの他の成分に対して過敏症の既往歴のある患者には禁忌です。
警告
過量投与または投与間隔の短さは、高い血漿濃度および重大な副作用を引き起こすことがあります。 患者には、この添付文書に記載されている推奨用量および投与ガイドラインを厳密に遵守するよう指導してください。 重篤な有害反応の管理には、人工呼吸器、オキシジェン、その他の人工呼吸薬の使用が必要な場合があります。
Lidocaine HCI 2%ゼリーは、敗血症または適用部位の重度の外傷粘膜がある場合は、そのような状況下で急速に全身吸収する可能性があるので、細心の注意をもって使用する必要があります。
気管内チューブの潤滑に使用する場合は、チューブの内腔に本品が入らないように注意すること。 気管内用スタイレットの潤滑に使用しないこと。 内腔に入った場合、ゼリーが内面で乾燥し、残留物となり、屈曲により固まりやすく、内腔を狭めることがある。 まれに、この残留物によって内腔が閉塞したとの報告がある。 (有害反応および用法・用量も参照のこと。)
注意事項
一般的なこと。 リドカインの安全性と有効性は、適切な投与量、正しい技術、十分な予防措置、および緊急事態への準備に依存します。 (警告および有害反応の項を参照)高い血漿濃度および重篤な有害作用を避けるため、効果的な麻酔をもたらす最低量を使用する必要がある。 リドカインの反復投与は、薬物またはその代謝物の緩やかな蓄積のため、反復投与ごとに血中濃度の著しい上昇を引き起こす可能性がある。 血中濃度上昇に対する耐性は、患者の状態によって異なります。 衰弱した患者、高齢の患者、急性疾患の患者、および小児は、年齢および身体状況に応じた減量が必要である。
リドカインHCI2%ゼリーは、既知の薬物過敏症の患者には慎重に使用されるべきです。 パラアミノ安息香酸誘導体(プロカイン、テトラカイン、ベンゾカインなど)にアレルギーがある患者は、リドカインに対する交差感受性を示していません。
麻酔を行う際に使用する多くの薬剤は、家族性悪性高熱症の引き金となりうる薬剤とみなされています。 アミド型局所麻酔薬がこの反応を誘発するかどうかは不明であり、全身麻酔の補完の必要性を事前に予測することはできないため、管理のための標準プロトコルを利用できるようにすることが示唆される。 体温上昇に先行して、頻脈、頻呼吸、不安定な血圧、代謝性アシドーシスなどの原因不明の徴候が早期に現れることがある。 成功する転帰は、早期診断、疑わしい誘因物質の迅速な中止、酸素療法、指示された支持手段およびダントロレン(使用前にダントロレンナトリウム静注用添付文書を参照)などの治療を実施することに依存します。 局所麻酔薬を口腔内に使用する場合、局所麻酔の生成により嚥下が障害され、誤嚥の危険性が高まることを患者に認識させる必要がある。 このため、局所麻酔剤を口腔内または咽頭部に使用した後60分間は、食物を摂取してはならない。
舌や頬粘膜のしびれは、意図しない咬傷の危険性を高める可能性がある。
発がん性-リドカインの発がん性の可能性を評価するための動物での長期的な研究は行われていない。
変異原性-リドカインの変異原性の可能性は、Ames Salmonella reverse mutation assay、ヒトリンパ球のin vitro chromosome aberrations assay、in vivo マウス小核アッセイでテストされています。
生殖能力の障害-リドカインの生殖能力への影響は、ラットモデルで調査されました。 30mg/kg、s.c.(180mg/m2)を交配ペアに投与しても、ラットの受胎能力及び一般生殖能力には変化がなかった。 リドカインの精子パラメータへの影響を検討した研究はない。 生殖能力に変化があったという証拠はありませんでした。
妊娠中の使用:
催奇形性作用。
リドカインの繁殖研究は、ラットとウサギの両方で実施されています。 ラットモデルでは、リドカイン50mg/kg(体表面積基準で300mg/m2)までの皮下投与で、胎児に害を与える証拠はありませんでした。 ウサギモデルでは、5mg/kg、s.c.(体表面積基準で60mg/m2)の用量で、胎児への有害性の証拠はなかった。 ウサギに25 mg/kg(300 mg/m2)を投与すると、母体毒性および胎児体重の有意でない減少(7%)および小骨格異常の増加(頭蓋骨および胸骨の欠損、指骨の骨化低下)など、胎児発育遅延の証拠が認められた。 ラットにおいて、妊娠15日目から産後20日まで、妊娠雌ラットに2、10、50 mg/kg(12, 60, 300 mg/m2)の用量で毎日皮下投与し、出生後の発達に対するリドカインの影響を検討した。 10 mg/kg(60 mg/m2)までの投与ではダムおよび仔ラットに悪影響は認められなかったが,50 mg/kg(300 mg/m2)では出生時および授乳期の両方で生存仔数が減少し,この影響は母体毒性に続発した可能性が高いことがわかった。
2番目の研究では、離乳から性成熟までの仔の評価を含む、ラットの出生後の発達に対するリドカインの影響を調べました。 ラットは10または30mg/kgのリドカイン(体表面積でそれぞれ60mg/m2および180mg/m2)を8カ月間投与された。 この期間は3回の発情期を包含していた。 しかし、リドカインの両用量は、最初の2回の交配期間から生まれた子供の離乳まで生存する1子あたりの平均数を著しく減少させた。
しかし、妊婦における適切かつよく管理された研究はない。 動物の繁殖研究は必ずしもヒトの反応を予測するものではないため、この薬剤は明らかに必要な場合にのみ妊娠中に使用されるべきである。 リドカインは陣痛と分娩に禁忌ではありません。 リドカイン塩酸塩2%ゼリーをリドカインを含む他の製品と併用する場合は、すべての製剤が寄与する総用量を念頭に置く必要があります
授乳婦。 リドカインはヒトの乳汁中に分泌される。 この観察の臨床的意義は不明である。 リドカインを授乳婦に投与する場合は注意が必要である。
小児への使用。 小児患者におけるリドカイン2%ゼリーの安全性と有効性は確立されていませんが、19人の未熟児(妊娠期間<33週)の研究では、鼻腔内および気管内チューブの潤滑に適量のリドカイン(例:リドカインゲル20mg/mlの0.3mL/kg)を使用した場合、リドカインまたはモノエチルグリシンエチルジドの血漿濃度と乳児体重に相関関係は認められませんでした。 リドカインの血漿中濃度が750 mcg/Lを超えた新生児はいなかった。 小児への投与量は、年齢、体重、体調に応じて減量する必要があります。 (用法・用量参照)
有害反応
リドカイン投与後の有害体験は、他のアミド系局所麻酔薬で観察されるものと性質が類似しています。 これらの有害事象は、一般的に用量に関連しており、過剰投与または急速な吸収による高い血漿レベル、または患者側の過敏症、特異体質、または耐性低下から生じる可能性があります。 重篤な有害事象は、一般に全身性のものです。
気管内チューブの内腔に乾燥ゼリー残渣が存在することに関連した気管内チューブ閉塞がまれに報告されています。 (警告及び用法・用量も参照のこと)
中枢神経系:
中枢神経系には以下のものがある。 中枢神経系の症状は興奮性および/または抑制性で、軽い頭痛、神経質、不安、多幸感、混乱、めまい、眠気、耳鳴り、かすみまたは複視、嘔吐、熱感、冷感またはしびれ、ひきつけ、振戦、けいれん、意識不明、呼吸抑制および停止が特徴である場合がある。 興奮性の発現は非常に短いか、まったく起こらないこともあり、その場合、毒性の最初の発現は意識不明および呼吸停止に合併する眠気である。
リドカイン投与後の眠気は通常、薬物の高い血中濃度の初期徴候であり、急速な吸収の結果として起こる可能性がある。 心血管系の症状は通常抑圧的で、徐脈、低血圧、心停止に至ることもある心血管系の崩壊によって特徴づけられる。
アレルギー性。 アレルギー反応は、皮膚病変、蕁麻疹、浮腫、またはアナフィラキシー様反応によって特徴付けられる。 アレルギー反応は、局所麻酔薬または製剤中の他の成分に対する感受性の結果として生じることがあります。 リドカインに対する感受性の結果としてのアレルギー反応は極めてまれであり、発生した場合は従来の方法で管理する必要があります。
過量投与
局所麻酔薬による急性緊急事態は、一般に局所麻酔薬の治療使用中に遭遇する高い血漿濃度と関連している。 (有害反応、警告、および注意の項を参照)
局所麻酔薬の緊急事態の管理
局所麻酔薬の緊急事態の管理。 第一に考慮すべきは予防で、局所麻酔薬を投与するたびに、心血管系および呼吸系のバイタルサインと患者の意識状態を注意深く常時監視することが最も効果的である。
痙攣の管理における最初のステップは、気道確保に直ちに注意を払い、酸素とマスクによる即時気道陽圧を可能にする送達システムによる補助換気または管理換気を行うことである。 これらの換気措置を行った直後に、けいれんの治療に使用される薬剤が静脈内投与されると循環を抑制することがあることを念頭に置いて、循環の妥当性を評価する必要がある。 十分な呼吸補助を行ってもけいれんが続く場合、循環動態が許せば、超短時間作用型バルビツール酸塩(チオペンタール、チアミラールなど)またはベンゾジアゼピン(ジアゼパムなど)を少量ずつ静脈内投与することができる。 臨床医は、局所麻酔薬を使用する前に、これらの抗痙攣薬についてよく理解しておく必要がある。 循環器系抑制の支持療法には、静脈内輸液の投与と、適切な場合には臨床状況に応じて血管拡張薬(例えば、エフェドリン)の投与が必要である。
直ちに治療しない場合、けいれんおよび循環器系抑制はいずれも低酸素、アシドーシス、徐脈、不整脈および心停止を引き起こす可能性がある。
リドカインHCIの非絶食雌ラットの経口LD50は459(346~773)mg/kg(塩として)、絶食雌ラットでは214(159~324)mg/kg(塩として)である。
用法・用量
リドカインHCI 2%ゼリーをリドカインを含む他の製品と併用する場合、すべての製剤が寄与する総用量を念頭に置かなければならない。
用量は様々で、麻酔する部位、組織の血管性、個人の耐性、麻酔の技術に依存する。 効果的な麻酔を提供するために必要な最低量を投与すべきである。 小児および高齢者、衰弱した患者には投与量を減らすべきである。 リドカインHCI 2%ゼリーによる副作用の発生率は極めて低いが、副作用の発生率は投与された局所麻酔薬の総量に正比例するので、特に大量に使用する場合は注意すること
男性成人の尿道の表面麻酔の場合。 リドカイン2%ゼリー30mLチューブを使用する場合、プラスチックコーンを熱湯で5分間滅菌し、冷却後、チューブに装着する。 コーンは、ガス滅菌でも低温滅菌でもよい。 約15mL(リドカインHCI 300mg)をゆっくりと尿道内に注入するか、患者が緊張感を覚えるまで注入する。 その後、陰茎クランプをコロナで数分間適用する。
超音波検査または膀胱鏡検査の前に、十分な麻酔を得るために陰茎クランプを5~10分間適用すべきである。
カテーテル挿入前には、通常、潤滑のため5~10mL(100~200mg)の少量で十分である。 リドカイン2%ゼリー30mLチューブを使用する場合、プラスチックコーンを熱湯で5分間滅菌し、冷却後、チューブに装着する。 コーンは、ガス滅菌でも低温滅菌でもよい。 ゼリー3~5mL(リドカインHCIとして60~100mg)をゆっくりと尿道内に注入する。 必要であれば、ゼリーの一部を綿棒に付着させ、尿道に導入してもよい。 十分な麻酔をかけるため、泌尿器科的処置の前に数分間時間を置くべきである。 使用直前に気管内チューブの外面に適量のゼリーを塗布する。 なお、本剤がチューブの内腔に入らないように注意する。 気管内用スタイレットの潤滑にゼリーを使用しないこと。 まれに内腔閉塞の報告があるので、「警告」及び「有害反応」を参照すること。
最大投与量
12時間以内にリドカインHCIとして600mgを超えて投与してはならない。 小児:年齢と体重によって異なるため、どのような薬剤でも最大投与量を推奨することは困難である。 正常な除脂肪体重と正常な除脂肪体重の発達を有する10歳未満の小児については、最大投与量は標準的な小児薬物公式の一つ(例えば、クラークの法則)を適用して決定することができる。 例えば、体重50ポンドの5歳の子供では、クラークの法則に従って計算すると、塩酸リドカインの用量は75〜100mgを超えないはずである。 いずれの場合も、リドカイン塩酸塩の最大投与量は体重の4.5 mg/kg (2 mg/lb) を超えてはならない。
HOW SUPPLIED
Lidocaine HCI 2% Jellyは、記載されている剤形で提供される。
NDC 17478-840-30 30 mLアルミニウムチューブ
NDC 17478-840-05 5 mLアルミニウムチューブ
30mLカートンに取り外し可能なアプリケーターコーンおよび内容物を表現するためのキーが含まれています。
PREMIERProRx®
製造元:
エイコーン 株式会社
Lake Forest, IL 60045
PremierProRx®はPremier Inc.の登録商標です。 の登録商標であり、ライセンスに基づき使用されています。
PLD00N Rev. 10/15
Principal Display Panel Text for Container Label:
NDC 17478-840-05 Premier Logo
Lidocaine Hydrochloride Jelly USP, 2%
Rx only
Sterile 5 mL

Priminal表示パネルテキスト for Carton Label.
Primential Display Panel Text for Carton Label.
Directory: Lidocaine Hydrochloride Jelly USP, 2%
Rx only
Sterile 5 mL
NDC 17478-840-05 Sterile 5 mL
Lidocaine Hydrochloride Jelly USP.L
Lidocaine Hydrochloride Jelly USP, 2%
医薬品のみ
プレミアロゴ

| リドカイン 塩酸リドカインゼリー |
|
|||||||||||||||
|
||||||||||||||||
|
||||||||||||||||
|
||||||||||||||||
|
||||||||||||||||
Labeler – (ラベリング) Akorn, Inc. (117696770)
登録者-。 Akorn Operating Company LLC (117693100)
| 設立 | |||
| 名前 | 住所 | ID/FEI | 運営 |
| エーコーン. Inc | 117696840 | MANUFACTURE(17478-840), ANALYSIS(17478-840), STERILIZE(17478-840), PACK(17478-840), LABEL(17478-840) | |
リドカイン外用剤の詳細
- 副作用
- 用法・用量 薬物相互作用
- 代替品の比較
- 価格 & クーポン
- En Español
- 208 Reviews
- 薬剤分類: 局所麻酔薬
- FDA 警告 (5)
妊娠中または授乳中
消費者リソース
- 患者情報
- リドカイン局所適用(上級リーディング)
専門家リソース
。
- 処方情報
- リドカイン(外用)(専門家による患者への助言)
- リドカインクリーム(FDA)
- リドカインゲル(FDA)
- リドカイン喉頭液
- 。.. +9 more
Other brands Lidocaine Viscous, ZTlido, Xylocaine Jelly, Xylocaine Topical, … +24 more
関連治療ガイド
- 肛門のかゆみ
- 消化器外科
- 麻酔
- 火傷、外部
- …。 +9 more
Medical Disclaimer
