- Introducción
- Materiales, Productos Químicos y Métodos
- Materiales
- Proceso de purificación del glicerol
- Primer paso: Acidificación
- Segundo Paso: Intercambio iónico
- Métodos analíticos
- Diseño de experimentos utilizando el método Taguchi
- Análisis de medias
- Análisis de Varianza
- Experimentos de confirmación
- Resultados y discusión
- Caracterización del glicerol crudo
- Acidificación
- Condiciones óptimas mediante el enfoque ANOM
- Efecto de los parámetros sobre la acidificación
- Contribución porcentual de los parámetros mediante ANOVA
- Experimentos de confirmación
- Intercambio iónico
- Condiciones óptimas mediante el enfoque ANOM
- Efecto de los parámetros en el intercambio iónico
- Porcentaje de contribución de los parámetros mediante ANOVA
- Experimento de confirmación
- Comparación de las características del glicerol purificado con otros trabajos
- Conclusión
- Contribuciones de los autores
- Conflicto de intereses
- Agradecimientos
Introducción
El biodiésel es un combustible biodegradable y renovable producido por transesterificación a partir de fuentes renovables como la soja, las microalgas, el aceite de cocina de palma y la jatrofa (da Silva César et al., 2018; Corach et al., 2019). Recientemente, el biodiésel está atrayendo a muchos investigadores ya que es uno de los biocombustibles más explorados que podría reducir la dependencia global de los combustibles fósiles y el efecto invernadero. Se estima que la producción de biodiésel aumentará anualmente un 4,5% y alcanzará los 41 Mm3 en 2022 (Monteiro et al., 2018).
El glicerol crudo es el principal subproducto producido durante el proceso de transesterificación en la planta de biodiésel, con la generación del 10 % en peso del producto biodiésel (Samul et al., 2014). Según el análisis, se genera alrededor de 1 kg de glicerol crudo con cada 10 kg de producción de biodiésel (Hajek y Skopal, 2010; Tan et al., 2013; Chol et al., 2018). El valor de mercado actual del glicerol puro es de 0,27-0,41 dólares por libra; sin embargo, el glicerol crudo con un 80% de pureza es tan bajo como 0,04-0,09 dólares por libra. Esto demuestra que el exceso de producción de glicerol afecta al precio de la glicerina en el mercado. Por lo tanto, la utilización del glicerol crudo para productos de valor añadido se ha convertido en un problema serio en la industria del biodiésel.
El glicerol con alta pureza tiene una amplia aplicación en varias industrias como la farmacéutica, la cosmética y la alimentaria. Sin embargo, el porcentaje de pureza del glicerol de la industria del biodiésel está limitando su conversión en un producto de alto valor (Samul et al., 2014; Talebian-Kiakalaieh et al., 2018). El glicerol crudo contiene un gran número de contaminantes como jabón, sales, etanol, metanol, agua, ácido graso, ésteres metílicos, glicéridos y cenizas (Tan et al., 2013; Dhabhai et al., 2016). Yang et al. (2012) afirmaron que las impurezas del glicerol crudo podrían influir en gran medida en su conversión en otros productos de valor añadido (Yang et al., 2012). Venkataramanan et al. (2012) también informaron de que los jabones presentes en el glicerol crudo tienen un fuerte efecto inhibidor sobre la utilización del glicerol por parte de las bacterias, lo que afecta al rendimiento del glicerol crudo como fuente de carbono en el proceso de fermentación (Venkataramanan et al., 2012). Como conclusión, las impurezas presentes en el glicerol crudo crean un reto importante para convertirlas en un producto de valor añadido. Por lo tanto, es importante purificar el glicerol crudo para evitar la saturación del mercado y aumentar los beneficios de la producción de biodiésel.
En la literatura, los procesos más utilizados son la destilación, la resina de intercambio iónico, la tecnología de separación por membranas, la acidificación, seguida de la neutralización y la extracción con disolventes. La acidificación es una técnica comúnmente utilizada para neutralizar las impurezas como el catalizador en sal inorgánica. Además de la acidificación, también es capaz de reducir la cantidad de jabones convirtiéndolos en ácido graso libre insoluble, ya que pueden afectar negativamente a la separación y causar una pérdida de rendimiento (Hajek y Skopal, 2010; Kovács et al., 2012). Dado que el proceso de acidificación no elimina todas las impurezas, es necesario un paso más de purificación para eliminar otras impurezas como el metanol, el aceite, el agua y el éster. Sin embargo, el proceso de destilación tiene algunas limitaciones con respecto a otros, ya que requiere un elevado aporte de energía para la vaporización y provoca descomposiciones térmicas (Lancrenon y Fedders, 2008). Además, en la destilación también se requiere un alto vacío para evitar la desnaturalización a alta temperatura del glicerol mediante la formación de acroleína (Manosak et al., 2011). Además, este proceso conlleva una elevada inversión de capital y costes de mantenimiento, acompañados de considerables pérdidas de glicerol (Sdrula, 2010). En comparación con el proceso de destilación, el proceso de intercambio iónico está ganando una amplia aceptación debido a la simplicidad de la operación, el bajo consumo de energía y el requisito de energía, así como el hecho de que también ha demostrado ser eficiente en la eliminación de trazas de impurezas, color y olor (Carmona et al., 2009, 2012). Además, Xiao et al. (2013) sugirieron que el proceso de purificación de múltiples pasos del glicerol crudo podría aumentar la pureza y hacerlo viable para varios usos (Xiao et al., 2013).
Este estudio tiene como objetivo obtener glicerol crudo con la mayor pureza a través de la purificación de dos pasos utilizando técnicas de acidificación e intercambio iónico, con la ayuda del método Taguchi. En este estudio, se utilizó el análisis estadístico, incluyendo una matriz ortogonal L9 de Taguchi, la relación señal-ruido, el análisis de la media, el análisis de la varianza y los análisis de regresión para identificar las condiciones óptimas de los procesos de purificación.
Materiales, Productos Químicos y Métodos
Materiales
El glicerol crudo se recogió de una planta local de biodiesel, en Malasia. Se adquirió una resina de intercambio catiónico fuerte H+, Amberlyst 15, de Sigma Aldrich Sdn. Bhd. Las propiedades de la resina se muestran en la Tabla 1. El ácido fosfórico (85 % en peso), los gránulos de hidróxido de sodio y el metanol se compraron a Merck Sdn. Bhd. Se utilizó agua destilada para la preparación de las soluciones químicas.

Tabla 1. Propiedades de las resinas de intercambio catiónico.
Proceso de purificación del glicerol
Primer paso: Acidificación
El glicerol crudo fue pretratado en base al procedimiento adoptado de Manosak et al. (2011). Los experimentos se llevaron a cabo en matraces Erlenmeyer de 500 ml y se equilibraron utilizando un agitador magnético. Inicialmente, el glicerol crudo se acidificó mediante el uso de ácido fosfórico hasta el valor de pH deseado y luego se agitó a una velocidad constante de 200 rpm durante 1 h. La solución se dejó inactiva para la separación de fases. Se separó en tres capas que son un ácido graso libre, glicerol y capas de sales inorgánicas, respectivamente. La primera capa, rica en ácido graso, se separó por decantación, y la sal precipitada se eliminó por filtración con un filtro de 0,45 μm. La capa intermedia, rica en glicerol, se neutralizó (pH 7) añadiendo NaOH. Las sales inorgánicas y de ácidos grasos que se formaron en la etapa de neutralización se eliminaron mediante un filtro de 0,45 μm. Los parámetros de entrada seleccionados para este diseño fueron el pH, la temperatura y el tiempo de reacción, que se designaron como parámetros A, B y C, respectivamente (Tabla 2). Para el diseño de los experimentos en este trabajo se utilizó la matriz ortogonal L9 (Tabla 3).
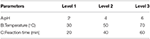
Tabla 2. Parámetros de funcionamiento y niveles.
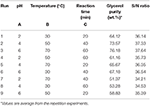
Tabla 3. Diseño experimental de arreglo ortogonal L9 y resultados de los experimentos de acidificación.
Segundo Paso: Intercambio iónico
En el proceso de intercambio iónico se utilizó el glicerol pretratado obtenido del proceso de acidificación con condiciones de operación optimizadas. Las resinas de intercambio iónico se investigaron haciendo pasar la alimentación a través de una columna de 300 ml de resina soportada en un tubo de vidrio. Para la eliminación de los iones libres se utilizaron resinas de intercambio iónico del tipo Amberlyst 15 en forma de hidrógeno. La resina se hinchó previamente con metanol (25 % en peso) en un recipiente de vidrio y se introdujo en la columna. Además, las perlas de sílice también se empaquetaron dentro de la columna para eliminar el exceso de contenido de humedad. Las resinas de intercambio iónico se utilizaron para adsorber los aniones y cationes libres en el glicerol pretratado. A continuación, el glicerol pretratado se cargó en el tanque de alimentación y se utilizó una bomba para hacer circular el glicerol crudo a través del lecho de resina de intercambio iónico en las condiciones de funcionamiento predeterminadas. La temperatura del experimento de lecho fijo se estableció a temperatura ambiente (22°C). A continuación, la muestra se introdujo en el evaporador rotatorio para el proceso de eliminación del metanol. Los efluentes fueron recogidos y analizados. Los parámetros de entrada seleccionados para este diseño fueron la cantidad de resina, el caudal y la cantidad de disolventes. Se seleccionó una matriz ortogonal L9 estándar (OA) y se realizaron nueve estudios experimentales para optimizar el proceso. La matriz ortogonal L9 está pensada para comprender el efecto de factores independientes, cada uno de los cuales tiene valores de nivel de 3 factores. El diseño experimental de experimentos de Taguchi sugiere la matriz ortogonal L9, donde nueve experimentos son suficientes para optimizar los parámetros. Cada parámetro en tres niveles para este estudio se muestra en la Tabla 4. La Tabla 5 muestra las ejecuciones experimentales con diferentes combinaciones de parámetros en diferentes niveles.
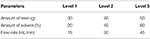
Tabla 4. Parámetros de funcionamiento y niveles.
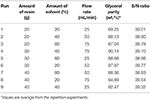
Tabla 5. Diseño experimental de matriz ortogonal L9 y resultados de los experimentos de intercambio iónico.
Métodos analíticos
Se utilizó la cromatografía de gases (GC) Agilent 6890 unida a un detector de ionización de llama (FID) para identificar la concentración de glicerol en las siguientes condiciones: (i) columna capilar (DB 5HT), 0,32 mm de diámetro interno, 15 m de longitud con 0,1 μm de película líquida, (ii) gas portador helio a 1,0 mL/min, y (iii) temperatura del inyector 200°C, y (iv) tiempo total de ejecución de 5 min. El contenido de agua del glicerol se midió utilizando el titulador Karl Fisher. Se utilizó el método estándar (ISO 2098-1972) para calcular el contenido de cenizas. El no-glicerol orgánico (MONG) del glicerol se midió restando la suma de los contenidos de glicerol, cenizas y agua, según el método estándar (ISO 2464-1973). Las determinaciones de pH para el glicerol crudo y purificado se llevaron a cabo utilizando un medidor de pH (Cyberscan pH 300, 19 Eutectic instruments).
Diseño de experimentos utilizando el método Taguchi
En este estudio, se utilizó el método Taguchi para diseñar y optimizar el proceso de purificación de glicerol crudo en dos etapas. Se utilizó el paquete de software Minitab 16 para ayudar al diseño de experimentos y al análisis estadístico en la determinación de las condiciones óptimas de funcionamiento. En este estudio, se utilizó el contenido de glicerol (wt.%) como parámetro para evaluar la efectividad del proceso de acidificación bajo diferentes condiciones de operación. Los datos obtenidos para cada experimento en OA se analizaron mediante la relación señal/ruido (S/N) para investigar el impacto de los factores influyentes y determinar la configuración óptima de los parámetros establecidos dentro del diseño experimental. La relación S/N puede optimizarse utilizando varios criterios, incluyendo el más grande-el mejor, el más pequeño-el mejor, o el nomina-el mejor.
En este estudio, se empleó el enfoque más grande-el mejor para evaluar la respuesta experimental para la purificación de glicerol. La relación S/N se calculó utilizando la ecuación (1) (Park, 1996; Sharma et al., 2005):
donde «n» representa el número total de réplicas de cada ensayo y Yi representa la pureza del glicerol en el experimento de réplica «i» realizado bajo las mismas condiciones experimentales de cada ensayo. Se calculó la relación S/N para cada experimento. Los parámetros significativos se identificaron en base a la relación S/N de la pureza del glicerol.
Análisis de medias
En este estudio, se utilizó el análisis de medias (ANOM) para determinar la condición óptima de funcionamiento del proceso de acidificación (Chary y Dastidar, 2012). La media de la relación S/N muestra el efecto de cada parámetro, independientemente. La media de la relación S/N se calculó promediando el valor de la relación S/N de todos los experimentos.
La media de la relación S/N de un parámetro individual «F» en el nivel «I» se calculó utilizando la ecuación (2):
Donde nFi es el número de apariciones del parámetro «F» en el nivel «i» y j representa la relación S/N del parámetro «F» en el nivel «i» en su jº valor (donde j = 1,2,3…, n).
Análisis de Varianza
El análisis de varianza (ANOVA) se llevó a cabo para evaluar estadísticamente el efecto de los diferentes parámetros en el rendimiento del proceso. El ANOVA se realizó calculando la suma de cuadrados (SS), la varianza (V), los grados de libertad (DOF), la relación de varianza (factor F) y el porcentaje de contribución (ρF). En el ANOVA, se investigó la significación de todos los parámetros y la interacción entre ellos mediante las ecuaciones que se indican a continuación. Según el método Taguchi, se utilizó el porcentaje de contribución de todos los parámetros estudiados para evaluar la influencia de cada parámetro en el proceso de acidificación e investigar qué parámetros afectaban significativamente a la respuesta del proceso mediante el análisis ANOVA (Roy, 2001). La contribución porcentual de cada parámetro, ρF, se calculó mediante la siguiente ecuación:
En la ecuación (3), Ve es la varianza debida al error, DOFF es el grado de libertad del parámetro estudiado, y se puede calcular restando uno al número de nivel del parámetro (L).
La suma de cuadrados debida al factor, SSF se calculó utilizando la Ecuación (4):
Lo cual, ηt = el total de la relación S/N de cada parámetro en ith nivel, ηi es la relación S/N de los resultados experimentales y m es el número de repetición de cada nivel del parámetro.
La TSM en la ecuación (3) se calculó utilizando la ecuación (5). SST es el total de cuadrados de la suma, N es el número de todas las observaciones,
La suma de cuadrados debida al error, SSe, se calculó mediante la Ecuación (6):
La varianza del parámetro, Vp se calculó mediante la Ecuación (7):
La razón de Fisher (F) que determina la significación de un parámetro se calculó mediante la Ecuación (8):
Experimentos de confirmación
Se realizó la prueba de confirmación para verificar las condiciones óptimas propuestas por el análisis ANOM y ANOVA. La pureza del glicerol y la relación S/N predichas se calcularon mediante la ecuación (9):
donde Ym = la media total de la relación S/N, Yi¯ = la relación S/N en el nivel óptimo, y k = el número de parámetros.
Resultados y discusión
Caracterización del glicerol crudo
El glicerol crudo era un líquido marrón oscuro con un pH de 9,6. Tiene un pH más alto en comparación con el glicerol comercial. El glicerol crudo contiene una pequeña cantidad de glicerol (46,8 % en peso), pero un alto contenido de cenizas, agua y MONG, como puede verse en la Tabla 6. Se observa que la principal impureza en el glicerol crudo es el contenido de MONG (50,4 % en peso). El MONG se compone de impurezas como el jabón, el alcohol y los ésteres metílicos en el glicerol de las etapas de procesamiento del biodiésel (Kongjao et al., 2010). Los ácidos grasos libres formados se liberarán como jabón soluble. Además, los ésteres metílicos quedarán suspendidos en la fase de glicerol durante el proceso de separación de fases (Kongjao et al., 2010). Estos compuestos orgánicos también pueden reaccionar con el exceso de catalizador alcalino, como el NaOH o el KOH, que permanece en la solución de glicerol para reformar el jabón. El contenido de cenizas (4,7 % en peso) se compone de materias inorgánicas procedentes de la utilización de catalizadores alcalinos como el NaOH y el KOH durante el proceso de transesterificación. El contenido de agua de 9,3 % en peso en la muestra de glicerol crudo puede deberse a la naturaleza higroscópica del glicerol, que absorbe la humedad de su entorno durante el proceso de transesterificación.

Tabla 6. Características del glicerol crudo obtenido de la producción de biodiésel y del glicerol comercial.
Acidificación
Se utilizó el método de Taguchi para estudiar el efecto de los parámetros sobre el rendimiento del proceso de acidificación e identificar la condición óptima de funcionamiento. Se utilizaron tres parámetros controlables (pH, temperatura y tiempo de reacción) con cada parámetro en tres niveles diferentes para diseñar el experimento. Sobre la base de los parámetros, niveles y grados de libertad seleccionados, se eligió un OA estándar L9. Basándose en el método Taguchi, los resultados de los experimentos se calcularon en términos de la relación S/N y luego se interpretaron. Las relaciones S/N miden las desviaciones de las características de calidad con respecto al valor deseado y calculan las condiciones óptimas (Karabas, 2013). El objetivo de este estudio es maximizar la pureza del glicerol. Por lo tanto, las características de calidad más altas son las más deseadas. Se utilizó la ecuación (1) para determinar la relación S/N. Las relaciones S/N de cada corrida experimental se obtuvieron sustituyendo los valores de pureza de glicerol y varias réplicas de cada corrida experimental «n» en la Ecuación (1).
Condiciones óptimas mediante el enfoque ANOM
ANOM se utiliza para identificar el efecto sobre los parámetros individuales e identificar la condición óptima para el proceso de acidificación (Chary y Dastidar, 2012). Este análisis se realizó promediando todas las relaciones S/N de ese parámetro particular utilizado en los experimentos. Se aplicó la ecuación (2) para calcular la media de la relación S/N y los valores obtenidos para cada experimento se presentan en la Tabla 7. Las condiciones óptimas de funcionamiento se determinaron en función de la máxima relación S/N en un determinado nivel. La media más alta de la relación S/N indica que el parámetro tiene un mayor efecto en el proceso de acidificación. Como puede verse en la Figura 1, las condiciones operativas óptimas para llevar a cabo la acidificación con el fin de obtener la máxima pureza del glicerol se identificaron como sigue: pH en el nivel 2 (2), temperatura de reacción en el nivel 3 (70°C) y tiempo de reacción en el nivel 2 (40 min). Los resultados obtenidos de ANOM se verificaron además mediante ANOVA.

Tabla 7. Tabla de respuesta de la media de las relaciones S/N para la pureza del glicerol.
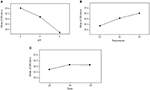
Figura 1. Valor medio de la relación S/N en el nivel 1-3 de cada parámetro: (A) efecto del pH, (B) efecto de la temperatura y (C) efecto del tiempo de reacción.
Efecto de los parámetros sobre la acidificación
La media de las relaciones S/N refleja el nivel de los parámetros sobre el proceso de acidificación. Como se muestra en la Figura 1, el pH es el parámetro dominante que afecta al proceso de acidificación y a la calidad del producto, seguido de la temperatura y el tiempo de reacción. Esto indica que el parámetro del pH afecta de forma crítica al proceso de acidificación y a la calidad del producto obtenido. La importancia de los parámetros también se obtuvo cuantitativamente a partir del ANOM. Se calculó calculando la desviación del valor más alto con respecto al valor más bajo. Se asignó el rango más alto al parámetro que presentaba el mayor valor de desviación. Una desviación grande indica una contribución significativa y el efecto de ese parámetro particular en el rendimiento del proceso de acidificación. Como se muestra en la Tabla 7, el pH fue el parámetro más significativo con una desviación de 2,32 y el tiempo de reacción fue el parámetro menos significativo con una desviación de 0,41.
Contribución porcentual de los parámetros mediante ANOVA
De acuerdo con el método Taguchi, se evaluó el porcentaje de contribución de cada parámetro para cuantificar con precisión el efecto del parámetro sobre la acidificación en términos de la pureza del glicerol (Roy, 2001). Los resultados del análisis ANOVA y las contribuciones porcentuales de cada parámetro se muestran en la Tabla 8. Se observó que el pH tuvo un efecto dominante en el proceso de acidificación, con una contribución porcentual del 76,37%. La contribución de los parámetros se encontró en el siguiente orden: pH (76,37%) > temperatura (19,44%) > tiempo de reacción (2,72%). Este resultado estuvo de acuerdo con los resultados obtenidos del análisis ANOM.

Tabla 8. Resultados del análisis ANOVA.
Experimentos de confirmación
El experimento de confirmación es un paso importante en el método de diseño de Taguchi. Este paso debe llevarse a cabo al final del estudio de optimización para verificar si las condiciones de funcionamiento optimizadas, que se identifican mediante ANOM, producen el resultado experimental deseado. La combinación de las condiciones operativas óptimas identificadas no se incluyó en las nueve ejecuciones experimentales del arreglo ortogonal. Por ello, se realizó un experimento de confirmación para el proceso de acidificación utilizando el valor optimizado de cada parámetro y se calculó la relación S/N. La pureza del glicerol se estimó utilizando la ecuación (9) y la comparación entre la pureza real y la predicha del glicerol se presenta en la Tabla 9. Como puede verse en la Tabla 9, la relación S/N obtenida a partir del experimento de confirmación está en buen acuerdo con las predicciones. Estos resultados mostraron que la optimización del proceso de acidificación para producir glicerol de la mayor pureza fue exitosa.

Tabla 9. Condiciones óptimas, valor real y predicho para la respuesta (pureza del glicerol).
Intercambio iónico
Se optimizaron tres parámetros controlables (cantidad de resina, cantidad de disolvente y caudal) con cada parámetro en tres niveles diferentes utilizando el diseño experimental de arreglos ortogonales de Taguchi. Basándose en el número de parámetros identificados, varios niveles y los grados de libertad, se seleccionó un OA estándar L9 en el presente estudio. Se realizaron un total de veintisiete ejecuciones experimentales basadas en el OA L9 con tres réplicas. Para cada serie experimental, se determinó la respuesta del proceso en términos de pureza del glicerol (wt.%) y se analizó posteriormente mediante el enfoque estadístico. Los datos recogidos sobre la pureza del glicerol se presentan en la Tabla 5. Según los resultados obtenidos, la pureza del glicerol (% en peso) de los experimentos varía entre 87,04 y 97,87 % en peso. Esto indica que el proceso de intercambio iónico depende de todos los parámetros controlables (cantidad de resina, cantidad de disolvente y velocidad de flujo), y este hallazgo se comprobó además mediante el análisis estadístico. Los resultados de los experimentos se convirtieron en la relación S/N. El objetivo de este estudio es maximizar la pureza del glicerol obtenido en el proceso de intercambio iónico. Por lo tanto, se utilizan características de mayor calidad para calcular la relación S/N.
Condiciones óptimas mediante el enfoque ANOM
La media de la relación S/N obtenida para el experimento se presenta en la Tabla 10. Las condiciones óptimas de funcionamiento se seleccionaron en función del valor máximo de la relación S/N a un determinado nivel de un parámetro. Un efecto más fuerte en el proceso de intercambio de iones se indica con una media más alta de la relación S/N. Por lo tanto, las condiciones óptimas de funcionamiento de los parámetros se obtuvieron en el nivel con la mayor media de las relaciones S/N. Como se muestra en la Figura 2, las condiciones operativas óptimas del proceso de intercambio iónico para alcanzar la máxima pureza del glicerol se identificaron como sigue: la cantidad de resina en el nivel 3 (40 g), el caudal en el nivel 1 (15 mL/min) y la cantidad de disolvente en el nivel 3 (60%). Los resultados obtenidos de ANOM se verificaron además mediante ANOVA.

Tabla 10. Tabla de respuesta de la media de las relaciones S/N para el intercambio de iones.
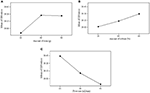
Figura 2. Valor medio de la relación S/N en el nivel 1-3 de cada parámetro: (A) efecto de la cantidad de resina, (B) efecto de la cantidad de disolvente y (C) efecto del caudal.
Efecto de los parámetros en el intercambio iónico
El rango de la media de las relaciones S/N refleja el nivel de influencia de los parámetros en el proceso de intercambio iónico. Como se muestra en la Figura 2, el caudal fue el parámetro dominante que afectaba al proceso de intercambio iónico y a la calidad del producto, seguido de la cantidad de resina y la cantidad de disolvente. La importancia de estos parámetros también se obtuvo cuantitativamente a partir del ANOM. Se determinó calculando la desviación del valor más alto respecto al más bajo. Se asignó el rango más alto al parámetro que presentaba el mayor valor de desviación. Una desviación sustancial indica una contribución significativa y el efecto de ese parámetro en particular en el rendimiento del proceso de intercambio de iones. Como se muestra en la Tabla 10, el caudal fue el parámetro que más contribuyó y la cantidad de disolvente fue el parámetro que menos contribuyó.
Porcentaje de contribución de los parámetros mediante ANOVA
Los resultados del ANOVA sobre la pureza del glicerol y el porcentaje de contribuciones de cada parámetro se presentan en la Tabla 11. Del resultado se desprende que la tasa de flujo exhibió un efecto dominante en el proceso de intercambio iónico con el porcentaje de contribución del 51,02%. La contribución de los parámetros en orden ascendente es la siguiente: caudal (51,02%) > cantidad de resina (28,42%) > cantidad de disolvente (12,33%). Los resultados experimentales estaban en buena concordancia con los resultados obtenidos del análisis ANOM.

Tabla 11. Resultados del análisis ANOVA para el proceso de intercambio iónico.
Experimento de confirmación
El modelo predijo un 96,91% de pureza de glicerol, y una relación S/N de 39,72 bajo las condiciones óptimas de 60% de disolvente, el caudal de 15 mL/min, y 40 g de resina. Los valores obtenidos experimentalmente se compararon con el valor predicho por el modelo para confirmar la validez del procedimiento de optimización en las condiciones de funcionamiento establecidas. El resultado muestra que se obtuvo una pureza máxima de glicerol (98,2%), y la relación S/N de 39,78 utilizando las condiciones operativas optimizadas. Los resultados de los experimentos de confirmación revelaron que el valor experimental real y la relación S/N obtenidos estaban en buena concordancia con los predichos. Por lo tanto, se puede concluir que la optimización del proceso de intercambio iónico para mejorar la pureza del glicerol fue exitosa.
Comparación de las características del glicerol purificado con otros trabajos
El resultado obtenido en este trabajo se ha comparado con estudios anteriores y se presenta en la Tabla 12. La tabla de comparación muestra que el método de purificación de doble paso compuesto por las técnicas de acidificación e intercambio iónico aplicadas en este trabajo produjo con éxito glicerol con la mayor pureza en comparación con otros trabajos. El porcentaje de glicerol crudo purificado obtenido en este estudio fue del 98%. Saifuddin et al. (2013) lograron un menor rendimiento de glicerol con una pureza del 93,1-94,2% utilizando tanto la acidificación como el tratamiento de adsorción en comparación con este trabajo. Además, nuestras técnicas de purificación en dos pasos fueron más eficaces y superiores en comparación con el tratamiento químico y físico utilizado por Manosak et al. (2011) y Kongjao et al. (2010) en términos de pureza del glicerol.

Tabla 12. Comparación de las características del glicerol purificado con otros trabajos.
Conclusión
El objetivo de este trabajo es la obtención de glicerol de alta pureza mediante el proceso de purificación en dos pasos con la ayuda de la herramienta de optimización Taguchi. El proceso de acidificación y seguido de intercambio iónico han producido glicerol con una pureza del 98,20 % en peso. En las condiciones optimizadas de pH (2), temperatura (70°C) y tiempo de reacción (40 min), el proceso de acidificación ha obtenido glicerol con una pureza del 76,18 % en peso. En el proceso de intercambio iónico, se utilizó el glicerol pretratado, que se obtuvo del proceso de acidificación con condiciones operativas optimizadas. En el proceso de intercambio iónico se ha obtenido glicerol con una pureza del 98,20% en peso en las condiciones optimizadas de 60% de disolvente, el caudal de 15 mL/min, y 40 g de resina. Los valores predichos por el método Taguchi se compararon con los resultados experimentales reales, y el resultado real coincidió con el resultado predicho. Se demuestra que Taguchi se aplicó con éxito para optimizar el paso de dos para la purificación del glicerol crudo derivado del biodiésel. Este estudio muestra una mejora en la pureza del glicerol de 35,60 a 98,20 % en peso tras la optimización de los procesos de acidificación e intercambio iónico, estando el contenido de glicerol en la cantidad aceptada en base a la norma BS 2621:1979.
Contribuciones de los autores
HT: diseño del trabajo, trabajo experimental, análisis e interpretación de los datos y redacción del manuscrito. AA: concepto del estudio, diseño del trabajo, y la revisión del manuscrito. AB: análisis e interpretación de los datos y redacción del manuscrito.
Conflicto de intereses
Los autores declaran que la investigación se llevó a cabo en ausencia de cualquier relación comercial o financiera que pudiera interpretarse como un potencial conflicto de intereses.
Agradecimientos
Los autores agradecen a la Universiti Malaya Research Grant (UMRG) – Frontier Science (AFR) RG384-17AFR Research Fund de la Universidad de Malaya por apoyar económicamente esta investigación.
Carmona, M., García, M. T., Alcázar, A., Carnicer, A., y Rodríguez, J. F. (2012). Combinación de procesos de intercambio iónico y adsorción de agua para obtener glicerol de alto grado a partir de biodiésel. J. Chem. Sci. Technol. 1, 14-20.
Google Scholar
Carmona, M. L., Valverde, J., Pérez, A., Warchol, J., y Juan Rodríguez, F. (2009). Purificación de soluciones de glicerol/agua de síntesis de biodiésel por intercambio iónico: eliminación de sodio Parte I. J. Chem. Technol. Biotechnol. 84, 738-744. doi: 10.1002/jctb.2106
CrossRef Full Text | Google Scholar
Chary, G. H. V. C., and Dastidar, M. G. (2012). Investigación de las condiciones óptimas en la aglomeración de carbón-aceite utilizando el diseño experimental de Taguchi. Fuel 98, 259-264. doi: 10.1016/j.fuel.2012.03.027
CrossRef Full Text | Google Scholar
Chol, C. G., Dhabhai, R., Dalai, A. K., and Reaney, M. (2018). Purificación del glicerol crudo derivado del proceso de producción de biodiésel: estudios experimentales y análisis tecno-económicos. Fuel Process. Technol. 178, 78-87. doi: 10.1016/j.fuproc.2018.05.023
CrossRef Full Text | Google Scholar
Corach, J., Galván, E. F., Sorichetti, P. A., y Romano, S. D. (2019). Estimación de la composición de mezclas de biodiésel y aceite de soja a partir de mediciones de permitividad. Fuel 235, 1309-1315. doi: 10.1016/j.fuel.2018.08.114
CrossRef Full Text | Google Scholar
da Silva César, A., Conejero, M. A., Barros Ribeiro, E. C., y Batalha, M. O. (2018). Análisis de competitividad de la «soja social» en la producción de biodiésel en Brasil. Renovar. Energy 133, 1147-1157. doi: 10.1016/j.renene.2018.08.108
CrossRef Full Text | Google Scholar
Dhabhai, R., Ahmadifeijani, E., Dalai, A. K., y Reaney, M. (2016). Purificación de glicerol crudo utilizando un tratamiento físico-químico secuencial, filtración por membrana y adsorción con carbón activado. Separat. Purificat. Technol. 168, 101-106. doi: 10.1016/j.seppur.2016.05.030
CrossRef Full Text | Google Scholar
Hajek, M., y Skopal, F. (2010). Tratamiento de la fase de glicerol formada por la producción de biodiésel. Bioresour. Technol. 101, 3242-3245. doi: 10.1016/j.biortech.2009.12.094
PubMed Abstract | CrossRef Full Text | Google Scholar
Karabas, H. (2013). Producción de biodiésel a partir de aceite crudo de bellota (Quercus frainetto L.): un proceso de optimización mediante el método Taguchi. Renew. Energy 53, 384-388. doi: 10.1016/j.renene.2012.12.002
CrossRef Full Text | Google Scholar
Kongjao, S., Damronglerd, S., y Hunsom, M. (2010). Purification of crude glycerol derived from waste used-oil methyl ester plant. Korean J. Chem. Eng. 27, 944-949. doi: 10.1007/s11814-010-0148-0
CrossRef Full Text | Google Scholar
Kovács, A., Czinkota, I., and Tóth, J. (2012). Improving acid number testing of biodiesel feedstock and product. J. Am. Oil Chem. Soc. 89, 409-417. doi: 10.1007/s11746-011-1929-2
CrossRef Full Text | Google Scholar
Lancrenon, X., and Fedders, J. (2008, June 2008). Una innovación en la purificación de la glicerina. Biodiesel Magazine.
Google Scholar
Manosak, R., Limpattayanate, S., y Hunsom, M. (2011). Sequential-refining of crude glycerol derived from waste used-oil methyl ester plant via a combined process of chemical and adsorption. Fuel Process. Technol. 92, 92-99. doi: 10.1016/j.fuproc.2010.09.002
CrossRef Full Text | Google Scholar
Monteiro, M. R., Kugelmeier, C. L., Pinheiro, R. S., Batalha, M. O., and da Silva César, A. (2018). Glicerol de la producción de biodiésel: caminos tecnológicos para la sostenibilidad. Renew. Sust. Energy Rev. 88, 109-122. doi: 10.1016/j.rser.2018.02.019
CrossRef Full Text | Google Scholar
Park, S. H. (1996). Diseño y análisis robusto para la ingeniería de la calidad. London: Chapman and Hall.
Google Scholar
Roy, R. K. (2001). Design of Experiments Using the Taguchi Approach: 16 Steps to Product and Process Inprovement. John Wiey and Sons.
Google Scholar
Saifuddin, N., Refal, H., y Kumaran, P. (2013). Rápida purificación del subproducto glicerol de la producción de biodiésel mediante un proceso combinado de acidificación asistida por microondas y adsorción a través de quitosano inmovilizado con teast. J. Appl. Sci. Eng. Technol. 7, 593-602. doi: 10.19026/rjaset.7.295
CrossRef Full Text | Google Scholar
Samul, D., Leja, K., y Grajek, W. (2014). Impurezas del glicerol crudo y su efecto en la producción de metabolitos. Ann. Microbiol. 64, 891-898. doi: 10.1007/s13213-013-0767-x
PubMed Abstract | CrossRef Full Text | Google Scholar
Sdrula, N. (2010). Un estudio utilizando la separación clásica o por membranas en el proceso de biodiésel. Desalination 250, 1070-1072. doi: 10.1016/j.desal.2009.09.110
CrossRef Full Text | Google Scholar
Sharma, P., Verma, A., Sidhu, R. K., and Pandey, O. P. (2005). Process parameter selection for strontium ferrite sintered magnets using Taguchi L9 orthogonal design. J. Mater. Process. Technol. 168, 147-151. doi: 10.1016/j.jmatprotec.2004.12.003
CrossRef Full Text | Google Scholar
Talebian-Kiakalaieh, A., Amin, N. A. S., Najaafi, N., y Tarighi, S. (2018). Una revisión sobre la acetalización catalítica de glicerol bio-renovable a aditivos de combustible. Front. Chem. 6:573. doi: 10.3389/fchem.2018.00573
PubMed Abstract | CrossRef Full Text | Google Scholar
Tan, H. W., Abdul Aziz, A. R., y Aroua, M. K. (2013). Producción de glicerol y sus aplicaciones como materia prima: una revisión. Renew. Sust. Energy Rev. 27, 118-127. doi: 10.1016/j.rser.2013.06.035
CrossRef Full Text | Google Scholar
Venkataramanan, K. P., Boatman, J. J., Kurniawan, Y., Taconi, K. A., Bothun, G. D., y Scholz, C. (2012). Impact of impurities in biodiesel-derived crude glycerol on the fermentation by Clostridium pasteurianum ATCC 6013. Appl. Microbiol. Biotechnol. 93, 1325-1335. doi: 10.1007/s00253-011-3766-5
PubMed Abstract | CrossRef Full Text | Google Scholar
Xiao, Y., Xiao, G., y Varma, A. (2013). Un procedimiento universal para la purificación de glicerol crudo a partir de diferentes materias primas en la producción de biodiésel: estudio experimental y de simulación. Ind. Eng. Chem. Res. 52, 14291-14296. doi: 10.1021/ie402003u
CrossRef Full Text | Google Scholar
Yang, F., Hanna, M. A., y Sun, R. (2012). Usos de valor añadido para el glicerol crudo-un subproducto de la producción de biodiésel. Biotechnol. Biofuels 5, 1-10. doi: 10.1186/1754-6834-5-13
PubMed Abstract | CrossRef Full Text | Google Scholar
