- Introduction
- Matériaux, produits chimiques et méthodes
- Matériaux
- Procédé de purification du glycérol
- Première étape : Acidification
- Deuxième étape : Échange d’ions
- Méthodes analytiques
- Design of Experiments Using the Taguchi Method
- Analyse de la moyenne
- Analyse de la variance
- Expériences de confirmation
- Résultats et discussion
- Caractérisation du glycérol brut
- Acidification
- Conditions optimales par l’approche ANOM
- Effet des paramètres sur l’acidification
- Contribution en pourcentage des paramètres par ANOVA
- Expériences de confirmation
- Échange d’ions
- Conditions optimales par l’approche ANOM
- Effet des paramètres sur l’échange d’ions
- Pourcentage de contribution des paramètres par ANOVA
- Expérience de confirmation
- Comparaison de la caractéristique du glycérol purifié avec d’autres travaux
- Conclusion
- Contributions des auteurs
- Conflit d’intérêt
- Remerciements
Introduction
Le biodiesel est un carburant biodégradable et renouvelable produit par transestérification à partir de sources renouvelables telles que le soja, les microalgues, l’huile de cuisson de palme et le jatropha (da Silva César et al., 2018 ; Corach et al., 2019). Récemment, le biodiesel attire de nombreux chercheurs car il est l’un des biocarburants les plus couramment explorés qui pourrait réduire la dépendance mondiale aux combustibles fossiles et l’effet de serre. La production de biodiesel est estimée augmenter annuellement de 4,5% et atteindre 41 Mm3 en 2022 (Monteiro et al., 2018).
Le glycérol brut est le principal sous-produit produit lors du processus de transestérification dans l’usine de biodiesel, avec la génération de 10 % en poids du produit biodiesel (Samul et al., 2014). D’après l’analyse, environ 1 kg de glycérol brut est généré pour chaque 10 kg de production de biodiesel (Hajek et Skopal, 2010 ; Tan et al., 2013 ; Chol et al., 2018). La valeur marchande actuelle du glycérol pur est de 0,27 à 0,41 USD par livre ; cependant, le glycérol brut avec une pureté de 80 % est aussi bas que 0,04 à 0,09 USD par livre. Cela prouve que la production excessive de glycérol affecte le prix du glycérol sur le marché. Par conséquent, l’utilisation du glycérol brut pour les produits à valeur ajoutée est devenue une question sérieuse dans l’industrie du biodiesel.
Le glycérol à haute pureté a une large application dans diverses industries telles que les produits pharmaceutiques, cosmétiques et alimentaires. Cependant, le pourcentage de pureté du glycérol issu de l’industrie du biodiesel limite sa conversion en un produit de haute valeur (Samul et al, 2014 ; Talebian-Kiakalaieh et al, 2018). Le glycérol brut contient un grand nombre de contaminants tels que du savon, des sels, de l’éthanol, du méthanol, de l’eau, des acides gras, des esters méthyliques, des glycérides et des cendres (Tan et al., 2013 ; Dhabhai et al., 2016). Yang et al. (2012) ont déclaré que les impuretés présentes dans le glycérol brut pouvaient grandement influencer sa conversion en d’autres produits à valeur ajoutée (Yang et al., 2012). Venkataramanan et al. (2012) ont également indiqué que les savons présents dans le glycérol brut ont un fort effet inhibiteur sur l’utilisation du glycérol par les bactéries, ce qui affecte la performance du glycérol brut comme source de carbone dans le processus de fermentation (Venkataramanan et al., 2012). En conclusion, les impuretés présentes dans le glycérol brut créent un défi important pour les convertir en un produit à valeur ajoutée. Par conséquent, il est important de purifier le glycérol brut pour éviter la saturation du marché et augmenter les profits de la production de biodiesel.
Dans la littérature, les procédés les plus couramment utilisés sont la distillation, la résine échangeuse d’ions, la technologie de séparation par membrane, l’acidification, suivie de la neutralisation et de l’extraction par solvant. L’acidification est une technique couramment utilisée pour neutraliser les impuretés comme le catalyseur en sel inorganique. Outre l’acidification, elle permet également de réduire la quantité de savons en les transformant en acides gras libres insolubles, car ils peuvent avoir un impact négatif sur la séparation et entraîner une perte de rendement (Hajek et Skopal, 2010 ; Kovács et al., 2012). Comme le processus d’acidification n’élimine pas toutes les impuretés, il nécessite une étape de purification supplémentaire pour éliminer d’autres impuretés comme le méthanol, l’huile, l’eau et l’ester. Cependant, le processus de distillation présente certaines limites par rapport aux autres, car il nécessite un apport énergétique élevé pour la vaporisation et provoque des décompositions thermiques (Lancrenon et Fedders, 2008). En outre, un vide élevé est également nécessaire dans la distillation pour éviter la dénaturation à haute température du glycérol par la formation d’acroléine (Manosak et al., 2011). En outre, ce procédé implique un investissement en capital et un coût de maintenance élevés, accompagnés de pertes considérables de glycérol (Sdrula, 2010). Par rapport au procédé de distillation, le procédé d’échange d’ions est de plus en plus accepté en raison de la simplicité de son fonctionnement, de sa faible consommation d’énergie et de ses besoins énergétiques, ainsi que du fait qu’il s’est également avéré efficace pour éliminer les traces d’impuretés, la couleur et l’odeur (Carmona et al., 2009, 2012). En outre, Xiao et al. (2013) ont suggéré que le processus de purification en plusieurs étapes du glycérol brut pourrait augmenter la pureté le rendre viable pour divers usages (Xiao et al., 2013).
Cette étude vise à obtenir du glycérol brut avec la plus grande pureté via une purification en deux étapes utilisant des techniques d’acidification et d’échange d’ions, avec l’aide de la méthode Taguchi. Dans cette étude, l’analyse statistique, y compris un réseau orthogonal L9 de Taguchi, le rapport signal/bruit, l’analyse de la moyenne, l’analyse de la variance et les analyses de régression ont été utilisés pour identifier les conditions optimales des processus de purification.
Matériaux, produits chimiques et méthodes
Matériaux
Le glycérol brut a été collecté à partir d’une usine locale de biodiesel, en Malaisie. Une résine échangeuse de cations forts H+, Amberlyst 15 a été achetée auprès de Sigma Aldrich Sdn. Bhd. Les propriétés de la résine sont indiquées dans le tableau 1. L’acide phosphorique (85 % en poids), les pastilles d’hydroxyde de sodium et le méthanol ont été achetés chez Merck Sdn. Bhd. De l’eau distillée a été utilisée pour la préparation des solutions chimiques.

Tableau 1. Propriétés des résines échangeuses de cations.
Procédé de purification du glycérol
Première étape : Acidification
Le glycérol brut a été prétraité sur la base de la procédure adoptée de Manosak et al. (2011). Les expériences ont été menées dans les flacons Erlenmeyer de 500 ml et équilibrées à l’aide d’un agitateur magnétique. Initialement, le glycérol brut a été acidifié à l’aide d’acide phosphorique jusqu’à la valeur de pH souhaitée, puis agité à un taux constant de 200 rpm pendant 1 h. La solution a ensuite été laissée au repos pour la séparation des phases. Elle a été séparée en trois couches qui sont respectivement des couches d’acide gras libre, de glycérol et de sel inorganique. La première couche, riche en acide gras a été séparée par décantation, et le sel précipité a été éliminé par filtrations à l’aide d’un filtre de 0,45 μm. La couche intermédiaire, qui est riche en glycérol, a été neutralisée (pH 7) par l’ajout de NaOH. Les sels inorganiques et d’acides gras qui se sont formés lors de l’étape de neutralisation ont été éliminés par un filtre de 0,45 μm. Les paramètres d’entrée sélectionnés pour cette conception étaient le pH, la température et le temps de réaction, désignés respectivement comme paramètres A, B et C (tableau 2). Le tableau orthogonal L9 a été utilisé pour concevoir les expériences dans ce travail (tableau 3).
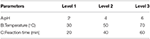
Tableau 2. Paramètres et niveaux de fonctionnement.
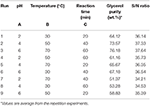
Tableau 3. Plan expérimental à réseau orthogonal L9 et résultats des expériences d’acidification.
Deuxième étape : Échange d’ions
Dans le processus d’échange d’ions, le glycérol prétraité obtenu à partir du processus d’acidification avec des conditions de fonctionnement optimisées a été utilisé. Les résines échangeuses d’ions ont été étudiées en faisant passer l’alimentation à travers une colonne de 300 ml de résine supportée dans un tube de verre. Des résines échangeuses d’ions de type Amberlyst 15 sous forme hydrogène ont été utilisées pour l’élimination des ions libres. La résine a été préalablement gonflée avec du méthanol (25 % en poids) dans un récipient en verre et introduite dans la colonne. En outre, des billes de silice ont également été placées dans la colonne pour éliminer l’excès d’humidité. Les résines échangeuses d’ions ont été utilisées pour adsorber les anions et les cations libres dans le glycérol prétraité. Le glycérol prétraité a ensuite été chargé dans le réservoir d’alimentation, et une pompe a été utilisée pour faire circuler le glycérol brut à travers le lit de résine échangeuse d’ions aux conditions de fonctionnement prédéterminées. La température de l’expérience à lit fixe a été réglée à la température ambiante (22°C). Ensuite, l’échantillon a été placé dans l’évaporateur rotatif pour le processus d’élimination du méthanol. Les effluents ont été collectés et analysés. Les paramètres d’entrée sélectionnés pour cette conception étaient la quantité de résine, le débit et la quantité de solvants. Un réseau orthogonal (OA) standard L9 a été sélectionné, et neuf études expérimentales ont été réalisées pour optimiser le processus. Le tableau orthogonal L9 est destiné à comprendre l’effet de facteurs indépendants, chacun ayant des valeurs de niveau de 3 facteurs. Le plan d’expériences de Taguchi suggère un tableau orthogonal L9, où neuf expériences sont suffisantes pour optimiser les paramètres. Chaque paramètre à trois niveaux pour cette étude est présenté dans le tableau 4. Le tableau 5 montre les parcours expérimentaux avec différentes combinaisons de paramètres à différents niveaux.
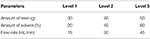
Tableau 4. Paramètres de fonctionnement et niveaux.
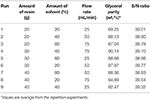
Tableau 5. Plan expérimental à réseau orthogonal L9 et résultats des expériences d’échange d’ions.
Méthodes analytiques
La chromatographie en phase gazeuse (GC) Agilent 6890 attachée à un détecteur à ionisation de flamme (FID) a été utilisée pour identifier la concentration de glycérol dans les conditions suivantes : (i) colonne capillaire (DB 5HT), diamètre interne de 0,32 mm, longueur de 15 m avec un film liquide de 0,1 μm, (ii) gaz porteur hélium à 1,0 mL/min, et (iii) température de l’injecteur 200°C, et (iv) durée totale de fonctionnement de 5 min. La teneur en eau du glycérol a été mesurée à l’aide d’un titrateur Karl Fisher. La méthode standard (ISO 2098-1972) a été utilisée pour calculer la teneur en cendres. Le non-glycérol organique (MONG) du glycérol a été mesuré en soustrayant la somme des teneurs en glycérol, en cendres et en eau selon la méthode standard (ISO 2464-1973). Les déterminations du pH du glycérol brut et purifié ont été effectuées à l’aide d’un pH-mètre (Cyberscan pH 300, 19 Eutectic instruments).
Design of Experiments Using the Taguchi Method
Dans cette étude, la méthode Taguchi a été utilisée pour concevoir et optimiser le procédé de purification en deux étapes du glycérol brut. Le progiciel Minitab 16 a été utilisé pour assister la conception des expériences et l’analyse statistique dans la détermination des conditions d’exploitation optimales. Dans cette étude, la teneur en glycérol (% en poids) a été utilisée comme paramètre pour évaluer l’efficacité du processus d’acidification dans différentes conditions de fonctionnement. Les données obtenues pour chaque expérience en OA ont été analysées par le rapport signal/bruit (rapport S/N) afin d’étudier l’impact des facteurs influents et de déterminer la configuration optimale des paramètres fixés dans le cadre du plan expérimental. Le rapport S/N peut être optimisé en utilisant plusieurs critères, y compris le plus grand-le meilleur, le plus petit-le meilleur, ou le nomina-le meilleur.
Dans cette étude, l’approche plus grande-le meilleur a été employée pour évaluer la réponse expérimentale pour la purification du glycérol. Le rapport S/N a été calculé à l’aide de l’équation (1) (Park, 1996 ; Sharma et al., 2005) :
où « n » représente le nombre total de réplications de chaque essai et Yi représente la pureté du glycérol dans l’expérience de réplication « i » réalisée dans les mêmes conditions expérimentales de chaque essai. Le rapport S/N a été calculé pour chaque expérience. Les paramètres significatifs ont été identifiés en fonction du rapport S/N de la pureté du glycérol.
Analyse de la moyenne
Dans cette étude, l’analyse de la moyenne (ANOM) a été utilisée pour déterminer la condition de fonctionnement optimale du processus d’acidification (Chary et Dastidar, 2012). La moyenne du rapport S/N montre l’effet de chaque paramètre, indépendamment. La moyenne du rapport S/N a été calculée en faisant la moyenne de la valeur du rapport S/N de toutes les expériences.
La moyenne du rapport S/N d’un paramètre individuel « F » au niveau « I » a été calculée en utilisant l’équation (2) :
Où nFi est le nombre d’apparitions du paramètre « F » au niveau « i » et j représente le rapport S/N du paramètre « F » au niveau « i » dans sa jème valeur (où j = 1,2,3…, n).
Analyse de la variance
L’analyse de la variance (ANOVA) a été effectuée pour évaluer statistiquement l’effet des différents paramètres sur la performance du procédé. L’ANOVA a été réalisée en calculant la somme des carrés (SS), la variance (V), les degrés de liberté (DOF), le rapport de variance (facteur F) et le pourcentage de contribution (ρF). Dans l’ANOVA, la signification de tous les paramètres et de l’interaction entre les paramètres a été étudiée à l’aide des équations énumérées ci-dessous. Selon la méthode Taguchi, le pourcentage de contribution de tous les paramètres étudiés a été utilisé pour évaluer l’influence de chaque paramètre sur le processus d’acidification et pour rechercher quels paramètres ont affecté de manière significative la réponse du processus par l’analyse ANOVA (Roy, 2001). Le pourcentage de contribution de chaque paramètre, ρF, a été calculé à l’aide de l’équation ci-dessous :
Dans l’équation (3), Ve est la variance due à l’erreur, DOFF est le degré de liberté du paramètre étudié, et il peut être calculé en soustrayant un du nombre de niveau du paramètre (L).
Les sommes des carrés dus au facteur, SSF ont été calculées en utilisant l’équation (4) :
Ceci, ηt = le total du rapport S/N de chaque paramètre dans le ie niveau, ηi est le rapport S/N des résultats expérimentaux et m est le nombre de répétitions de chaque niveau du paramètre.
La SST dans l’équation (3) a été calculée en utilisant l’équation (5). SST est le total de la somme des carrés, N est le nombre de toutes les observations,
La somme des carrés dus à l’erreur, SSe, a été calculée par l’équation (6) :
La variance du paramètre, Vp, a été calculée par l’équation (7) :
Le ratio de Fisher (F) qui détermine la significativité d’un paramètre a été calculé par l’équation (8) :
Expériences de confirmation
Un test de confirmation a été effectué pour vérifier les conditions optimales proposées par l’analyse ANOM et ANOVA. La pureté du glycérol et le rapport S/N prédits ont été calculés à l’aide de l’équation (9) :
où Ym = La moyenne totale du rapport S/N, Yi¯ = le rapport S/N au niveau optimal, et k = le nombre de paramètres.
Résultats et discussion
Caractérisation du glycérol brut
Le glycérol brut était un liquide brun foncé avec un pH de 9,6. Il a un pH plus élevé par rapport au glycérol commercial. Le glycérol brut contient une petite quantité de glycérol (46,8 % en poids), mais une teneur élevée en cendres, en eau et en MONG, comme on peut le voir dans le tableau 6. On constate que la principale impureté du glycérol brut est la teneur en MONG (50,4 % en poids). Le MONG est composé d’impuretés telles que le savon, l’alcool et les esters méthyliques dans le glycérol provenant des étapes de traitement du biodiesel (Kongjao et al., 2010). Les acides gras libres formés seront libérés sous forme de savon soluble. De plus, les esters méthyliques seront en suspension dans la phase glycérol pendant le processus de séparation des phases (Kongjao et al., 2010). Ces composés organiques peuvent également réagir avec l’excès de catalyseur alcalin tel que NaOH ou KOH, qui reste dans la solution de glycérol pour reformer le savon. La teneur en cendres (4,7 % en poids) est composée de matières inorganiques provenant de l’utilisation de catalyseurs alcalins comme le NaOH et le KOH pendant le processus de transestérification. La teneur en eau de 9,3 % en poids dans l’échantillon de glycérol brut est peut-être due à la nature hygroscopique du glycérol qui absorbe l’humidité environnante pendant le processus de transestérification.

Tableau 6. Caractéristiques du glycérol brut obtenu à partir de la production de biodiesel et du glycérol commercial.
Acidification
La méthode de Taguchi a été utilisée pour étudier l’effet des paramètres sur la performance du processus d’acidification et identifier la condition de fonctionnement optimale. Trois paramètres contrôlables (pH, température et temps de réaction) avec chaque paramètre à trois niveaux différents ont été utilisés pour concevoir l’expérience. Sur la base des paramètres, des niveaux et des degrés de liberté sélectionnés, un OA standard L9 a été choisi. Sur la base de la méthode de Taguchi, les résultats des expériences ont été calculés en termes de rapport S/N, puis interprétés. Les rapports S/N mesurent les déviations des caractéristiques de qualité par rapport à la valeur souhaitée et calculent les conditions optimales (Karabas, 2013). L’objectif de cette étude est de maximiser la pureté du glycérol. Ainsi, des caractéristiques de qualité plus élevées sont mieux souhaitées. L’équation (1) a été utilisée pour déterminer le rapport S/N. Les rapports S/N de chaque série expérimentale ont été obtenus en substituant les valeurs de la pureté du glycérol et plusieurs répétitions de chaque série expérimentale « n » dans l’équation (1).
Conditions optimales par l’approche ANOM
L’ANOM est utilisé pour identifier l’effet sur les paramètres individuels et identifier la condition optimale pour le processus d’acidification (Chary et Dastidar, 2012). Cette analyse a été effectuée en faisant la moyenne de tous les rapports S/N de ce paramètre particulier utilisé dans les expériences. L’équation (2) a été appliquée pour calculer la moyenne du rapport S/N et les valeurs obtenues pour chaque expérience sont présentées dans le tableau 7. Les conditions de fonctionnement optimales ont été déterminées sur la base du rapport S/N maximum à un certain niveau. Une moyenne plus élevée du rapport S/N indique que le paramètre a un effet plus fort sur le processus d’acidification. Comme on peut le voir sur la figure 1, les conditions opératoires optimales pour réaliser l’acidification afin d’obtenir la pureté maximale du glycérol ont été identifiées comme suit : pH au niveau 2 (2), température de réaction au niveau 3 (70°C) et temps de réaction au niveau 2 (40 min). Les résultats obtenus par l’ANOM ont été vérifiés par l’ANOVA.

Tableau 7. Tableau de réponse de la moyenne des rapports S/N pour la pureté du glycérol.
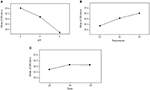
Figure 1. Valeur moyenne du rapport S/N au niveau 1-3 de chaque paramètre : (A) effet du pH, (B) effet de la température, et (C) effet du temps de réaction.
Effet des paramètres sur l’acidification
La moyenne des rapports S/N reflète le niveau des paramètres sur le processus d’acidification. Comme le montre la figure 1, le pH est le paramètre dominant qui affecte le processus d’acidification et la qualité du produit, suivi par la température et le temps de réaction. Ceci indique que le paramètre du pH est affecté de manière critique par le processus d’acidification et la qualité du produit obtenu. L’importance des paramètres a également été obtenue quantitativement à partir d’ANOM. Elle a été calculée en calculant l’écart entre la valeur la plus élevée et la valeur la plus faible. Le rang le plus élevé a été attribué au paramètre qui présentait la plus grande valeur d’écart. Un écart important indique une contribution et un effet significatifs de ce paramètre particulier sur la performance du processus d’acidification. Comme le montre le tableau 7, le pH était le paramètre le plus significatif avec un écart de 2,32 et le temps de réaction était le paramètre le moins significatif avec un écart de 0,41.
Contribution en pourcentage des paramètres par ANOVA
Selon la méthode Taguchi, le pourcentage contribué par chaque paramètre a été évalué pour quantifier précisément l’effet du paramètre sur l’acidification en termes de pureté du glycérol (Roy, 2001). Les résultats de l’analyse ANOVA et les contributions en pourcentage de chaque paramètre sont présentés dans le tableau 8. Il a été observé que le pH avait un effet dominant sur le processus d’acidification, avec une contribution en pourcentage de 76,37 %. La contribution des paramètres a été trouvée dans l’ordre suivant : pH (76,37%) > température (19,44%) > temps de réaction (2,72%). Ce résultat était en accord avec les résultats obtenus par l’analyse ANOM.

Tableau 8. Résultats de l’analyse ANOVA.
Expériences de confirmation
L’expérience de confirmation est une étape importante de la méthode de conception Taguchi. Cette étape doit être réalisée à la fin de l’étude d’optimisation pour vérifier si les conditions de fonctionnement optimisées, qui sont identifiées à l’aide de l’ANOM, produisent les résultats expérimentaux souhaités. La combinaison des conditions de fonctionnement optimales identifiées n’a pas été incluse dans les neuf séries expérimentales du réseau orthogonal. Ainsi, une expérience de confirmation a été réalisée pour le processus d’acidification en utilisant la valeur optimisée de chaque paramètre et le rapport S/N a été calculé. La pureté du glycérol a été estimée en utilisant l’équation (9) et la comparaison entre la pureté réelle et prédite du glycérol est présentée dans le tableau 9. Comme on peut le voir dans le tableau 9, le rapport S/N obtenu à partir de l’expérience de confirmation est en bon accord avec les prédictions. Ces résultats montrent que l’optimisation du procédé d’acidification pour obtenir un glycérol de la plus grande pureté a été réussie.

Tableau 9. Conditions optimales, valeur réelle et prédite pour la réponse (pureté du glycérol).
Échange d’ions
Trois paramètres contrôlables (quantité de résine, quantité de solvant et débit) avec chaque paramètre à trois niveaux différents ont été optimisés en utilisant le plan expérimental des réseaux orthogonaux de Taguchi. Sur la base du nombre de paramètres identifiés, de plusieurs niveaux et des degrés de liberté, un OA standard L9 a été sélectionné dans l’étude actuelle. Au total, vingt-sept séries expérimentales ont été menées sur la base du plan d’expérience L9 avec trois répétitions. Pour chaque cycle expérimental, la réponse du procédé en termes de pureté du glycérol (% en poids) a été déterminée et analysée par l’approche statistique. Les données recueillies sur la pureté du glycérol sont présentées dans le tableau 5. D’après les résultats obtenus, la pureté du glycérol (% en poids) des expériences varie de 87,04 à 97,87 % en poids. Cela indique que le processus d’échange d’ions dépend de tous les paramètres contrôlables (quantité de résine, quantité de solvant et débit), ce qui a été confirmé par l’analyse statistique. Les résultats des expériences ont été convertis en rapport S/N. Cette étude vise à maximiser la pureté du glycérol obtenu par le procédé d’échange d’ions. Ainsi, des caractéristiques de qualité supérieure sont utilisées pour calculer le rapport S/N.
Conditions optimales par l’approche ANOM
La moyenne du rapport S/N obtenu pour l’expérience est présentée dans le tableau 10. Les conditions optimales de fonctionnement ont été sélectionnées sur la base de la valeur maximale du rapport S/N à un certain niveau d’un paramètre. Un effet plus fort sur le processus d’échange d’ions est indiqué par une moyenne du rapport S/N plus élevée. Par conséquent, les conditions de fonctionnement optimales pour les paramètres ont été obtenues au niveau présentant la plus grande moyenne de rapports S/N. Comme le montre la figure 2, les conditions de fonctionnement optimales du procédé d’échange d’ions pour obtenir la pureté maximale du glycérol ont été identifiées comme suit : la quantité de résine au niveau 3 (40 g), le débit au niveau 1 (15 mL/min) et la quantité de solvant au niveau 3 (60 %). Les résultats obtenus à partir de l’ANOM ont été ensuite vérifiés par ANOVA.

Tableau 10. Tableau de réponse de la moyenne des rapports S/N pour l’échange d’ions.
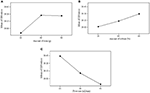
Figure 2. Valeur moyenne du rapport S/N au niveau 1-3 de chaque paramètre : (A) effet de la quantité de résine, (B) effet de la quantité de solvant, et (C) effet du débit.
Effet des paramètres sur l’échange d’ions
La plage de la moyenne des rapports S/N reflète le niveau d’influence des paramètres sur le processus d’échange d’ions. Comme le montre la figure 2, le débit était le paramètre dominant affectant le processus d’échange d’ions et la qualité du produit, suivi par la quantité de résine et la quantité de solvant. L’importance de ces paramètres a également été obtenue quantitativement à partir d’ANOM. Elle a été déterminée en calculant l’écart entre la valeur la plus élevée et la valeur la plus faible. Le rang le plus élevé a été attribué au paramètre présentant la plus grande valeur d’écart. Une déviation substantielle indique une contribution et un effet significatifs de ce paramètre particulier sur la performance du processus d’échange d’ions. Comme le montre le tableau 10, le débit était le principal paramètre contributif et la quantité de solvant était le paramètre le moins contributif.
Pourcentage de contribution des paramètres par ANOVA
Les résultats de l’ANOVA sur la pureté du glycérol et le pourcentage des contributions de chaque paramètre sont présentés dans le tableau 11. Il est clair d’après le résultat que le débit a présenté un effet dominant sur le processus d’échange d’ions avec le pourcentage de contribution de 51,02%. La contribution des paramètres par ordre croissant est la suivante : débit (51,02%) > quantité de résine (28,42%) > quantité de solvant (12,33%). Les résultats expérimentaux étaient en bon accord avec les résultats obtenus par l’analyse ANOM.

Tableau 11. Résultats de l’analyse ANOVA pour le procédé d’échange d’ions.
Expérience de confirmation
Le modèle a prédit 96,91% de pureté du glycérol, et un rapport S/N de 39,72 dans les conditions optimales de 60% de solvant, le débit de 15 mL/min, et 40 g de résine. Les valeurs obtenues expérimentalement ont été comparées à la valeur prédite par le modèle pour confirmer la validité de la procédure d’optimisation dans les conditions de fonctionnement établies. Le résultat montre qu’une pureté maximale du glycérol (98,2 %) et un rapport S/N de 39,78 ont été obtenus en utilisant les conditions de fonctionnement optimisées. Les résultats des expériences de confirmation ont révélé que la valeur expérimentale réelle et le rapport S/N obtenus étaient en bon accord avec les valeurs prédites. Par conséquent, on peut conclure que l’optimisation du procédé d’échange d’ions pour améliorer la pureté du glycérol a été réussie.
Comparaison de la caractéristique du glycérol purifié avec d’autres travaux
Le résultat obtenu dans ce travail a été comparé avec les études précédentes et présenté dans le tableau 12. Le tableau de comparaison montre que la méthode de purification en deux étapes comprenant les techniques d’acidification et d’échange d’ions appliquée dans ce travail a produit avec succès du glycérol avec la plus grande pureté par rapport aux autres travaux. Le pourcentage de glycérol brut purifié obtenu dans cette étude était de 98%. Saifuddin et al. (2013) ont obtenu un rendement inférieur de glycérol avec une pureté de 93,1-94,2% en utilisant à la fois l’acidification et le traitement par adsorption par rapport à ce travail. En outre, nos techniques de purification en deux étapes étaient plus efficaces et supérieures par rapport au traitement chimique et physique utilisé par Manosak et al. (2011) et Kongjao et al. (2010) en termes de pureté du glycérol.

Tableau 12. Comparaison des caractéristiques du glycérol purifié avec d’autres travaux.
Conclusion
Le but de ce travail est d’obtenir un glycérol de haute pureté par le processus de purification en deux étapes à l’aide de l’outil d’optimisation Taguchi. Le processus d’acidification et suivi par l’échange d’ions ont produit du glycérol avec la pureté de 98,20 % en poids. Dans les conditions optimisées de pH (2), de température (70°C) et de temps de réaction (40 min), le processus d’acidification a permis d’obtenir du glycérol d’une pureté de 76,18 % en poids. Dans le procédé d’échange d’ions, le glycérol prétraité, qui a été obtenu à partir du procédé d’acidification avec des conditions de fonctionnement optimisées, a été utilisé. Le procédé d’échange d’ions a permis d’obtenir du glycérol d’une pureté de 98,20 % en poids dans les conditions optimisées suivantes : 60 % de solvant, débit de 15 mL/min et 40 g de résine. Les valeurs prédites par la méthode Taguchi ont été comparées à celles des résultats expérimentaux réels, et le résultat réel s’est avéré être en bon accord avec le résultat prédit. Cela démontre que la méthode Taguchi a été appliquée avec succès pour optimiser la purification en deux étapes du glycérol brut dérivé du biodiesel. Cette étude montre une amélioration de la pureté du glycérol de 35,60 à 98,20 % en poids après l’optimisation des processus d’acidification et d’échange d’ions, la teneur en glycérol étant dans la quantité acceptée sur la base de BS 2621:1979.
Contributions des auteurs
HT : conception du travail, travail expérimental, analyse et interprétation des données, et rédaction du manuscrit. AA : concept de l’étude, conception du travail, et révision du manuscrit. AB : analyse et interprétation des données et rédaction du manuscrit.
Conflit d’intérêt
Les auteurs déclarent que la recherche a été menée en l’absence de toute relation commerciale ou financière qui pourrait être interprétée comme un conflit d’intérêt potentiel.
Remerciements
Les auteurs sont reconnaissants à l’Universiti Malaya Research Grant (UMRG) – Frontier Science (AFR) RG384-17AFR Research Fund de l’Université de Malaya pour avoir soutenu financièrement cette recherche.
Carmona, M., Garcia, M. T., Alcazar, A., Carnicer, A., et Rodriguez, J. F. (2012). Combinaison des processus d’échange d’ions et d’adsorption d’eau pour un glycérol de haute qualité à partir de biodiesel. J. Chem. Sci. Technol. 1, 14-20.
Google Scholar
Carmona, M. L., Valverde, J., Perez, A., Warchol, J., et Juan Rodriguez, F. (2009). Purification des solutions glycérol/eau provenant de la synthèse du biodiesel par échange d’ions : élimination du sodium Partie I. J. Chem. Technol. Biotechnol. 84, 738-744. doi : 10.1002/jctb.2106
CrossRef Full Text | Google Scholar
Chary, G. H. V. C., et Dastidar, M. G. (2012). Enquête sur les conditions optimales de l’agglomération charbon-huile en utilisant le plan d’expérience Taguchi. Fuel 98, 259-264. doi : 10.1016/j.fuel.2012.03.027
CrossRef Full Text | Google Scholar
Chol, C. G., Dhabhai, R., Dalai, A. K., et Reaney, M. (2018). Purification du glycérol brut dérivé du processus de production de biodiesel : études expérimentales et analyses technico-économiques. Fuel Process. Technol. 178, 78-87. doi : 10.1016/j.fuproc.2018.05.023
CrossRef Full Text | Google Scholar
Corach, J., Galván, E. F., Sorichetti, P. A., et Romano, S. D. (2019). Estimation de la composition des mélanges de biodiesel de soja / huile de soja à partir de mesures de permittivité. Fuel 235, 1309-1315. doi : 10.1016/j.fuel.2018.08.114
CrossRef Full Text | Google Scholar
da Silva César, A., Conejero, M. A., Barros Ribeiro, E. C., et Batalha, M. O. (2018). Analyse de la compétitivité du « soja social » dans la production de biodiesel au Brésil. Renew. Energy 133, 1147-1157. doi : 10.1016/j.renene.2018.08.108
CrossRef Full Text | Google Scholar
Dhabhai, R., Ahmadifeijani, E., Dalai, A. K., et Reaney, M. (2016). Purification du glycérol brut en utilisant un traitement physico-chimique séquentiel, une filtration sur membrane et une adsorption sur charbon actif. Separat. Purificat. Technol. 168, 101-106. doi : 10.1016/j.seppur.2016.05.030
CrossRef Full Text | Google Scholar
Hajek, M., et Skopal, F. (2010). Traitement de la phase glycérol formée par la production de biodiesel. Bioresour. Technol. 101, 3242-3245. doi : 10.1016/j.biortech.2009.12.094
PubMed Abstract | CrossRef Full Text | Google Scholar
Karabas, H. (2013). Production de biodiesel à partir d’huile brute de noyau de gland (Quercus frainetto L.) : un processus d’optimisation utilisant la méthode Taguchi. Renew. Energy 53, 384-388. doi : 10.1016/j.renene.2012.12.002
CrossRef Full Text | Google Scholar
Kongjao, S., Damronglerd, S., et Hunsom, M. (2010). Purification du glycérol brut dérivé de l’usine d’esters méthyliques d’huiles usagées. Korean J. Chem. Eng. 27, 944-949. doi : 10.1007/s11814-010-0148-0
CrossRef Full Text | Google Scholar
Kovács, A., Czinkota, I., et Tóth, J. (2012). Amélioration de l’essai de l’indice d’acidité de la matière première et du produit du biodiesel. J. Am. Oil Chem. Soc. 89, 409-417. doi : 10.1007/s11746-011-1929-2
CrossRef Full Text | Google Scholar
Lancrenon, X., and Fedders, J. (2008, June 2008). Une innovation dans la purification de la glycérine. Biodiesel Magazine.
Google Scholar
Manosak, R., Limpattayanate, S., et Hunsom, M. (2011). Raffinage séquentiel du glycérol brut dérivé de l’usine d’esters méthyliques d’huiles usées via un processus combiné de chimie et d’adsorption. Fuel Process. Technol. 92, 92-99. doi : 10.1016/j.fuproc.2010.09.002
CrossRef Full Text | Google Scholar
Monteiro, M. R., Kugelmeier, C. L., Pinheiro, R. S., Batalha, M. O., et da Silva César, A. (2018). Glycérol de la production de biodiesel : voies technologiques pour la durabilité. Renew. Sust. Energy Rev. 88, 109-122. doi : 10.1016/j.rser.2018.02.019
CrossRef Full Text | Google Scholar
Park, S. H. (1996). Conception et analyse robustes pour l’ingénierie de la qualité. Londres : Chapman and Hall.
Google Scholar
Roy, R. K. (2001). Conception d’expériences à l’aide de l’approche Taguchi : 16 étapes pour l’amélioration des produits et des processus. John Wiey and Sons.
Google Scholar
Saifuddin, N., Refal, H., et Kumaran, P. (2013). Purification rapide du sous-produit glycérol de la production de biodiesel par le biais d’un processus combiné d’acidification assistée par micro-ondes et d’adsorption via le chitosane immobilisé avec du teast. J. Appl. Sci. Eng. Technol. 7, 593-602. doi : 10.19026/rjaset.7.295
CrossRef Full Text | Google Scholar
Samul, D., Leja, K., et Grajek, W. (2014). Impuretés du glycérol brut et leur effet sur la production de métabolites. Ann. Microbiol. 64, 891-898. doi : 10.1007/s13213-013-0767-x
PubMed Abstract | CrossRef Full Text | Google Scholar
Sdrula, N. (2010). Une étude utilisant la séparation classique ou par membrane dans le processus de biodiesel. Desalination 250, 1070-1072. doi : 10.1016/j.desal.2009.09.110
CrossRef Full Text | Google Scholar
Sharma, P., Verma, A., Sidhu, R. K., et Pandey, O. P. (2005). Sélection des paramètres de processus pour les aimants frittés en ferrite de strontium en utilisant la conception orthogonale L9 de Taguchi. J. Mater. Process. Technol. 168, 147-151. doi : 10.1016/j.jmatprotec.2004.12.003
CrossRef Full Text | Google Scholar
Talebian-Kiakalaieh, A., Amin, N. A. S., Najaafi, N., et Tarighi, S. (2018). Une revue sur l’acétalisation catalytique du glycérol bio-renouvelable en additifs de carburant. Front. Chem. 6:573. doi : 10.3389/fchem.2018.00573
PubMed Abstract | CrossRef Full Text | Google Scholar
Tan, H. W., Abdul Aziz, A. R., et Aroua, M. K. (2013). La production de glycérol et ses applications en tant que matière première : une revue. Renew. Sust. Energy Rev. 27, 118-127. doi : 10.1016/j.rser.2013.06.035
CrossRef Full Text | Google Scholar
Venkataramanan, K. P., Boatman, J. J., Kurniawan, Y., Taconi, K. A., Bothun, G. D., et Scholz, C. (2012). Impact des impuretés dans le glycérol brut dérivé du biodiesel sur la fermentation par Clostridium pasteurianum ATCC 6013. Appl. Microbiol. Biotechnol. 93, 1325-1335. doi : 10.1007/s00253-011-3766-5
PubMed Abstract | CrossRef Full Text | Google Scholar
Xiao, Y., Xiao, G., et Varma, A. (2013). Une procédure universelle pour la purification du glycérol brut à partir de différentes matières premières dans la production de biodiesel : étude expérimentale et de simulation. Ind. Eng. Chem. Res. 52, 14291-14296. doi : 10.1021/ie402003u
CrossRef Full Text | Google Scholar
Yang, F., Hanna, M. A., et Sun, R. (2012). Utilisations à valeur ajoutée pour le glycérol brut – un sous-produit de la production de biodiesel. Biotechnol. Biofuels 5, 1-10. doi : 10.1186/1754-6834-5-13
PubMed Abstract | CrossRef Full Text | Google Scholar
.
