Objectifs d’apprentissage
- Écrire la formule chimique d’un composé ionique simple.
- Reconnaître les ions polyatomiques dans les formules chimiques.
Nous avons déjà rencontré quelques formules chimiques de composés ioniques simples. Une formule chimique est une liste concise des éléments d’un composé et des ratios de ces éléments. Pour mieux comprendre la signification d’une formule chimique, nous devons examiner comment un composé ionique est construit à partir de ses ions.
Les composés ioniques existent sous forme d’ions positifs et négatifs alternés dans des réseaux tridimensionnels réguliers appelés cristaux (Figure \(\PageIndex{1}\)). Comme vous pouvez le voir, il n’y a pas de » particules » individuelles de NaCl dans le réseau ; il s’agit plutôt d’un réseau continu d’ions sodium et chlorure alternés. Cependant, nous pouvons utiliser le rapport entre les ions sodium et les ions chlorure, exprimé par les nombres entiers les plus bas possibles, pour décrire le composé. Dans le cas du chlorure de sodium, le rapport entre les ions sodium et les ions chlorure, exprimé par les nombres entiers les plus bas, est de 1:1, nous utilisons donc NaCl (un symbole Na et un symbole Cl) pour représenter le composé. Ainsi, NaCl est la formule chimique du chlorure de sodium, qui est un moyen concis de décrire le nombre relatif des différents ions dans le composé. Un échantillon macroscopique est composé de myriades de paires NaCl, chaque paire étant appelée unité de formule. Bien qu’il soit pratique de penser que les cristaux de NaCl sont composés d’unités NaCl individuelles, la figure \(\PageIndex{1}\) montre qu’aucun ion unique n’est exclusivement associé à un autre ion unique. Chaque ion est entouré d’ions de charge opposée.
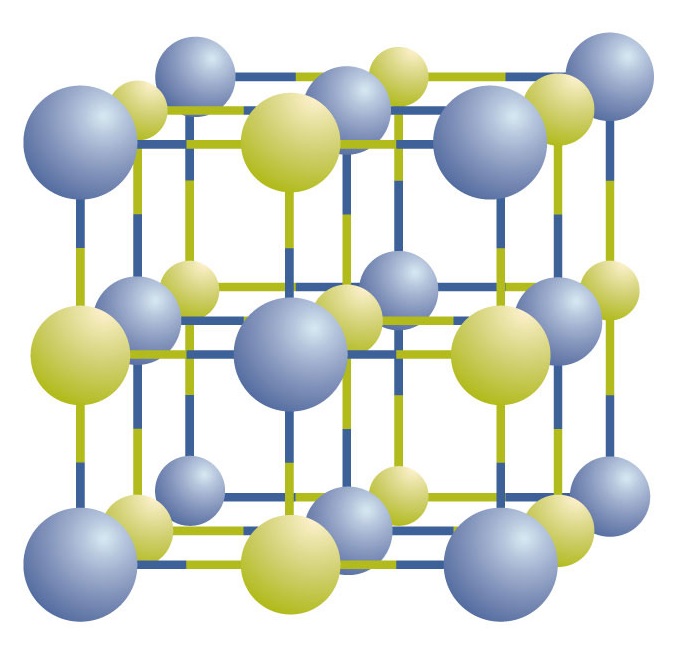
Figure \(\PageIndex{1}\) Un cristal de chlorure de sodium. Un cristal contient un réseau tridimensionnel d’ions positifs et négatifs alternés. Le motif précis dépend du composé. Un cristal de chlorure de sodium, représenté ici, est un ensemble d’ions sodium et chlore alternés.
La formule d’un composé ionique suit plusieurs conventions. Tout d’abord, le cation est écrit avant l’anion. Comme la plupart des métaux forment des cations et que la plupart des non-métaux forment des anions, les formules énumèrent généralement le métal en premier et ensuite le non-métal. Deuxièmement, les charges ne sont pas écrites dans une formule. Rappelez-vous que dans un composé ionique, les espèces constitutives sont des ions et non des atomes neutres, même si la formule ne contient pas de charges. Enfin, la formule correcte d’un composé ionique obéit toujours à la règle suivante : la charge positive totale doit être égale à la charge négative totale. Pour déterminer la formule appropriée de n’importe quelle combinaison d’ions, il faut déterminer combien de chaque ion est nécessaire pour équilibrer les charges positives et négatives totales du composé.
Cette règle est finalement basée sur le fait que la matière est, globalement, électriquement neutre.
Par convention, on suppose qu’il n’y a qu’un seul atome si un indice n’est pas présent. On n’utilise pas 1 comme indice.
Si l’on regarde le composé ionique constitué d’ions lithium et d’ions bromure, on constate que l’ion lithium a une charge 1+ et l’ion bromure une charge 1-. Un seul ion de chaque est nécessaire pour équilibrer ces charges. La formule du bromure de lithium est LiBr.
Lorsqu’un composé ionique est formé à partir de magnésium et d’oxygène, l’ion magnésium a une charge 2+, et l’atome d’oxygène a une charge 2-. Bien que ces deux ions aient des charges plus élevées que les ions du bromure de lithium, ils s’équilibrent toujours dans un rapport de un à un. Par conséquent, la formule appropriée pour ce composé ionique est MgO.
Prenons maintenant le composé ionique formé par le magnésium et le chlore. Un ion de magnésium a une charge 2+, tandis qu’un ion de chlore a une charge 1-:
Mg2+ Cl-
La combinaison d’un ion de chaque ne permet pas d’équilibrer complètement les charges positives et négatives. La façon la plus simple d’équilibrer ces charges est de supposer la présence de deux ions chlorure pour chaque ion magnésium:
Mg2+ Cl- Cl-
Maintenant les charges positives et négatives sont équilibrées. Nous pourrions écrire la formule chimique de ce composé ionique sous la forme MgClCl, mais la convention est d’utiliser un indice numérique lorsqu’il y a plus d’un ion d’un type donné-MgCl2. Cette formule chimique indique qu’il y a un ion magnésium et deux ions chlorure dans cette formule. (Ne lisez pas la partie « Cl2 » de la formule comme une molécule de chlore élémentaire diatomique. Le chlore n’existe pas en tant qu’élément diatomique dans ce composé. Il existe plutôt sous forme de deux ions chlorure individuels). Par convention, le rapport du nombre entier le plus faible est utilisé dans les formules des composés ioniques. La formule Mg2Cl4 a des charges équilibrées avec les ions dans un rapport de 1:2, mais ce n’est pas le rapport de nombre entier le plus bas.
Par convention, le rapport de nombre entier le plus bas des ions est utilisé dans les formules ioniques. Il existe des exceptions pour certains ions, tels que Hg22+
Exemple \(\PageIndex{1}\)
Écrivez la formule chimique d’un composé ionique composé de chaque paire d’ions.
- l’ion sodium et l’ion soufre
- l’ion aluminium et l’ion fluorure
- l’ion fer 3+ et l’ion oxygène
Solution
- Pour obtenir un octet de coquille de valence, le sodium forme un ion avec une charge 1+, tandis que l’ion soufre a une charge 2-. Deux ions 1+ de sodium sont nécessaires pour équilibrer la charge 2 de l’ion soufre. Plutôt que d’écrire la formule sous la forme NaNaS, nous l’abrégeons par convention en Na2S.
- L’ion aluminium a une charge 3+, tandis que l’ion fluorure formé par le fluor a une charge 1-. Trois ions fluor 1- sont nécessaires pour équilibrer la charge 3+ de l’ion aluminium. Cette combinaison s’écrit AlF3.
- Le fer peut former deux ions possibles, mais l’ion de charge 3+ est spécifié ici. L’atome d’oxygène a une charge 2 en tant qu’ion. Pour équilibrer les charges positives et négatives, on se tourne vers le multiple le moins commun-6 : deux ions 3+ de fer donneront 6+, tandis que trois ions 2- d’oxygène donneront 6-, équilibrant ainsi les charges positives et négatives globales. Ainsi, la formule de ce composé ionique est Fe2O3.
Exercice \(\PageIndex{1}\)
Écrivez la formule chimique d’un composé ionique composé de chaque paire d’ions.
- l’ion calcium et l’ion oxygène
- l’ion cuivre 2+ et l’ion soufre
- l’ion cuivre 1+ et l’ion soufre
Ions polyatomiques
Certains ions sont constitués de groupes d’atomes liés entre eux et ont une charge électrique globale. Comme ces ions contiennent plus d’un atome, ils sont appelés ions polyatomiques. Les ions polyatomiques ont des formules, des noms et des charges caractéristiques qu’il faut mémoriser. Par exemple, NO3- est l’ion nitrate ; il possède un atome d’azote et trois atomes d’oxygène et une charge globale de 1. Le tableau \(\PageIndex{1}\) énumère les ions polyatomiques les plus courants.
| Nom | Formule |
|---|---|
| Ion ammonium | NH4+ |
| Ion acétate | C2H3O2- |
| Ion carbonate | CO32- |
| Ion hydrogénocarbonate (ion bicarbonate) | HCO3- |
| Ion cyanure | CN- |
| Ion hydroxyde | OH- |
| Ion phosphate | PO43- |
| Ion hydrogène phosphate | HPO42- |
| Ion dihydrogène phosphate | H2PO4- |
| Ion nitrate | NO3- |
| Ion sulfite | SO32- |
La règle pour construire les formules des composés ioniques contenant des ions polyatomiques est la même que pour les formules contenant des ions monatomiques (un seul atome) : la formule est la suivanteatome) : les charges positives et négatives doivent s’équilibrer. Si plusieurs ions polyatomiques sont nécessaires pour équilibrer la charge, la formule entière de l’ion polyatomique doit être mise entre parenthèses, et l’indice numérique est placé à l’extérieur des parenthèses. Cela permet de montrer que l’indice s’applique à l’ensemble de l’ion polyatomique. Un exemple est Ba(NO3)2.
Exemple \(\PageIndex{2}\)
Écrivez la formule chimique d’un composé ionique composé de chaque paire d’ions.
- l’ion potassium et l’ion sulfate
- l’ion calcium et l’ion nitrate
Solution
- Les ions potassium ont une charge de 1+, tandis que les ions sulfate ont une charge de 2-. Nous aurons besoin de deux ions potassium pour équilibrer la charge de l’ion sulfate, donc la formule chimique appropriée est K2SO4.
- Les ions calcium ont une charge de 2+, tandis que les ions nitrate ont une charge de 1-. Nous aurons besoin de deux ions nitrate pour équilibrer la charge de chaque ion calcium. La formule du nitrate doit être mise entre parenthèses. Ainsi, nous écrivons Ca(NO3)2 comme formule pour ce composé ionique.
Exercice \(\PageIndex{2}\)
Écrivez la formule chimique d’un composé ionique composé de chaque paire d’ions.
- l’ion magnésium et l’ion carbonate
- l’ion aluminium et l’ion acétate
Reconnaître les composés ioniques
Il existe deux façons de reconnaître les composés ioniques. Premièrement, les composés entre des éléments métalliques et non métalliques sont généralement ioniques. Par exemple, CaBr2 contient un élément métallique (le calcium, un métal du groupe 2A) et un élément non métallique (le brome, un non-métal du groupe 7A). Il s’agit donc très probablement d’un composé ionique. (En fait, il est ionique.) En revanche, le composé NO2 contient deux éléments qui sont tous deux non métalliques (azote, du groupe 5A, et oxygène, du groupe 6A). Ce n’est pas un composé ionique ; il appartient à la catégorie des composés covalents dont il est question ailleurs. Notez également que cette combinaison d’azote et d’oxygène n’a pas de charge électrique spécifiée, ce n’est donc pas l’ion nitrite.
Deuxièmement, si vous reconnaissez la formule d’un ion polyatomique dans un composé, le composé est ionique. Par exemple, si vous voyez la formule Ba(NO3)2, vous pouvez reconnaître la partie « NO3 » comme étant l’ion nitrate, \(\rm{NO_3^-}\). (Rappelez-vous que la convention pour écrire les formules des composés ioniques est de ne pas inclure la charge ionique). Ceci est un indice que l’autre partie de la formule, Ba, est en fait l’ion Ba2+, la charge 2+ équilibrant la charge globale 2- des deux ions nitrate. Ainsi, ce composé est également ionique.
Exemple \(\PageIndex{3}\)
Identifiez chaque composé comme ionique ou non ionique.
- Na2O
- PCl3
- NH4Cl
- OF2
Solution
- Le sodium est un métal et l’oxygène est un non-métal ; par conséquent, Na2O devrait être ionique.
- Le phosphore et le chlore sont tous deux des non-métaux. Par conséquent, PCl3 n’est pas ionique.
- Le NH4 dans la formule représente l’ion ammonium, NH4+, ce qui indique que ce composé est ionique.
- L’oxygène et le fluor sont tous deux des non-métaux. Par conséquent, OF2 n’est pas ionique.
Exercice \(\PageIndex{3}\)
Identifiez chaque composé comme ionique ou non ionique.
- N2O
- FeCl3
- (NH4)3PO4
- SOCl2
Regardons de plus près : Sang et eau de mer
La science reconnaît depuis longtemps que le sang et l’eau de mer ont des compositions similaires. Après tout, ces deux liquides contiennent des composés ioniques dissous. Cette similitude pourrait être plus qu’une simple coïncidence ; de nombreux scientifiques pensent que les premières formes de vie sur Terre sont apparues dans les océans. Un examen plus approfondi montre toutefois que le sang et l’eau de mer sont très différents. Une solution de chlorure de sodium à 0,9 % correspond approximativement à la concentration de sel présente dans le sang. En revanche, l’eau de mer est principalement une solution de chlorure de sodium à 3 %, soit plus de trois fois la concentration dans le sang. Voici une comparaison des quantités d’ions dans le sang et l’eau de mer :
| Ion | Pourcentage dans l’eau de mer | Pourcentage dans le sang |
|---|---|---|
| Na+ | 2.36 | 0,322 |
| Cl- | 1,94 | 0,366 |
| Mg2+ | 0,13 | 0,002 |
| SO42- | 0.09 | – |
| K+ | 0,04 | 0,016 |
| Ca2+ | 0.04 | 0,0096 |
| HCO3- | 0,002 | 0.165 |
| HPO42-, H2PO4- | – | 0,01 |
La plupart des ions sont plus abondants dans l’eau de mer que dans le sang, à quelques exceptions importantes près. Il y a beaucoup plus d’ions hydrogénocarbonate (HCO3-) dans le sang que dans l’eau de mer. Cette différence est importante car l’ion hydrogénocarbonate et certains ions apparentés jouent un rôle crucial dans le contrôle des propriétés acido-basiques du sang. La quantité d’ions hydrogénophosphate (HPO42- et H2PO4-) dans l’eau de mer est très faible, mais ils sont présents en plus grande quantité dans le sang, où ils affectent également les propriétés acido-basiques. Une autre différence notable est que le sang n’a pas de quantités significatives de l’ion sulfate (SO42-), mais cet ion est présent dans l’eau de mer.
Principes clés
- Les formules chimiques appropriées pour les composés ioniques équilibrent la charge positive totale avec la charge négative totale.
- Il existe également des groupes d’atomes ayant une charge globale, appelés ions polyatomiques.
Contributeurs et attributions
-
Anonyme
.
