Mesures initiales
Il faut porter une blouse, des gants et des lunettes de protection. Une lumière adéquate est mieux fournie par une lampe frontale avec un faisceau étroit réglable. Les patients doivent être installés confortablement en position assise, en tenant une bassine sous leur menton.
Comme toujours, il faut d’abord s’occuper des ABC (A irway, B reathing, et C irculation). Rarement, une épistaxis sévère peut nécessiter une intubation endotrachéale.
On doit demander aux patients stables de saisir et de pincer tout leur nez, en maintenant une pression continue pendant au moins 10 minutes. Assurez-vous qu’ils compriment les tissus mous du nez contre la cloison nasale ; le fait de pincer les os nasaux durs et incompressibles ne facilitera pas le contrôle de l’hémorragie.
Les patients présentant une hémorragie importante doivent recevoir une ligne intraveineuse (IV) et une perfusion de cristalloïdes, ainsi qu’une surveillance cardiaque continue et une oxymétrie de pouls. Les patients présentent fréquemment une pression artérielle élevée ; cependant, une réduction significative peut généralement être obtenue avec une analgésie et une sédation légère seulement.
Un traitement antihypertenseur spécifique est rarement nécessaire et devrait être évité dans le cadre d’une hémorragie importante. La relation entre l’hypertension et l’épistaxis est souvent mal comprise. Les patients souffrant d’épistaxis présentent généralement une tension artérielle élevée. L’épistaxis est plus fréquente chez les patients hypertendus, peut-être en raison de la fragilité vasculaire due à une maladie de longue date.
L’hypertension, cependant, est rarement une cause directe de l’épistaxis. Plus souvent, l’épistaxis et l’anxiété associée provoquent une élévation aiguë de la pression artérielle. La thérapie doit donc être axée sur le contrôle de l’hémorragie et la réduction de l’anxiété comme principaux moyens de réduire la pression artérielle.
Insérer des pledgets imbibés d’une solution anesthésique-vasoconstrictrice dans la cavité nasale pour anesthésier et rétrécir la muqueuse nasale. Trempez les compresses dans une solution topique de cocaïne à 4 % ou une solution de lidocaïne à 4 % et d’épinéphrine topique (1:10 000) et placez-les dans la cavité nasale. Laissez-les en place pendant 10-15 minutes.
Si un point de saignement est facilement identifié, une cautérisation chimique douce peut être effectuée après l’application d’une anesthésie topique adéquate. L’extrémité d’un bâtonnet de nitrate d’argent est roulée sur la muqueuse jusqu’à la formation d’une escarre grise. Pour éviter la nécrose ou la perforation du septum, un seul côté du septum doit être cautérisé à la fois. Pour être efficace, la cautérisation doit être effectuée après le contrôle du saignement. La cautérisation thermique à l’aide d’un dispositif d’électrocautérisation est réservée aux saignements plus agressifs et est effectuée avec le patient sous anesthésie locale ou générale.
Si les tentatives de contrôle de l’hémorragie par pression ou cautérisation échouent, le nez doit être emballé. Les options comprennent un emballage nasal traditionnel, une éponge nasale préfabriquée, un ballon d’épistaxis ou des matériaux absorbables.
Une revue de la littérature par Kamhieh et Fox a suggéré que l’acide tranexamique est un traitement efficace de l’épistaxis. Bien qu’un essai ait rapporté que l’acide tranexamique topique ne présente pas de bénéfice significatif dans l’épistaxis aiguë, les essais les plus importants ont indiqué une efficacité significative. Une étude a également rapporté que l’acide tranexamique oral n’était pas efficace dans l’épistaxis aiguë, mais deux essais randomisés et contrôlés ont trouvé qu’il réduisait la gravité et la fréquence des épistaxis récurrentes chez les patients atteints de télangiectasie hémorragique héréditaire.
Une autre revue de la littérature, par Gottlieb et al, a également indiqué que l’acide tranexamique topique est efficace contre l’épistaxis aiguë. Alors que le taux d’arrêt du saignement dans les 30 minutes ne différait pas significativement entre le groupe acide tranexamique et les témoins, un plus grand nombre de patients traités avec l’agent ont pu sortir de l’hôpital dans les 2 heures suivant leur arrivée. De plus, lors du suivi de 24 heures et d’une semaine, il y avait moins d’épisodes de re-saignement avec l’acide tranexamique. Le taux de complication associé à l’acide tranexamique ne différait pas de celui des témoins.
Contrairement à l’étude de Gottlieb, un rapport rétrospectif de Birmingham et al n’a trouvé aucune différence significative dans la durée de séjour aux urgences entre les patients atteints d’épistaxis aiguës qui ont été traités avec de l’acide tranexamique topique et ceux qui ont reçu des soins standard. Cependant, les taux de consultations d’oto-rhino-laryngologistes et de packing nasal étaient significativement plus faibles dans le groupe acide tranexamique que chez les patients recevant les soins standards (30,0% contre 65,2% et 16,7% contre 23,9%, respectivement).
Packaging traditionnel (gaze de pétrolatum)
Le packing nasal antérieur traditionnel avec de la gaze de pétrolatum a été largement supplanté par l’utilisation de tampons et de ballons, qui sont facilement disponibles et plus facilement placés. Cette méthode est souvent mal exécutée, la quantité de gaze utilisée étant insuffisante et placée principalement dans le naris antérieur. Lorsqu’elle est placée de cette manière, la gaze sert de bouchon plutôt que de pack hémostatique. Les médecins inexpérimentés dans la mise en place correcte d’un pack de gaze devraient plutôt utiliser un tampon nasal ou un ballon.
La technique correcte de mise en place d’un pack de gaze est la suivante . Saisissez le ruban de gaze à environ 6 pouces de son extrémité avec une pince à baïonnette. Placez-le dans la cavité nasale le plus en arrière possible, en veillant à ce que l’extrémité libre dépasse du nez. Lors du premier passage, la gaze est pressée sur le plancher du nasopharynx avec des baïonnettes fermées.
Puis, saisissez le ruban à environ 4-5 pouces de l’alvéole nasale, et repositionnez le spéculum nasal de sorte que la lame inférieure maintienne le ruban contre le bord inférieur de l’alvéole nasale. Apportez une deuxième bande dans le nez, et pressez vers le bas.
Continuez ce processus, en superposant la gaze de l’inférieur vers le supérieur jusqu’à ce que le naris soit complètement emballé. Les deux extrémités du ruban doivent dépasser du naris et doivent être fixées avec du ruban adhésif. Si cette mesure ne permet pas d’arrêter le saignement, envisager un tamponnement nasal bilatéral.
Packing avec éponge compressée
Tailler l’éponge compressée (par exemple Merocel) pour qu’elle s’adapte parfaitement au naris. Humidifiez l’extrémité avec un lubrifiant chirurgical ou une pommade antibiotique topique. Saisissez fermement la longueur de l’éponge avec une pince à baïonnette, écartez les narines verticalement avec un spéculum nasal et faites avancer l’éponge le long du plancher de la cavité nasale. Une fois mouillée par du sang ou une petite quantité de sérum physiologique, l’éponge se dilate pour remplir la cavité nasale et tamponner le saignement (voir les images ci-dessous).
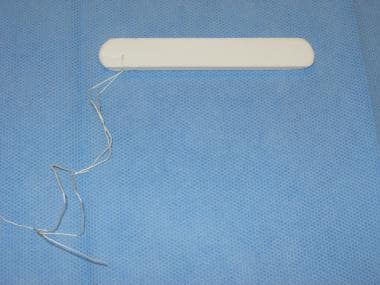 Éponge comprimée – Merocel.
Éponge comprimée – Merocel. 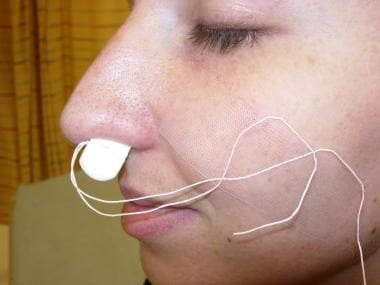 Merocel placé dans la narine gauche pour le tamponnement antérieur.
Merocel placé dans la narine gauche pour le tamponnement antérieur. Packing avec ballons d’épistaxis
Les ballons d’épistaxis antérieurs (par exemple, Rapid Rhino) sont disponibles en différentes longueurs (voir les images ci-dessous). Une couche externe en carboxycellulose favorise l’agrégation des plaquettes. Les ballons sont aussi efficaces que les tampons nasaux, plus faciles à insérer et à retirer, et plus confortables pour le patient. Pour insérer le ballon, imbiber sa couche externe tricotée d’eau, l’insérer le long du plancher de la cavité nasale et le gonfler lentement avec de l’air jusqu’à ce que le saignement s’arrête.
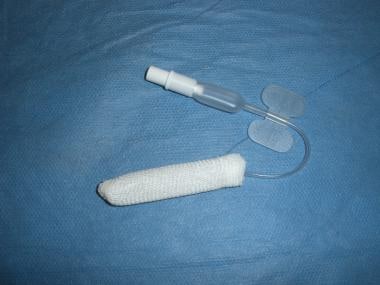 Rapid Rhino – 5,5 cm pour le remplissage nasal antérieur.
Rapid Rhino – 5,5 cm pour le remplissage nasal antérieur. 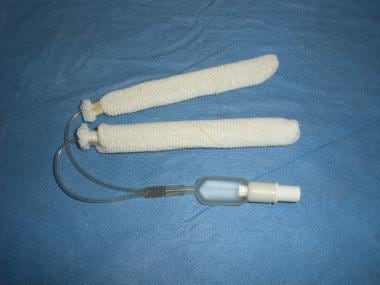 Rapid Rhino bilatéral – 7,5 cm pour le packing nasal antérieur/postérieur.
Rapid Rhino bilatéral – 7,5 cm pour le packing nasal antérieur/postérieur. L’épistaxis postérieure est fréquemment traitée avec des dispositifs à double ballonnet qui ont des ballonnets antérieur et postérieur séparés.
Après avoir passé le ballonnet postérieur à travers le naris et dans la cavité nasale postérieure, le gonfler avec 4-5 ml d’eau stérile et le tirer doucement vers l’avant pour qu’il s’adapte bien au choane postérieur. Une fois que le saignement dans le pharynx postérieur a été contrôlé, remplissez le ballon antérieur avec de l’eau stérile jusqu’à ce que le saignement s’arrête complètement. Évitez le surgonflage, car il peut en résulter une nécrose de pression ou des dommages au septum. Enregistrer la quantité de liquide placée dans chaque ballonnet.
Si une sonde de Foley est utilisée, placer un cathéter de 12-16 français avec un ballonnet de 30 ml dans le nez le long du plancher du nasopharynx, jusqu’à ce que l’extrémité soit visible dans le pharynx postérieur. Gonfler lentement le ballon avec 15 ml d’eau stérile, le tirer vers l’avant jusqu’à ce qu’il soit fermement placé contre les choanes postérieures, et le fixer en place avec un clamp ombilical. Utilisez un clamp de contrefort avec une gaze de coton pour éviter la nécrose par pression sur les alènes nasales ou la columelle. Enfin, placez un pack nasal antérieur.
Voir aussi Pack nasal épistaxis antérieur et Pack nasal épistaxis postérieur.
Packing avec des matériaux absorbables
Les matériaux absorbables tels que la cellulose oxydée (Surgicel), la mousse de gélatine (Gelfoam) et la combinaison de gélatine et de thrombine (FloSeal) sont des alternatives appropriées au packing nasal pour les saignements antérieurs. Ils tamponnent directement les sites de saignement, augmentent la formation de caillots et protègent la muqueuse nasale de la dessiccation ou d’autres traumatismes. Ils sont faciles à utiliser et confortables et se conforment à l’irrégularité des contours nasaux.
Consultations
Les tentatives de tamponnement nasal peuvent entraîner un ralentissement significatif de l’hémorragie mais pas son arrêt. L’incapacité à contrôler complètement l’hémorragie est une indication absolue pour consulter un oto-rhino-laryngologiste aux urgences.
L’épistaxis qui nécessite un packing postérieur doit être géré en coopération avec un oto-rhino-laryngologiste. En raison des multiples complications possibles, l’admission est nécessaire, généralement dans un cadre surveillé.
La consultation d’un hématologue est indiquée pour les patients présentant des dyscrasies hémorragiques ou des coagulopathies.
Poursuite des soins hospitaliers
Admettre les patients avec un packing postérieur. Le packing nasal postérieur est particulièrement inconfortable pour le patient et favorise l’hypoxie et l’hypoventilation. Le fait de ne pas admettre et de ne pas surveiller de manière appropriée tous les patients qui ont besoin d’un conditionnement postérieur peut entraîner une mortalité importante.
Les patients âgés ou les patients souffrant de troubles cardiaques ou d’une maladie pulmonaire obstructive chronique (MPOC) doivent recevoir un supplément d’oxygène et être admis dans un environnement surveillé.
Un saignement important ou non contrôlé provenant d’un site postérieur peut nécessiter une prise en charge chirurgicale ; cela se produit dans environ 30 % des cas. L’embolisation par radiologie interventionnelle des artères impliquées et la ligature chirurgicale des vaisseaux sont des options possibles dans de tels cas.
Autres soins ambulatoires
Les patients sortant de l’hôpital avec un packing antérieur doivent recevoir des soins de suivi avec un oto-rhino-laryngologiste dans les 48-72 h. Le packing nasal empêche le drainage des sinus et augmente le risque de sinusite ou de syndrome de choc toxique.
Les tumeurs ou autres pathologies graves sont des causes peu fréquentes d’épistaxis. Cependant, tous les patients qui présentent une épistaxis doivent faire l’objet d’un suivi auprès d’un oto-rhino-laryngologiste pour un examen nasopharyngé complet. Une épistaxis unilatérale récurrente doit particulièrement faire craindre un néoplasme.
Envisager de placer les patients sous un antibiotique à large spectre (par exemple, une pénicilline ou une céphalosporine de première génération) pour couvrir tous les pathogènes probables dans le contexte du milieu clinique.
Des analgésiques oraux doivent également être prescrits. Le contrôle de la douleur est essentiel à la qualité des soins aux patients : il assure le confort du patient, favorise la toilette pulmonaire et permet les régimes de physiothérapie. La plupart des analgésiques ont des propriétés sédatives, ce qui est bénéfique pour les patients qui ont des lésions cutanées douloureuses. Conseillez aux patients d’éviter l’aspirine, les produits contenant de l’aspirine et les anti-inflammatoires non stéroïdiens (AINS).
Les patients qui prennent de la warfarine peuvent généralement poursuivre leur traitement actuel sans modification. L’arrêt temporaire de la warfarine ou l’inversion active de la coagulopathie ne sont indiqués qu’en cas d’hémorragie incontrôlée et de rapport international normalisé (INR) suprathérapeutique.
Lignes directrices du COVID-19
En mai 2020, D’Aguanno et al ont publié les recommandations cliniques suivantes pour traiter l’épistaxis pendant la pandémie de coronavirus 2019 (COVID-19) :
-
Recommandation stricte pour l’utilisation d’équipements jetables
-
Préférence pour l’utilisation de masques FFP3 (Europe) ou N99 (États-Unis)
-
Utilisation de masques FFP2 ou N95, couverts par un masque chirurgical, si les masques FFP3 ne sont pas disponibles
-
Forte recommandation pour la casquette et les couvre-chaussures, les lunettes de protection, la blouse et les gants doubles en nitrile
-
Contrôle des facteurs de risque de saignement de nez (pression artérielle, facteurs de coagulation, traitements en cours avec des agents antithrombotiques ou anticoagulants).
-
Il faut vérifier l’absence de fièvre, de symptômes respiratoires et de contacts à risque
-
Rechercher une perte soudaine de l’odorat et/ou du goût
-
Masque chirurgical pour les patients, si cela est permis
-
Évaluation immédiate de la gravité du saignement de nez
-
Une intervention non invasive est recommandée, y compris la compression bidigitale et l’utilisation d’agents antifibrinolytiques
-
Si les salles d’opération conventionnelles ne sont pas disponibles, utiliser des espaces bien délimités au sein du service des urgences
-
Utilisation d’un personnel clinique réduit et expérimenté, y compris un chirurgien et une infirmière de bloc, avec un équipement de protection individuelle (EPI) approprié
-
Éviter toute intervention inutile
-
Effectuer un emballage nasal ou une cautérisation en cas d’échec de la procédure non invasive
-
Utilisation d’un emballage résorbable, si disponible
-
Report de la chirurgie pour épistaxis postérieure nécessitant une ligature de l’artère sphénopalatine, jusqu’à ce que le test COVID-19 soit effectué
-
Éviter les sprays atomisés d’anesthésique local ; les compresses imbibées sont préférables
-
Pendant la procédure, utiliser un système d’aspiration, employant un système fermé avec un filtre viral
-
Le patient doit recevoir des instructions post-procédure en ce qui concerne le retrait du packing ou la prophylaxie antibiotique, afin de diminuer le risque de récidive et d’optimiser le résultat
-
Une exécution soigneuse des procédures de blouse et de déshabillage doit être employée
-
Utilisation d’EPI standard par le personnel qui manipule la décontamination du matériel chirurgical
.
