- o-Xylen Chemické vlastnosti,použití,výroba
- Xylen
- Přesná destilace pro separaci o-xylenu a p-xylenu
- Chemické vlastnosti
- Použití
- Způsob výroby
- Kategorie
- Třída toxicity
- Akutní toxicita
- Výbušnost a nebezpečné vlastnosti
- Hořlavost a nebezpečné vlastnosti
- Skladování a přepravní vlastnosti
- Hasicí prostředky
- Pracovní norma
- Chemické vlastnosti
- Fyzikální vlastnosti
- Použití
- Definice
- Syntéza Reference(s)
- Všeobecný popis
- Vzduch & Voda Reakce
- Profil reaktivity
- Zdravotní nebezpečnost
- Nebezpečí požáru
- Chemická reaktivita
- Bezpečnostní profil
- Zdroj
- Výskyt v životním prostředí
- Metody čištění
o-Xylen Chemické vlastnosti,použití,výroba
Xylen
Xylen označuje aromatický uhlovodík, jehož dva atomy vodíku na benzenovém kruhu jsou nahrazeny dvěma methylovými skupinami. Má tři izomery o-xylen (1, 2-dimethylbenzen), m-xylen a p-xylen. Průmyslovými produkty jsou směsi těchto tří izomerů s podílem 10 % o-, 70 % m- a 20 % p-. V koksárenském průmyslu je jedním z rafinovaných produktů surového benzenu.
Xylen je druh bezbarvé hořlavé kapaliny; teplota tání o-, m- a p-xylenu je 25,2 ℃,-47,9 ℃ a 13,3 ℃; teploty varu jsou 144.4 ℃, 139,1 ℃ a 138,3 ℃, zatímco relativní hustota je 0,8802, 0,8642 a 0,8611; není rozpustný ve vodě, ale mísí se s mnoha druhy organických rozpouštědel. Při katalytické oxidaci vznikají anhydrid ftalový, kyselina isoftalová a kyselina tereftalová.
Xylen je jednou z důležitých surovin organických chemikálií, přirozeně se vyskytující v uhelném dehtu a některých druzích ropy. Lze jej získat frakcionací lehké ropné části uhelného dehtu nebo katalytickým reformingem lehkého benzínu. Průmysl provádí hlavně extrakci pomocí frakce C8 v reformátech benzínu. Alternativně jej lze vyrábět disproporcionační reakcí toluenu za přítomnosti katalyzátoru a vysoké teploty a vysokého tlaku. V současné době průmysl k jejich separaci používá především metodu kryogenní krystalizace, adsorpce a tvorby komplexů nebo molekulových sít. O-xylen má poměrně vysoký bod varu a lze jej oddělit pomocí destilace. p-xylen má rovněž vysoký bod tání a lze jej čistit pomocí frakční krystalizace. Směsný xylen bez separace může být přímo použit jako rozpouštědlo s tím, že je doplněn do benzinu schopného zlepšit protiexplozivní vlastnosti. Jsou součástí leteckého benzinu. O-xylen se používá hlavně k přípravě ftalanhydridu, který je důležitou surovinou pro výrobu různých barviv a indikátorů (např. fenolftaleinu). Kromě toho lze o-xylen použít také k přípravě polyesterové pryskyřice, repelentů proti hmyzu, změkčovadel a barviv. Z o-xylenu může nitrací a redukcí vzniknout 4,6-dimethyl-1,3-fenylendiamin, který je meziproduktem pro syntetická barviva. M-xylen lze také použít jako surovinu pro syntetické vonné látky (např. xylenové pižmo). P-xylen se používá hlavně při výrobě kyseliny tereftalové, která je důležitou surovinou pro syntetická polyesterová vlákna (polyester).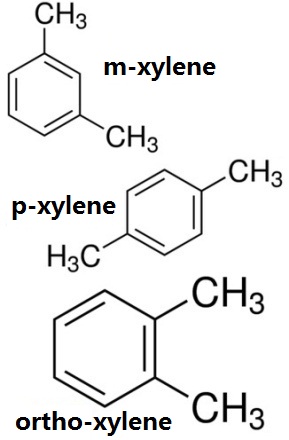
Obrázek 1 chemická struktura tří izomerů xylenu, orto-xylen, m-xylen, p-xylen chemická struktura.
Výše uvedené informace jsou upraveny podle Chemicalbook.
Přesná destilace pro separaci o-xylenu a p-xylenu
Xylen je uveden v koksovaném surovém benzenu a ropném krakovaném oleji. Surový benzen po počáteční destilaci, promývání kyselinou sírovou a destilaci pro oddělení benzenu a toluenu, po níž následuje destilace, můžeme získat xylen, známý také jako koksovaný xylen. Kvalita koksovaného xylenu závisí na separační kapacitě destilační kolony, teplotě v horní části kolony a refluxním poměru. Čína rozdělila výrobky z koksovatelného xylenu do tří úrovní. Koksovací xylen obvykle obsahuje 16 % o-xylenu, 50 % m-xylenu, 21 % p-xylenu a 7 % ethylbenzenu. Xylen vyráběný v ropném průmyslu má nízký obsah m-xylenu a vysoký obsah ethylbenzenu. Průmyslový xylen je nejen rozpouštědlem a přísadou gumárenského a nátěrového průmyslu, ale také přísadou leteckého a energetického paliva. O-xylen, m-xylen a p-xylen oddělený z průmyslového xylenu jsou surovinami pro výrobu kyseliny ftalové, kyseliny isoftalové a kyseliny tereftalové. Kyselina ftalová a kyselina tereftalová se používají při výrobě změkčovadel, polyesterových pryskyřic a polyesterových vláken. M-xylen lze použít samostatně jako rozpouštědlo a přísady do paliv. O-xylen obsažený v průmyslovém xylenu se liší od ostatních izomerů o více než 5,2 ℃. Přesnou destilací můžeme získat o-xylen s čistotou přes 95 %, následně se k čištění použije sulfonace a destilace, takže můžeme získat ještě čistší o-xylen.
Xylen patří mezi Lewisovy báze, které mohou tvořit polární komplex s HF-BF3 (Lewisova kyselina). Zásaditost M-xylenu je asi 100krát silnější než zásaditost ostatních aromatických látek C8. Když směs izomerů xylenu přijde do styku s rozpouštědlem HF-BF3, může m-xylen tvořit komplex s fluoridem a je přednostně extrahován do fluoridové fáze. Fluoridová fáze obsahující m-xylen se zahřívá při nižším tlaku, aby se komplex rozložil, čímž se ze směsi oddělí m-xylen. Rozpouštědlo HF-BF3 lze získat zpět destilací pro recyklaci. Pokud je surovinou směs orto-xylenu, m-xylenu a p-xylenu, můžeme po extrakci m-xylenu dále použít přesnou destilaci k oddělení o-xylenu a p-xylenu.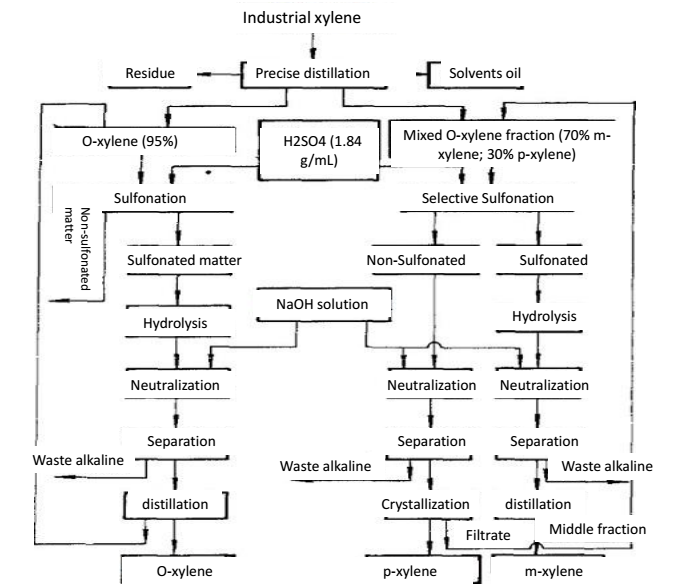
Obrázek 2 metoda přesné destilace pro oddělení o-xylenu a p-xylenu.
Chemické vlastnosti
Jeví se jako bezbarvá průhledná kapalina s aromatickým zápachem. Je mísitelný s ethanolem, ethyletherem, acetonem a benzenem, ale nerozpustný ve vodě.
Použití
(1) Používá se zejména při výrobě ftalanhydridu
(2) O-xylen je surovinou pro výrobu germicidu fenraminu, tetrachlorfenylpeptidu a herbicidu bensulfuron-methylu. Používá se jako meziprodukt pro výrobu kyseliny o-methylbenzoové.
(3) Používá se hlavně jako chemická surovina a rozpouštědlo. Lze jej použít k výrobě ftalanhydridu, barviv, pesticidů a léčiv, například vitaminů. Může se také používat jako aditiva do leteckého benzinu.
(4) Používá se jako chromatografické standardy a rozpouštědla
(5) Jako surovina pro syntézu anhydridu a další organické syntézy;
Způsob výroby
Průmysl používá superdestilační metodu k oddělení o-xylenu od směsného xylenu. O-xylen má v porovnání s ostatními složkami ve směsném xylenu rozdíl v bodu varu přes 5 ℃. Pro destilaci je zapotřebí asi 150 zásobníků, refluxní poměr je 5-8 a spotřebuje se relativně hodně energie.
O-xylen se původně vyráběl hlavně z uhelného dehtu. V současné době se většina domácí i zahraniční výroby o-xylenu uskutečňuje především extrakcí z ropy katalytickým reformingem a tepelným krakováním aromatických uhlovodíků. Díky tomu jsou si struktury o-xylenu, p-xylenu a m-xylenu v xylenu velmi podobné; jejich fyzikální parametry jsou také dosti podobné. Při průmyslové separaci o-xylenu se používá hlavně metoda superdestilace; nejprve se oddělí o-xylen a ethylbenzen od směsného xylenu, což vyžaduje použití destilační věže se 100 ~ 150 zásobníky; následně se oddělí o-xylen a ethylbenzen, aby se získal čistý o-xylen.
Kategorie
Hořlavé kapaliny
Třída toxicity
otravy
Akutní toxicita
Perorální – potkan LDL0: 5000 mg/kg; břišní injekce – myš LD50: Výbušnost: 1364 mg/kg
Výbušnost a nebezpečné vlastnosti
výbušný ve směsi se vzduchem
Hořlavost a nebezpečné vlastnosti
hořlavý při působení plamene, tepla, oxidantů Hořlavý při hoření uvolňuje dráždivý kouř
Skladování a přepravní vlastnosti
sklad: větraný, nízkoteplotní a suchý; opatrně nakládat a vykládat; skladovat odděleně od oxidantů a kyselin.
Hasicí prostředky
mlha voda, pěna, písek, oxid uhličitý, 1211 hasivo
Pracovní norma
TLV-TWA 100 PPM (440 mg/m 3); STEL 150; PPM (655 mg/m 3)
Chemické vlastnosti
bezbarvá kapalina
Fyzikální vlastnosti
Čirá, bezbarvá kapalina aromatického zápachu. Prahovou koncentraci zápachu 380 ppbv uvedli Nagata a Takeuchi (1990).
Použití
Příprava kyseliny ftalové, ftalanhydridu, kyseliny tereftalové, kyseliny isoftalové; rozpouštědlo pro alkydové pryskyřice, laky, emaily, kaučukové cementy; výroba barviv, léčiv a insekticidů; motorová paliva.
Definice
ChEBI: xylen substituovaný methylovými skupinami v polohách 1 a 3.
Syntéza Reference(s)
Journal of the American Chemical Society, 97, s. 7262, 1975 DOI: 10.1021/ja00858a011
The Journal of Organic Chemistry, 44, s. 2185, 1979 DOI: 10.1021/jo01327a032
Všeobecný popis
Bezbarvá vodnatá kapalina sladkého zápachu. Méně hustá než voda. Nerozpustná ve vodě. Dráždivé páry.
Vzduch & Voda Reakce
Vysoce hořlavý. Nerozpustný ve vodě.
Profil reaktivity
1,2-dimethylbenzen může reagovat s oxidačními materiály. .
Zdravotní nebezpečnost
Výpary způsobují bolesti hlavy a závratě. Kapalina dráždí oči a kůži. Při vniknutí do plic způsobuje silný kašel, úzkost a rychle se rozvíjející plicní edém. Při požití způsobuje nevolnost, zvracení, křeče, bolesti hlavy a kóma. Může být smrtelný. Může dojít k poškození ledvin a jater.
Nebezpečí požáru
Chování při požáru: Páry jsou těžší než vzduch a mohou se dostat na značnou vzdálenost ke zdroji vznícení a vzplanout.
Chemická reaktivita
Reaktivita s vodou Bez reakce; Reaktivita s běžnými materiály: Žádná reakce; Stabilita během přepravy: Stabilní; Neutralizační činidla pro kyseliny a žíraviny: Není relevantní; Polymerace: Není relevantní; Inhibitor polymerace: Není relevantní.
Bezpečnostní profil
Středně toxický bj7intraperitoneální cestou. Mírně toxický při požití a vdechnutí. Experimentálníteratogen. Běžná látka znečišťující ovzduší. Velmi nebezpečné nebezpečí požáru při vystavení teplu nebo plameni. Výbušný ve formě par při vystavení teplu nebo plameni. K hašení požáru použijte pěnu, CO2, suchou chemikálii. neslučitelný s oxidačními materiály. při zahřátí k rozkladu uvolňuje štiplavý kouř a dráždivé výpary. Uvolňuje se z moderních stavebních materiálů (CENEAR69,22,91). Viz také další položky o xylenu.
Zdroj
Zjištěno v destilované vodě rozpustné frakci 87 oktanového benzinu (3,83 mg/l), 94 oktanového benzinu (11,4 mg/l), Gasoholu (8,49 mg/l), topném oleji č. 2 (1,73 mg/l), leteckém palivu A (0,5 mg/l).87 mg/l), motorová nafta (1,75 mg/l), vojenské tryskové palivo JP-4 (1,99 mg/l) (Potter, 1996), nový motorový olej (16,2 až 17,5 μg/l) a použitý motorový olej (294 až 308 μg/l) (Chen et al..), 1994). Průměrné objemové procento a odhadovaná molární frakce v benzínu PS-6 Amerického ropného institutu jsou 2,088 a 0,01959 (Poulsen et al., 1992). Schauer et al. (1999) zaznamenali o-xylen ve výfukových plynech středně těžkého nákladního automobilu s naftovým motorem v množství emisí 830 μg/km. Motorová nafta získaná ze servisní stanice ve švýcarském Schlierenu obsahovala o-xylen v koncentraci 223 mg/l (Schluep etal., 2001).
Kalifornský reformulovaný benzin fáze II obsahoval o-xylen v koncentraci 19,7 g/kg.
Míra emisí z výfuku benzinových automobilů s katalyzátory a bez katalyzátorů byla 5,41 a 562 mg/km (Schauer et al.,
Thomas a Delfino (1991) ekvilibrovali podzemní vodu bez kontaminantů odebranou v Gainesville na Floridě s jednotlivými frakcemi tří jednotlivých ropných produktů při teplotě 24-25 °C po dobu 24 h. Vodná fáze byla analyzována na organické sloučeniny pomocí zkušební metody602 schválené U.S. EPA. Průměrné koncentrace m+p-xylenu zaznamenané ve frakcích bezolovnatého benzinu, petroleje a motorové nafty rozpustných ve vodě byly 8,611, 0,658 a 0,228 mg/l. Když autoři analyzovali vodnou fázi pomocí zkušební metody 610 schválené U.S. EPA, byly průměrné koncentrace m+p-xylenu ve frakcích bezolovnatého benzinu, petroleje a motorové nafty rozpustných ve vodě nižší, tj. 6,068, 0,360 a 0,222 mg/l. Na základě laboratorní analýzy 7 vzorků uhelného dehtu se koncentrace o-xylenu pohybovaly od 2 do 2 000 ppm (EPRI, 1990). Vysokoteplotní uhelný dehet obsahoval o-xylen v průměrné koncentraci 0,04 % hmot. (McNeil, 1983).
Schauer et al. (2001) měřili míru emisí organických sloučenin pro těkavé organické sloučeniny, polotěkavé organické sloučeniny v plynné fázi a organické sloučeniny v částicové fázi ze spalování borovice, dubu a eukalyptu v domácnostech (v krbu). Emise o-xylenu v plynné fázi činily 18,1 mg/kg spálené borovice. Míra emisí o-xylenu nebyla při spalování dubu a eukalyptu měřena.
Norma pro pitnou vodu (konečná): Pro všechny xyleny jsou MCLG i MCL 10 mg/l. Kromě toho byla doporučena hodnota DWEL 70 mg/l (U.S. EPA, 2000).
Výskyt v životním prostředí
Biologický. Uváděné produkty biodegradace komerčního přípravku obsahujícího xylenzahrnují α-hydroxy-p-toluovou kyselinu, p-methylbenzylalkohol, benzylalkohol, 4-methylkatechol, mandp-toluové kyseliny (Fishbein, 1985). o-Xylen byl také kometabolizován, což vedlo ke vzniku kyseliny o-toluové (Pitter a Chudoba, 1990). V anoxických podzemních vodách poblíž Bemidji, MI, se o-xylenanaerobní bázi biologicky rozkládal na meziprodukt kyselinu o-toluovou (Cozzarelli et al., 1990). V podzemních vodách kontaminovaných benzínem byla jako první meziprodukt při anaerobní degradaci xylenů identifikována kyselina methylbenzylsukcinová (Reusser a Field, 2002).
Fotolytická. Cox et al. (1980) uvedli rychlostní konstantu 1,33 x 10-11 cm3/molekulu?s pro reakci plynného o-xylenu s OH radikály na základě hodnoty 8 x 10-12 cm3/molekulu?s pro reakci ethylenu s OH radikály.
Povrchová voda. Poločas vypařování o-xylenu v povrchové vodě (hloubka 1 m) při 25 °C se odhaduje na 5,18 h (Mackay a Leinonen, 1975).
Podzemní voda. Nielsen et al. (1996) studovali rozklad o-xylenu v mělkém, glaciofluviálním, neohraničeném písčitém vodonosníku v Jutsku v Dánsku. V rámci studie mikrokosmu in situ byl skrz zahloubený vrt přibližně 5 m pod úrovní terénu instalován válec, který byl dole otevřený a nahoře stíněný. Pět litrů vody bylo provzdušněno atmosférickým vzduchem, aby byly zachovány aerobní podmínky. Podzemní voda byla analyzována každý týden po dobu přibližně 3 měsíců za účelem stanovení koncentrace o-xylenu v čase. Experimentálně stanovená rychlostní konstanta biodegradace prvního řádu a odpovídající poločas rozpadu po 7denní lag fázi byly 0,1/d a 6,93 d.
Fotolytická. Když byl syntetický vzduch obsahující plynnou kyselinu dusičnou a o-xylen vystaven umělému slunečnímu světlu (λ = 300-450 nm), vznikaly jako produkty biacetyl, peroxyacetalnitrát a methylnitrát (Cox et al., 1980). Roztok n-hexanu obsahující o-xylen a nanesený jako tenký film (4 mm) na studenou vodu (10 °C) byl ozářen rtuťovou středotlakou lampou. Za 3 h se 13,6 % o-xylenu fotooxidovalo na o-methylbenzaldehyd, o-benzylalkohol, kyselinu o-benzoovou a o-methylacetofenon (Moza a Feicht, 1989). Ozáření o-xylenu při ≈ 2537 ? při 35 °C a 6 mmHg izomeruje na m-xylen (Calvert a Pitts, 1966). Glyoxal, methylglyoxal a biacetyl vznikly fotooxidací o-xylenu OH radikály na vzduchu při 25 °C (Tuazon et al.,1986a).
Chemické/fyzikální. Za atmosférických podmínek vedla reakce o-xylenu v plynné fázi s OHradikály a oxidy dusíku ke vzniku o-tolualdehydu, o-methylbenzylnitrátu, nitro-oxylenů, 2,3- a 3,4-dimethylfenolu (Atkinson, 1990). Kanno et al. (1982) studovali vodnou reakci o-xylenu a dalších aromatických uhlovodíků (benzenu, toluenu, m- a p-xylenu a naftalenu) s kyselinou chloristou v přítomnosti amonného iontu. Uvádějí, že aromatický kruh nebyl chlorován, jak se očekávalo, ale byl štěpen chloraminem za vzniku kyanogenchloridu. Množství vzniklého kyanogenchloridu se zvyšovalo při nižších hodnotách pH (Kanno et al., 1982). V plynné fázi reagoval o-xylen s nitrátovými radikály v čištěném vzduchu za vzniku těchto produktů: 5-nitro-2-methyltoluen a 6-nitro-2-methyltoluen, o-methylbenzaldehyd a arylnitrát (Chiodini et al., 1993).
Metody čištění
o-Xylen (4,4 kg) se sulfonuje mícháním po dobu 4 hodin s 2,5 l konc H2SO4 při 95o. Po ochlazení a oddělení nesulfonovaného materiálu se produkt zředí 3 l vody a neutralizuje 40% NaOH. Po ochlazení se oddělí o-xylensulfonát sodný, který se rekrystalizuje z poloviny své hmotnosti ve vodě. Sůl se rozpustí v minimálním množství studené vody, poté se smíchá se stejným množstvím studené vody a se stejným objemem konc H2SO4 a zahřeje se na 110o. o-xylen se regeneruje a destiluje s vodní parou. Destilát se nasytí NaCl, organická vrstva se oddělí, vysuší a redestiluje.
