15.4 Fyzikální vlastnosti karboxylových kyselin
Cíl výuky
- Porovnat teploty varu karboxylových kyselin s alkoholy o podobné molární hmotnosti.
- Porovnat rozpustnost karboxylových kyselin ve vodě s rozpustností srovnatelných alkanů a alkoholů ve vodě.
Mnohé karboxylové kyseliny jsou bezbarvé kapaliny s nepříjemným zápachem. Všechny karboxylové kyseliny s 5 až 10 atomy uhlíku mají „kozí“ zápach (což vysvětluje zápach sýra Limburger). Tyto kyseliny vznikají také působením kožních bakterií na lidský maz (kožní oleje), což vysvětluje zápach špatně větraných šaten. Kyseliny s více než 10 atomy uhlíku jsou pevné látky podobné vosku a jejich zápach se zmenšuje s rostoucí molární hmotností a následnou klesající těkavostí.
Karboxylové kyseliny vykazují silnou vodíkovou vazbu mezi molekulami. Proto mají ve srovnání s jinými látkami srovnatelné molární hmotnosti vysoké teploty varu.
Karboxylová skupina se snadno zapojuje do vodíkové vazby s molekulami vody (obrázek 15.3 „Vodíková vazba mezi molekulou kyseliny octové a molekulami vody“). Kyseliny s jedním až čtyřmi atomy uhlíku jsou s vodou zcela mísitelné. S rostoucí délkou uhlíkového řetězce rozpustnost klesá, protože dipólové síly ztrácejí na významu a převažují disperzní síly. Kyselina hexanová je ve vodě sotva rozpustná (asi 1,0 g/100 g vody). Kyselina palmitová , která má velkou nepolární uhlovodíkovou složku, je ve vodě v podstatě nerozpustná. Karboxylové kyseliny jsou obecně rozpustné v takových organických rozpouštědlech, jako je ethanol, toluen a diethylether.
Obrázek 15: Rozpustnost v organických rozpouštědlech.3 Vodíková vazba mezi molekulou kyseliny octové a molekulou vody
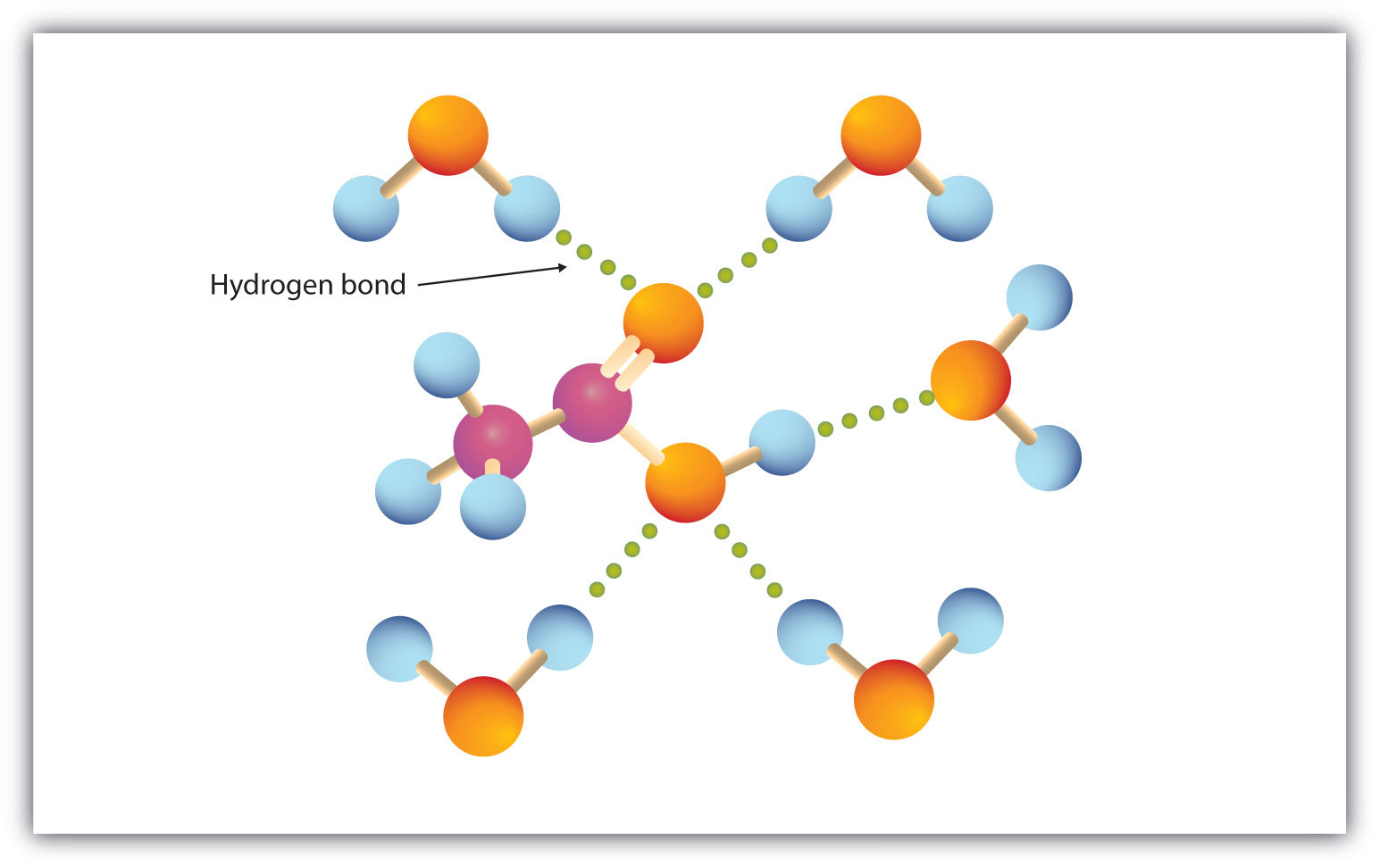
Karboxylové kyseliny s nízkou molární hmotností jsou ve vodě poměrně dobře rozpustné.
Tabulka 15.2 „Fyzikální konstanty karboxylových kyselin“ uvádí některé fyzikální vlastnosti vybraných karboxylových kyselin. Prvních šest je homologních. Všimněte si, že teploty varu se zvyšují s rostoucí molární hmotností, ale teploty tání nevykazují žádný pravidelný průběh.
Tabulka 15.2 Fyzikální konstanty karboxylových kyselin
| Kondenzovaný strukturní vzorec | Název kyseliny | Teplota tání (°C) | Teplota varu (°C) | Rozpustnost (g/100 g vody) |
|---|---|---|---|---|
| HCOOH | kyselina mravenčí | 8 | 100 | mísitelná |
| CH3COOH | kyselina octová | 17 | 118 | mísitelná |
| CH3CH2COOH | kyselina propionová | -22 | 141 | mísitelná |
| CH3(CH2)2COOH | kyselina máselná | -5 | 163 | mísitelná |
| CH3(CH2)3COOH | kyselina valerová | -35 | 187 | 5 |
| CH3(CH2)4COOH | kyselina kapronová | -3 | 205 | 1.1 |
| C6H5COOH | kyselina benzoová | 122 | 249 | 0.29 |
Cvičení na přehled pojmů
-
Která sloučenina má vyšší bod varu – kyselina butanová (molární hmotnost 88) nebo 2-pentanon (molární hmotnost 86)? Vysvětlete.
-
Předpokládáte, že kyselina máselná (kyselina butanová) je ve vodě rozpustná více nebo méně než 1-butanol? Vysvětlete.
Odpovědi
-
kyselina máselná kvůli vodíkové vazbě (Ve 2-pentanonu neexistuje mezimolekulární vodíková vazba.)
-
rozpustnější, protože je zde rozsáhlejší vodíková vazba
Klíčové poznatky
- Karboxylové kyseliny mají ve srovnání s jinými látkami srovnatelné molární hmotnosti vysoké teploty varu. Bod varu se zvyšuje s molární hmotností.
- Karboxylové kyseliny, které mají jeden až čtyři atomy uhlíku, jsou zcela mísitelné s vodou. Rozpustnost klesá s molární hmotností.
Cvičení
-
Která sloučenina má vyšší bod varu – CH3CH2CH2OCH2CH3 nebo CH3CH2CH2COOH? Vysvětlete.
-
Která sloučenina má vyšší bod varu-CH3CH2CH2CH2CH2OH nebo CH3CH2CH2COOH? Vysvětlete.
-
Která sloučenina je rozpustnější ve vodě-CH3COOH nebo CH3CH2CH2CH3? Vysvětlete.
-
Která sloučenina je rozpustnější ve vodě-CH3CH2COOH nebo CH3CH2CH2CH2CH2COOH? Vysvětlete.
Odpovědi
-
CH3CH2CH2COOH kvůli vodíkové vazbě (U CH3CH2CH2OCH2CH3 neexistuje mezimolekulární vodíková vazba.)
-
CH3COOH, protože se zapojuje do vodíkové vazby s vodou (S CH3CH2CH2CH3 neexistuje mezimolekulární vodíková vazba.)
